工业上利用反应:N2(g)+3H2(g) 2NH3(g)合成氨气。已知在1×105Pa和25℃时,拆开1molN≡N键和1molH—H键所需能量分别为946kJ和436kJ,生成1molN—H键放出的能量为391kJ。回答下列问题:
2NH3(g)合成氨气。已知在1×105Pa和25℃时,拆开1molN≡N键和1molH—H键所需能量分别为946kJ和436kJ,生成1molN—H键放出的能量为391kJ。回答下列问题:
(1)根据上述数据判断,在1×105Pa和25℃时,工业合成氨的反应是_______ 反应(填“吸热”或“放热”);
(2)每消耗1molN2,反应放出或吸收的热量Q1为_______ kJ;
(3)1molN2和3molH2在该条件下反应,达平衡时,放出或吸收的热量为Q2kJ,则Q2_______ Q1(填“>”“<”或“=”)。
 2NH3(g)合成氨气。已知在1×105Pa和25℃时,拆开1molN≡N键和1molH—H键所需能量分别为946kJ和436kJ,生成1molN—H键放出的能量为391kJ。回答下列问题:
2NH3(g)合成氨气。已知在1×105Pa和25℃时,拆开1molN≡N键和1molH—H键所需能量分别为946kJ和436kJ,生成1molN—H键放出的能量为391kJ。回答下列问题:(1)根据上述数据判断,在1×105Pa和25℃时,工业合成氨的反应是
(2)每消耗1molN2,反应放出或吸收的热量Q1为
(3)1molN2和3molH2在该条件下反应,达平衡时,放出或吸收的热量为Q2kJ,则Q2
更新时间:2022-09-25 19:21:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】学习化学反应原理能够指导促进人类生活质量的提高。
(1)氢气是最理想的能源。一定质量的氢气完全燃烧,生成液态水时放出热量比气态水___________ (填“多”或“少”)。 氢气完全燃烧放出热量
氢气完全燃烧放出热量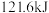 ,其中断裂
,其中断裂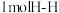 键吸收
键吸收 ,断裂
,断裂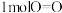 键吸收
键吸收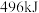 ,则形成
,则形成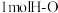 键放出热量
键放出热量___________  。
。
(2)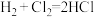 反应中能量变化如图所示。该反应
反应中能量变化如图所示。该反应___________ (填“放出”或“吸收”) ___________  的热量,为
的热量,为___________ 反应。

(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池。某兴趣小组拟将刻蚀电路板的反应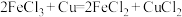 设计成原电池,则负极所用电极材料为
设计成原电池,则负极所用电极材料为___________ ,当线路中转移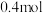 电子时,则被腐蚀铜的质量为
电子时,则被腐蚀铜的质量为___________ g。
(4)目前,氢氧燃料电池得到了广泛的应用,其反应原理示意图如图。
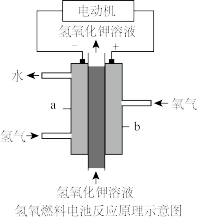
①a为燃料电池的___________ (填“正”或“负”)极。
②该电池的总反应为___________ 。
③电池工作过程中, 将移向
将移向___________ (填“正”或“负”)极。
(1)氢气是最理想的能源。一定质量的氢气完全燃烧,生成液态水时放出热量比气态水
 氢气完全燃烧放出热量
氢气完全燃烧放出热量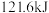 ,其中断裂
,其中断裂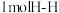 键吸收
键吸收 ,断裂
,断裂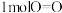 键吸收
键吸收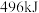 ,则形成
,则形成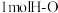 键放出热量
键放出热量 。
。(2)
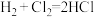 反应中能量变化如图所示。该反应
反应中能量变化如图所示。该反应 的热量,为
的热量,为
(3)理论上讲,任何自发的氧化还原反应都可以设计成原电池。某兴趣小组拟将刻蚀电路板的反应
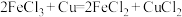 设计成原电池,则负极所用电极材料为
设计成原电池,则负极所用电极材料为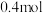 电子时,则被腐蚀铜的质量为
电子时,则被腐蚀铜的质量为(4)目前,氢氧燃料电池得到了广泛的应用,其反应原理示意图如图。

①a为燃料电池的
②该电池的总反应为
③电池工作过程中,
 将移向
将移向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)有①168 O 、17 8O 、188O ;②H2、D2、T2;③石墨、金刚石;④11H 、21H、31H;四组微粒或物质。互为同位素的是________ (填编号,下同),互为同素异形体的是_________ 。
(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391kJ。则由氢气和氮气反应生成1 mol NH3需要___________ (填“放出”或“吸收”)____________ k J能量。
(3)如图为原电池装置示意图:
①若A为Zn,B为Cu,电解质溶液为稀硫酸,则A电极名称为_______ (填“正极”或“负极”),写出正极电极反应式:___________ 。
②若A为铜片,B为铁片,电解质为CuSO4溶液,则铜片为___________ (填“正极”或“负极”),写出负极电极反应式:_________________________ 。
(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391kJ。则由氢气和氮气反应生成1 mol NH3需要
(3)如图为原电池装置示意图:

①若A为Zn,B为Cu,电解质溶液为稀硫酸,则A电极名称为
②若A为铜片,B为铁片,电解质为CuSO4溶液,则铜片为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】合成氨技术的创立开辟了人工固氮的重要途径。
(1)我国科学家研究了在铁掺杂W18O19纳米反应器催化剂表面上实现常温低电位合成氨,反应历程如图,其中吸附在催化剂表面的物种用*标注。需要吸收能量最大的能垒E=___________ eV。

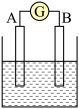
一定条件下,在体积为5L的密闭容器中,ABC三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。
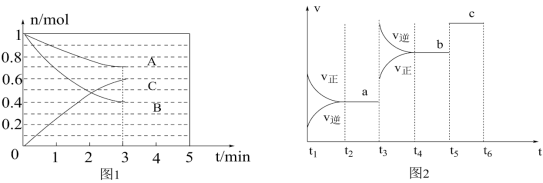
(2)该反应的化学方程式为___________ 。
(3)该反应的反应速率v随时间t的变化关系如图2所示,根据图判断,在t3时刻改变的外界条件是___________ 。
(1)我国科学家研究了在铁掺杂W18O19纳米反应器催化剂表面上实现常温低电位合成氨,反应历程如图,其中吸附在催化剂表面的物种用*标注。需要吸收能量最大的能垒E=

一定条件下,在体积为5L的密闭容器中,ABC三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达到平衡后,降低温度,A的体积分数将减小。

(2)该反应的化学方程式为
(3)该反应的反应速率v随时间t的变化关系如图2所示,根据图判断,在t3时刻改变的外界条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】书写下列化学方程式
(1)下图是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式___________ 。

(2)已知:C(s) + O2(g) = CO2(g) ΔH=-437.3 kJ•mol-1
H2(g) +1/2O2(g) = H2O(g) ΔH=-285.8 kJ•mol-1
CO(g) +1/2O2(g) = CO2(g) ΔH=-283.0 kJ•mol-1
则固态碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是___________ 。
(3)已知拆开1mol H-H键、1molN≡N和1mol N—H键分别需要的能量是436kJ、948kJ、391 kJ。则N2、H2合成NH3的热化学方程式为:___________ 。
(4)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一。已知存在如下反应:
i.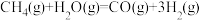

ii.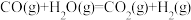

iii.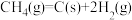

……
iii为积炭反应,利用 和
和 计算
计算 时,还需要利用
时,还需要利用___________ 反应的 。
。
(1)下图是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式

(2)已知:C(s) + O2(g) = CO2(g) ΔH=-437.3 kJ•mol-1
H2(g) +1/2O2(g) = H2O(g) ΔH=-285.8 kJ•mol-1
CO(g) +1/2O2(g) = CO2(g) ΔH=-283.0 kJ•mol-1
则固态碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是
(3)已知拆开1mol H-H键、1molN≡N和1mol N—H键分别需要的能量是436kJ、948kJ、391 kJ。则N2、H2合成NH3的热化学方程式为:
(4)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一。已知存在如下反应:
i.
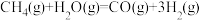

ii.
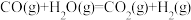

iii.
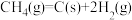

……
iii为积炭反应,利用
 和
和 计算
计算 时,还需要利用
时,还需要利用 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】当前能源危机是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法不利于能源“开源节流”的是________ (填字母)。
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗、增加资源的重复使用和资源的循环再生

(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,_________ (填 “金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH=______________ 。
(3)N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为_____ 。
(4)综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:_______________ 。
(1)下列做法不利于能源“开源节流”的是
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗、增加资源的重复使用和资源的循环再生

(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,
(3)N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为
(4)综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。
(1)汽油在不同空/燃比(空气与燃油气的体积比)时尾气的主要成分不同,空/燃比较小时的有毒气体主要是_____ (填化学式)。
(2)人们把拆开1 mol化学键所吸收的能量看成该化学键的键能。
已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。
查阅资料获知如下反应的热化学方程式:
N2(g)+O2(g)=2NO(g) ΔH=+180 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+68 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
① 一定条件下,N2与O2反应生成NO能够自发进行,其原因是______ ;NO分子中化学键的键能为_______ kJ·mol—1。
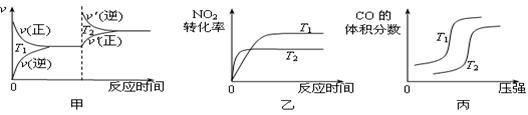
② CO与NO2反应的热化学方程式为4CO(g)+2NO2(g)=4CO2(g)+N2(g) ΔH=______ 。对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是______ (填代号)。
(1)汽油在不同空/燃比(空气与燃油气的体积比)时尾气的主要成分不同,空/燃比较小时的有毒气体主要是
(2)人们把拆开1 mol化学键所吸收的能量看成该化学键的键能。
已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。
查阅资料获知如下反应的热化学方程式:
N2(g)+O2(g)=2NO(g) ΔH=+180 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+68 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
① 一定条件下,N2与O2反应生成NO能够自发进行,其原因是
② CO与NO2反应的热化学方程式为4CO(g)+2NO2(g)=4CO2(g)+N2(g) ΔH=

您最近一年使用:0次



