当前能源危机是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法不利于能源“开源节流”的是________ (填字母)。
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗、增加资源的重复使用和资源的循环再生

(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,_________ (填 “金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH=______________ 。
(3)N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为_____ 。
(4)综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:_______________ 。
(1)下列做法不利于能源“开源节流”的是
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
D.减少资源消耗、增加资源的重复使用和资源的循环再生

(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。则在通常状况下,金刚石和石墨相比较,
(3)N2、O2分子中化学键的键能分别是946 kJ/mol、497kJ/mol。已知:N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol。NO分子中化学键的键能为
(4)综合上述有关信息,请写出用CO除去NO生成无污染气体的热化学方程式:
更新时间:2018-07-19 20:55:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知下列热化学方程式:
①H2(g)+1/2O2(g)=H2O(l) ΔH =-285.8 kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH =-241.8 kJ/mol
③C(s)+1/2O2(g)=CO(g) ΔH =-110.5 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ/mol
回答下列问题:
(1)H2的燃烧热ΔH=_______ ;C的燃烧热为__________ 。
(2)燃烧1 g H2生成液态水,放出的热量为_________ 。
(3)已知CO的燃烧热为283.0 kJ/mol,现有CO、H2和CO2组成的混合气体116.8 L(标准状况),完全燃烧后放出总热量为867.9 kJ,且生成18 g液态水,则混合气体中H2为_________ L,CO在混合气体中的体积分数约为_________ (精确至小数点后一位)。
①H2(g)+1/2O2(g)=H2O(l) ΔH =-285.8 kJ/mol
②H2(g)+1/2O2(g)=H2O(g) ΔH =-241.8 kJ/mol
③C(s)+1/2O2(g)=CO(g) ΔH =-110.5 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ/mol
回答下列问题:
(1)H2的燃烧热ΔH=
(2)燃烧1 g H2生成液态水,放出的热量为
(3)已知CO的燃烧热为283.0 kJ/mol,现有CO、H2和CO2组成的混合气体116.8 L(标准状况),完全燃烧后放出总热量为867.9 kJ,且生成18 g液态水,则混合气体中H2为
您最近一年使用:0次
【推荐2】(1)101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ热量,氢气的燃烧热△H =_______ ;氢气燃烧的热化学方程式为_______ 。
(2)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
①倒入NaOH溶液的正确操作是________ (填选项字母,下同)。
A.沿玻璃棒缓慢倒入
B.一次性迅速倒入
C.分三次少量倒入
②使硫酸与NaOH溶液混合均匀的正确操作是_______ 。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(3)工业合成氨反应为N2(g)+3H2(g)⇌2NH3(g),一定条件下,在2 L密闭容器中进行实验,测得有关数据如下表所示:
则0〜10 s内,用氢气的浓度变化表示的平均反应速率是_______ ,该反应的化学平衡常数是_________ 。根据混合气体各成分的物质性质,你认为工业上将氨气从混合气体中分离出来的措施是_______ ,从而达到反应气体循环利用的目的。
(2)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
①倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入
B.一次性迅速倒入
C.分三次少量倒入
②使硫酸与NaOH溶液混合均匀的正确操作是
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(3)工业合成氨反应为N2(g)+3H2(g)⇌2NH3(g),一定条件下,在2 L密闭容器中进行实验,测得有关数据如下表所示:
| 物质 | N2(g) | H2(g) | NH3(g) |
| 起始(mol) | 2 | 7 | 0 |
| 10 s(mol) | 1.6 | ||
| 平衡时(mol) | 2 |
则0〜10 s内,用氢气的浓度变化表示的平均反应速率是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 ΔH=88.6kJ/mol
ΔH=88.6kJ/mol
则M、N相比,较稳定的是________ 。
(2)已知CH3OH(l)的燃烧热为726.5kJ·mol-1,CH3OH(l)+ O2(g)===CO2(g)+2H2(g) ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g) ΔH=-akJ·mol-1,则a________ 726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:______________________________________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 ΔH=88.6kJ/mol
ΔH=88.6kJ/mol则M、N相比,较稳定的是
(2)已知CH3OH(l)的燃烧热为726.5kJ·mol-1,CH3OH(l)+
 O2(g)===CO2(g)+2H2(g) ΔH=-akJ·mol-1,则a
O2(g)===CO2(g)+2H2(g) ΔH=-akJ·mol-1,则a(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1) 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下: ,则S(单斜,s)、S(斜方,s)相比,较稳定的是
,则S(单斜,s)、S(斜方,s)相比,较稳定的是___________ [填“S(单斜,s)”或“S(斜方、s)”]。
(2)下表中的数据表示破坏 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 )。
)。
热化学方程式: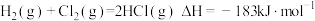 ,则
,则 键的键能为
键的键能为___________  。
。
(3)标准状况下,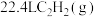 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出
,放出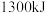 热量,请写出该反应的热化学方程式:
热量,请写出该反应的热化学方程式:___________ 。
(4)已知: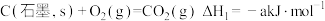
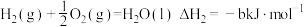
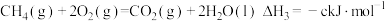
计算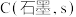 与
与 反应生成
反应生成 的
的 为
为___________ (用含a、b、c的式子表示) 。
。
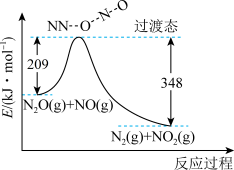
(5) 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成
的能量变化如图所示。则反应过程中,每生成 理论上放出的热量为
理论上放出的热量为___________
(1)
 分子可形成单斜硫和斜方硫,转化过程如下:
分子可形成单斜硫和斜方硫,转化过程如下: ,则S(单斜,s)、S(斜方,s)相比,较稳定的是
,则S(单斜,s)、S(斜方,s)相比,较稳定的是(2)下表中的数据表示破坏
 化学键需消耗的能量(即键能,单位为
化学键需消耗的能量(即键能,单位为 )。
)。| 化学键 |  |  |
| 键能 | 436 | 431 |
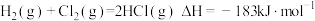 ,则
,则 键的键能为
键的键能为 。
。(3)标准状况下,
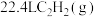 在
在 中完全燃烧生成
中完全燃烧生成 和
和 ,放出
,放出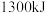 热量,请写出该反应的热化学方程式:
热量,请写出该反应的热化学方程式:(4)已知:
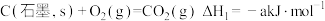
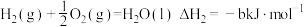
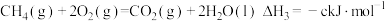
计算
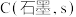 与
与 反应生成
反应生成 的
的 为
为 。
。(5)
 和
和 反应生成
反应生成 和
和 的能量变化如图所示。则反应过程中,每生成
的能量变化如图所示。则反应过程中,每生成 理论上放出的热量为
理论上放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)已知在高温、高压、催化剂作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量。
①石墨和金刚石________ 能量高,________ 更稳定。
②推测石墨与金刚石各1 mol在相同条件下燃烧,________ 放出的热量多。
(2)①司机是否酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应为2CrO3(红色)+3C2H5OH+3H2SO4====Cr2(SO4)3(绿色)+3CH3CHO+6H2O。
被检测的气体的成分是_______ ,上述反应中的氧化剂是_______ 。还原剂是_______ 。
②1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列_________ 事实(填入编号)。
a.苯不能使溴的四氯化碳溶液褪色 b.苯能与H2发生加成反应 c.苯没有同分异构体 d.邻二溴苯只有一种
现代化学认为苯分子碳碳之间的键是__________________ 。
①石墨和金刚石
②推测石墨与金刚石各1 mol在相同条件下燃烧,
(2)①司机是否酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应为2CrO3(红色)+3C2H5OH+3H2SO4====Cr2(SO4)3(绿色)+3CH3CHO+6H2O。
被检测的气体的成分是
②1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列
a.苯不能使溴的四氯化碳溶液褪色 b.苯能与H2发生加成反应 c.苯没有同分异构体 d.邻二溴苯只有一种
现代化学认为苯分子碳碳之间的键是
您最近一年使用:0次
【推荐3】(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的△H(化学计量数相同)分别为△H1、△H2,△H1_____ △H2(填“>”“<”或“=”,下同)。
(2)相同条件下,1 mol P4所具有的能量_______ 4 mol P原子所具有的能量。
(3)已知P4(白磷,s) 4P(红磷,s)△H=-17 kJ· mol-1,比较下列反应中△H的大小:△H1
4P(红磷,s)△H=-17 kJ· mol-1,比较下列反应中△H的大小:△H1_____ △H2。
①P4(白磷,s)+5O2(g)=P4O10(s)△H1,
②4P(红磷,s)+5O2(g)=P4O10(s)△H2。
(4)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ· mol-1,则浓硫酸与稀氢氧化钠溶液反应生成2 mol水,放出的热量______ 114.6kJ。
(5)已知:28gFe(s)与CO2(g)在一定条件下,完全反应生成FeO(s)和CO(g),吸收了a kJ热量,该反应的热化学方程式是___________________________________ 。
(2)相同条件下,1 mol P4所具有的能量
(3)已知P4(白磷,s)
 4P(红磷,s)△H=-17 kJ· mol-1,比较下列反应中△H的大小:△H1
4P(红磷,s)△H=-17 kJ· mol-1,比较下列反应中△H的大小:△H1①P4(白磷,s)+5O2(g)=P4O10(s)△H1,
②4P(红磷,s)+5O2(g)=P4O10(s)△H2。
(4)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ· mol-1,则浓硫酸与稀氢氧化钠溶液反应生成2 mol水,放出的热量
(5)已知:28gFe(s)与CO2(g)在一定条件下,完全反应生成FeO(s)和CO(g),吸收了a kJ热量,该反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】石灰石脱硫法是以石灰石为原料通过系列反应将硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:CaSO4 (s)+CO (g) =CaO(s)+SO2 (g)+CO2 (g) ΔH1=+218.4 kJ·mol-1(反应Ⅰ),CaSO4(s)+4CO(g)=CaS(s)+4CO2(g) ΔH2=-175.6 kJ·mol-1(反应Ⅱ),结合反应Ⅰ、Ⅱ写出CaSO4(s)与CaS(s)的反应的热化学方程式_______________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】依据事实,写出下列反应的热化学方程式.
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为______________ 。
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ______________ 。
(3)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
根据键能数据,计算并写出CH4(g)与F2(g)反应生CF4(g)和另一种气体的热化学方程式:_________________________________ ;
(4)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe (s)+3CO(g) ΔH 1=+489.0 kJ· mol-1,
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1,则CO还原Fe2O3(s)的热化学方程式为_______________________________________________________ 。
(5)在298K下,C、Al的单质各1mol完全燃烧,分别放出热量m kJ和n kJ。又知一定条件下,Al能将C从CO2置换出来,写出此置换反应的热化学方程式__________________ ;
(6)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:

1 mol NH4+(aq) 全部氧化成NO3-(aq)的热化学方程式是________________________ 。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ
(3)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
| 化学键 | C—H | C—F | H—F | F—F |
| 键能 | 414 | 489 | 565 | 158 |
(4)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe (s)+3CO(g) ΔH 1=+489.0 kJ· mol-1,
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1,则CO还原Fe2O3(s)的热化学方程式为
(5)在298K下,C、Al的单质各1mol完全燃烧,分别放出热量m kJ和n kJ。又知一定条件下,Al能将C从CO2置换出来,写出此置换反应的热化学方程式
(6)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:

1 mol NH4+(aq) 全部氧化成NO3-(aq)的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】光催化是新发展的一个催化技术,TiO2是目前研究成功的应用广泛的光催化剂,它是由金红石矿(主要成分为TiO2)先制备为TiCl4,再转化为纯TiO2。
请根据表中数据作答:
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行___________ ?
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向___________ 。
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向___________ 。
| 物种 | TiO2(s) | TiCl4(g) | Cl2(g) | O2(g) | C(s) | CO(g) |
| ΔrΗΘm /kJ∙molˉ1 | –944.7 | –763.2 | 0 | 0 | 0 | –110.5 |
| SΘm/J∙molˉ1∙Kˉ1 | 55.02 | 354.9 | 223.1 | 205.1 | 5.74 | 197.7 |
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义。请回答下列问题:
(1)SO2既是大气污染物,还能形成硫酸型酸雨,燃煤“固硫”可有效减少酸雨,请写出燃煤“固硫”的一种方法:_______ 。
(2)汽车尾气中NO生成过程的能量变化示意图如下所示:

该条件下,N2和O2完全反应生成NO的反应为_______ 反应(填“放热”或“吸热”)。
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①NiO电极上的电极反应式为_______ ;
②标准状况下,若Pt电极上消耗11.2 L氧气时,则转移的电子总数为_______ 。
(4)一种新型催化剂能使NO和CO发生反应:2NO+2CO 2CO2+N2。T℃时,将0.6 mol NO和0.8 mol CO充入2 L密闭容器中,模拟尾气转化,容器中CO物质的量随时间变化关系如图所示:
2CO2+N2。T℃时,将0.6 mol NO和0.8 mol CO充入2 L密闭容器中,模拟尾气转化,容器中CO物质的量随时间变化关系如图所示:

①图中A、B、C三点处于化学平衡状态的点是_______ ;
②反应0~10 min内,v(N2)=_______ mol·L-1·min-1;
③只改变下列某一反应条件时,能使上述转化速率加快的是_______ (填字母序号)。
a.降温 b.缩小容积
c.使用高效催化剂 d.减小CO2的物质的量
(1)SO2既是大气污染物,还能形成硫酸型酸雨,燃煤“固硫”可有效减少酸雨,请写出燃煤“固硫”的一种方法:
(2)汽车尾气中NO生成过程的能量变化示意图如下所示:

该条件下,N2和O2完全反应生成NO的反应为
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①NiO电极上的电极反应式为
②标准状况下,若Pt电极上消耗11.2 L氧气时,则转移的电子总数为
(4)一种新型催化剂能使NO和CO发生反应:2NO+2CO
 2CO2+N2。T℃时,将0.6 mol NO和0.8 mol CO充入2 L密闭容器中,模拟尾气转化,容器中CO物质的量随时间变化关系如图所示:
2CO2+N2。T℃时,将0.6 mol NO和0.8 mol CO充入2 L密闭容器中,模拟尾气转化,容器中CO物质的量随时间变化关系如图所示:
①图中A、B、C三点处于化学平衡状态的点是
②反应0~10 min内,v(N2)=
③只改变下列某一反应条件时,能使上述转化速率加快的是
a.降温 b.缩小容积
c.使用高效催化剂 d.减小CO2的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物的转化是资源利用和环境保护的重要研究课题。
(1)合成氨工业是最基本的无机化工之一,氨是化肥工业和基本有机化工的主要原料。合成氨反应中有关化学键键能数据如下表:
①已知:合成氨反应:N2(g)+3H2(g) 2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
 N2(g)+
N2(g)+ H2(g)的活化能Ea=
H2(g)的活化能Ea=_____ 。
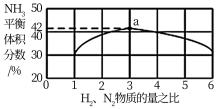
②图1表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据如图中a点数据计算N2的平衡体积分数:_____ (保留3位有效数字)。
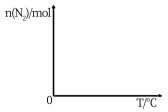
③依据温度对合成氨反应的影响,在如图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,N2物质的量变化的曲线示意图_____ 。
(2)选择性催化还原脱硝技术(SCR)是目前较成熟的烟气脱硝技术,该技术是指在温度300~420℃之间和催化剂条件下,用还原剂(如NH3)选择性地与NOx反应。
①SCR脱硝技术中发生的主要反应为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比
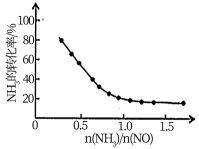
4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比 会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当
会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当 >1.0时,烟气中NO浓度反而增大,主要原因是
>1.0时,烟气中NO浓度反而增大,主要原因是_____ 。
②碱性溶液处理烟气中的氮氧化物也是一种脱硝的方法,写出NO2被Na2CO3溶液吸收生成三种盐的化学反应方程式_____ 。
(1)合成氨工业是最基本的无机化工之一,氨是化肥工业和基本有机化工的主要原料。合成氨反应中有关化学键键能数据如下表:
| 化学键 | H—H | N≡N | N—H |
| E/kJ•mol-1 | 436 | 946 | 391 |
①已知:合成氨反应:N2(g)+3H2(g)
 2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
2NH3(g)的活化能Ea=508kJ•mol-1,则氨分解反应:NH3(g)
 N2(g)+
N2(g)+ H2(g)的活化能Ea=
H2(g)的活化能Ea=②图1表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据如图中a点数据计算N2的平衡体积分数:

③依据温度对合成氨反应的影响,在如图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,N2物质的量变化的曲线示意图

(2)选择性催化还原脱硝技术(SCR)是目前较成熟的烟气脱硝技术,该技术是指在温度300~420℃之间和催化剂条件下,用还原剂(如NH3)选择性地与NOx反应。
①SCR脱硝技术中发生的主要反应为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比
4N2(g)+6H2O(g) △H=-1625.5kJ•mol-1;氨氮比 会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当
会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当 >1.0时,烟气中NO浓度反而增大,主要原因是
>1.0时,烟气中NO浓度反而增大,主要原因是
②碱性溶液处理烟气中的氮氧化物也是一种脱硝的方法,写出NO2被Na2CO3溶液吸收生成三种盐的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.请根据化学反应与热能的有关知识,填写下列空白:
(1)下列属于吸热反应的是___________ (填序号)。
①酸碱中和反应 ②燃烧木炭取暖 ③氢氧化钡晶体和氯化铵晶体反应
④煅烧石灰石制生石灰 ⑤铝热反应 ⑥碘升华
(2)已知H2、O2和H2O分子中的化学键H-H、O=O、O-H键能分别为Q1kJ/mol、Q2kJ/mol、Q3kJ/mol,由此可以推知下列关系正确的是___________ (填字母编号)。
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
II.已知2mol氢气燃烧生成液态水时放出572kJ热量。
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量______ (填“>”“<”或“=”)572kJ。
(4)写出表示氢气燃烧热的热化学方程式____________________________________ 。
(5)若将上述氢气燃烧反应设计成原电池,电解质溶液用KOH,请写出该电池负极的电极反应式:________________________ ,若电解质为熔融氧化物,产物在______ 极附近产生。
(1)下列属于吸热反应的是
①酸碱中和反应 ②燃烧木炭取暖 ③氢氧化钡晶体和氯化铵晶体反应
④煅烧石灰石制生石灰 ⑤铝热反应 ⑥碘升华
(2)已知H2、O2和H2O分子中的化学键H-H、O=O、O-H键能分别为Q1kJ/mol、Q2kJ/mol、Q3kJ/mol,由此可以推知下列关系正确的是
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
II.已知2mol氢气燃烧生成液态水时放出572kJ热量。
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量
(4)写出表示氢气燃烧热的热化学方程式
(5)若将上述氢气燃烧反应设计成原电池,电解质溶液用KOH,请写出该电池负极的电极反应式:
您最近一年使用:0次



