实验室需要0.5 mol·L-1硫酸溶液500mL。由计算知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积应选用_______mL量筒最好。
| A.10 mL | B.15 mL | C.20 mL | D.50 mL |
更新时间:2022-08-25 09:57:02
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】硫酸钾和硫酸铁的混合溶液,已知其中 的浓度为0.5 mol/L,硫酸根离子浓度为0.9 mol/L,则
的浓度为0.5 mol/L,硫酸根离子浓度为0.9 mol/L,则 的物质的量浓度为
的物质的量浓度为
 的浓度为0.5 mol/L,硫酸根离子浓度为0.9 mol/L,则
的浓度为0.5 mol/L,硫酸根离子浓度为0.9 mol/L,则 的物质的量浓度为
的物质的量浓度为| A.0.1 mol/L | B.0.15 mol/L | C.0.3 mol/L | D.0.2 mol/L |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】某仅含Na+、K+、SO 、Cl-的溶液中,存在关系c(Na+):c(K+):c(Cl-)=7:3:6,若c(Na+)=0.28mol·L-1,则c(SO
、Cl-的溶液中,存在关系c(Na+):c(K+):c(Cl-)=7:3:6,若c(Na+)=0.28mol·L-1,则c(SO )=
)=
 、Cl-的溶液中,存在关系c(Na+):c(K+):c(Cl-)=7:3:6,若c(Na+)=0.28mol·L-1,则c(SO
、Cl-的溶液中,存在关系c(Na+):c(K+):c(Cl-)=7:3:6,若c(Na+)=0.28mol·L-1,则c(SO )=
)=| A.0.02 mol·L-1 | B.0.16 mol·L-1 | C.0.04 mol·L-1 | D.0.08 mol·L-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺流程如下:
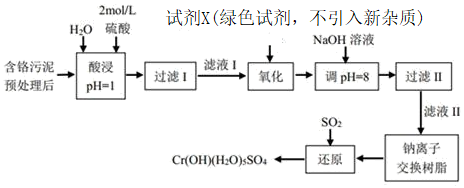
已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Ca2+和Mg2+;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
下列说法不正确的是

已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Ca2+和Mg2+;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Cr3+ |
| 沉淀完全时的pH | 3.7 | 11.1 | 9( >9溶解) |
| A.在实验室中用18.4 mol∙L−1的浓硫酸配制480 mL2 mol∙L−1的硫酸时,需量取浓硫酸52.2 mL |
B.试剂X的作用是将滤液I中的Cr3+转化为Cr2O |
| C.已知钠离子交换树脂的反应原理为Mn+ + nNaR=MRn+nNa+ ,上述流程中利用钠离子交换树脂可除去滤液II中的金属阳离子Ca2+和Mg2+ |
| D.上述流程中用SO2进行还原时,理论上所需的氧化剂与还原剂物质的量之比为2:3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关1molNaOH的说法中,正确的是
| A.NaOH的摩尔质量为40g |
| B.1mol NaOH 的质量为40g/mol |
| C.标准状况下,1molNaOH 所占的体积为22.4L |
| D.将1molNaOH溶于水配成100mL溶液,则溶液中溶质的物质的量浓度为10mol/L |
您最近一年使用:0次



