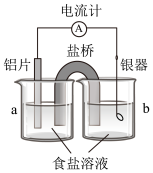
依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示。请回答下列问题:
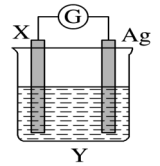
(1)电解质溶液Y是_______ 。
(2)银电极为电池的_______ 极,发生的电极反应式为_______ ;
(3)外电路中的电子_______ (填“流出”或“流入”)Ag电极。
(4)当有1.6g铜溶解时,银棒增重_______ g。

(1)电解质溶液Y是
(2)银电极为电池的
(3)外电路中的电子
(4)当有1.6g铜溶解时,银棒增重
更新时间:2022-09-24 13:40:04
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】I.物质中的化学能在一定条件下可转化为电能。
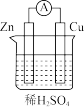
(1)将锌片放入盛有稀硫酸的烧杯中,反应的离子方程式是_________________ 。
(2)将锌片、铜片按照图所示装置连接,能证明化学能转化为电能的实验现象是:铜片上有气泡产生、_ 。
(3)稀硫酸在如图所示装置中的作用是:传导离子、__________________ 。
(4)下列反应通过原电池装置,可实现化学能直接转化为电能的是______ (填序号)。
① CaO+H2O = Ca(OH) 2
② 2H2+O2 = 2H2O
③ Cu+2Ag+ = Cu2++ 2Ag
Ⅱ.
(5)纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。其正极的电极反应式:______ ,工作时电池电解质溶液的碱性___ (填“增强”、“减弱”或“不变”)。
Ⅲ.固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。
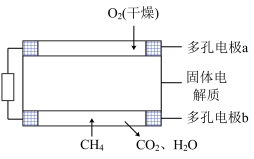
(6)a电极为电池的______ 极,固体电解质中的阳离子向_______ 极移动;
(7)b电极的电极反应式为:________________________ ;
(8)电池的总反应方程式为:___________________________ 。当电路中有2mol电子转移时,理论上负极消耗的气体在标况下的体积是_________ L。

(1)将锌片放入盛有稀硫酸的烧杯中,反应的离子方程式是
(2)将锌片、铜片按照图所示装置连接,能证明化学能转化为电能的实验现象是:铜片上有气泡产生、
(3)稀硫酸在如图所示装置中的作用是:传导离子、
(4)下列反应通过原电池装置,可实现化学能直接转化为电能的是
① CaO+H2O = Ca(OH) 2
② 2H2+O2 = 2H2O
③ Cu+2Ag+ = Cu2++ 2Ag
Ⅱ.
(5)纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。其正极的电极反应式:
Ⅲ.固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。

(6)a电极为电池的
(7)b电极的电极反应式为:
(8)电池的总反应方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS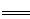 Na2Sx,正极的电极反应式为
Na2Sx,正极的电极反应式为__________ 。M(由Na2O和Al2O3制得)的两个作用是_______________ 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的__________ 倍。

 Na2Sx,正极的电极反应式为
Na2Sx,正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】锌铜原电池装置如图所示.回答下列问题:
(1)该装置能够将化学能转化为___________ 能。
(2)装置中使用的电解质有______________________ 。
(3)盐桥中的 移向
移向___________ 溶液(填“ ”或“
”或“ ”)。
”)。
(4)写出正极的电极反应式______________________ 。
(1)该装置能够将化学能转化为
(2)装置中使用的电解质有
(3)盐桥中的
 移向
移向 ”或“
”或“ ”)。
”)。(4)写出正极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】设计出燃料电池使汽油氧化直接产生电流是本世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,回答如下问题:
(1)以丁烷(C4H10)为汽油代表,这个电池放电时发生的化学反应___________ ;
(2)这个电池负极发生的反应是:C4H10 + 13O2—+ 26e-=4CO2+5H2O,正极发生的反应是:_______________________ ;固体电解质里O2-的移动方向是:____________ ;向外电路释放的电子的电极是:________________ ;
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:________ ;
(4)汽油燃料电池最大的障碍是氧化反应不完全产生_________ 堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年,这正是新一代化学家的历史使命。
(1)以丁烷(C4H10)为汽油代表,这个电池放电时发生的化学反应
(2)这个电池负极发生的反应是:C4H10 + 13O2—+ 26e-=4CO2+5H2O,正极发生的反应是:
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:
(4)汽油燃料电池最大的障碍是氧化反应不完全产生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

(1)以下叙述中,正确的是____ 。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的 均增大 D.乙中电子从铜片经导线流向锌片
均增大 D.乙中电子从铜片经导线流向锌片
E.乙溶液中 向锌片方向移动
向锌片方向移动
(2)变化过程中能量转化的形式主要是:甲为____ (填写选项字母)。
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有 电子发生转移,则生成的氢气在标况下的体积为
电子发生转移,则生成的氢气在标况下的体积为____ L。
(4)下列反应可以作为原电池工作时发生的反应的是:_______。
(5)乙中负极电极反应方程式为:________ 。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的
 均增大 D.乙中电子从铜片经导线流向锌片
均增大 D.乙中电子从铜片经导线流向锌片E.乙溶液中
 向锌片方向移动
向锌片方向移动(2)变化过程中能量转化的形式主要是:甲为
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有
 电子发生转移,则生成的氢气在标况下的体积为
电子发生转移,则生成的氢气在标况下的体积为(4)下列反应可以作为原电池工作时发生的反应的是:_______。
A.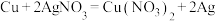 | B.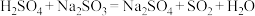 |
C. | D.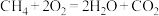 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】近来,科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子作溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更加安全。电池总反应式为:C2H5OH+3O2→2CO2+3H2O。
(1)电池正极的电极方程式为:____ 。
(2)1mol乙醇被氧化转移____ mol电子。
(3)铜、硝酸银溶液和银组成的原电池装置中,当导线中有0.02mol电子通过时,理论上银片的质量变化了____ g。
(1)电池正极的电极方程式为:
(2)1mol乙醇被氧化转移
(3)铜、硝酸银溶液和银组成的原电池装置中,当导线中有0.02mol电子通过时,理论上银片的质量变化了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,请回答下列问题:
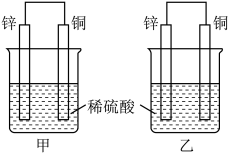
(1)下列说法正确的是________ 。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲____ 乙(填“>”、“<“或“=”)。
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为__________ 。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为______ 。
(5)利用下列反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电流方向,写出电极反应式。___

_______ 是正极,正极反应式:_____________ ;
________ 是负极,负极反应式:____________
(6)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂一碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中__ 作正极,负极的电极反应为_______ 。

(1)下列说法正确的是
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
(5)利用下列反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电流方向,写出电极反应式。

(6)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂一碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请根据化学反应与热能的有关知识,填写下列空白:
(1)下列反应中,属于吸热反应的是______ (填数字序号,下同),属于放热反应的是______ 。
①煅烧石灰石制生石灰②燃烧木炭取暖 ③炸药爆炸 ④酸碱中和反应⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1molH-H、1molO=O、1molO-H键需吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是______ (填字母编号)。
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
(3)用导线连接锌片、铜片后浸入稀硫酸溶液中,构成了原电池,工作一段时间后,锌片的质量减少了3.25g,此电池负极的电极反应式是______________ ,铜片表面析出了氢气____ L(标准状况)。
(1)下列反应中,属于吸热反应的是
①煅烧石灰石制生石灰②燃烧木炭取暖 ③炸药爆炸 ④酸碱中和反应⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1molH-H、1molO=O、1molO-H键需吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
(3)用导线连接锌片、铜片后浸入稀硫酸溶液中,构成了原电池,工作一段时间后,锌片的质量减少了3.25g,此电池负极的电极反应式是
您最近一年使用:0次