某课外小组分别用图中所示装置对原电池和电解原理进行实验探究。请回答:
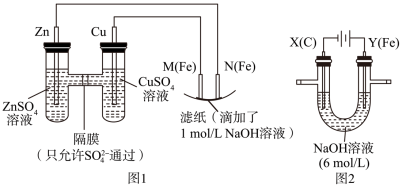
用图1装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是___________(填序号)。
(2)N极为___________ (填 “正” “负” “阴” “阳”)电极,发生反应的电极反应式为___________ 。
(3)实验过程中,SO
_____ (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有___________ 。
用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现:高铁酸根(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)电解过程中,Y极发生的电极反应为_____ 和___________ 。
(6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少___________ g。
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为___________ 。

用图1装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是___________(填序号)。
| A.铝 | B.石墨 |
| C.银 | D.铂 |
(3)实验过程中,SO

用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现:高铁酸根(FeO
 )在溶液中呈紫红色。
)在溶液中呈紫红色。(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
更新时间:2022-09-22 20:43:46
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】原电池
(1)原电池是一种将___________ 转化为________ 的装置。
(2)构成原电池的条件分别是_______ 、_________ 、________ 、_______ 。
(3)理论上所有的氧化还原反应都可以设计成原电池装置。
(4)在外电路中依靠____ 的定向移动导电,电解质溶液中靠_____ 的定向移动导电。
(5)原电池的正极材料若是金属单质,则金属单质被__________ ,无法失电子被腐蚀。
(6)原电池可以_______ 化学反应速率。
(1)原电池是一种将
(2)构成原电池的条件分别是
(3)理论上所有的氧化还原反应都可以设计成原电池装置。
(4)在外电路中依靠
(5)原电池的正极材料若是金属单质,则金属单质被
(6)原电池可以
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某校化学兴趣小组进行探究性活动:将氧化还原反应2Fe3++2I-=2Fe2++I2设计成带盐桥的原电池。提供的试剂:FeCl3溶液、KI溶液;其他用品任选。回答下列问题:
(1)画出设计的原电池装置图,并标出电极材料、电极名称及电解质溶液。
(2)发生氧化反应的电极反应式为_______ 。
(3)反应达到平衡时,外电路导线中_______ (填“有”或“无”)电流通过。
(4)平衡后向FeCl3溶液中加入少量FeCl2固体,当固体全部溶解后,此时该溶液中的电极为_______ (填“正”或“负”)极。
(1)画出设计的原电池装置图,并标出电极材料、电极名称及电解质溶液。
(3)反应达到平衡时,外电路导线中
(4)平衡后向FeCl3溶液中加入少量FeCl2固体,当固体全部溶解后,此时该溶液中的电极为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】电解原理常用于某些物质的制备。回答下列问题:
(1) 可以通过石墨为电板,
可以通过石墨为电板, 和
和 的混合溶液为电解液电解制取。阳极发生的电极反应式为
的混合溶液为电解液电解制取。阳极发生的电极反应式为_______ ,阴极上观察到的现象是_______ ;若电解液中不加入 ,阴极发生的电极反应式为
,阴极发生的电极反应式为_______ 。
(2) 可采用“电解法”制备,装置如图所示。
可采用“电解法”制备,装置如图所示。

①写出电解时阴极的电极反应式_______ 。
②电解过程中通过阳离子交换膜的离子主要为_______ ,其迁移方向是_______ 。
(1)
 可以通过石墨为电板,
可以通过石墨为电板, 和
和 的混合溶液为电解液电解制取。阳极发生的电极反应式为
的混合溶液为电解液电解制取。阳极发生的电极反应式为 ,阴极发生的电极反应式为
,阴极发生的电极反应式为(2)
 可采用“电解法”制备,装置如图所示。
可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在如图所示的三个烧杯中均盛有足量的氯化铜溶液。请按要求回答下列问题:

(1)A、B、C三个装置中属于电解池的是______ 。
(2)A池中Cu是______ 极,A池中Cl-移向___________ 极(填“Zn”或“Cu”),总反应的离子方程式为___________ 。
(3)B池中C电极上发生___________ 反应(填“氧化”或“还原”),B池中总反应的化学方程式为___________ 。
(4)C池中Cu是___________ 极,电极反应为___________ ,反应过程中c(Cu2+)___________ (填“变大”“变小”或“不变”)。

(1)A、B、C三个装置中属于电解池的是
(2)A池中Cu是
(3)B池中C电极上发生
(4)C池中Cu是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】从H+、Cu2+、Na+、SO42-、Cl-等五种离子中选择适当的离子组成电解质,使之符合下列要求。
(1)以碳棒为电极,电解时电解质质量减小,水量不变,应选用的电解质是________________________________ ;
(2)以碳棒为电极,电解时电解质质量不变,水量减少,应选用的电解质是________________________________ ;
(3)以碳棒为阳极,铁棒为阴极,电解时电解质质量和水量都减少,则应选用的电解质是_________________________________ 。
(1)以碳棒为电极,电解时电解质质量减小,水量不变,应选用的电解质是
(2)以碳棒为电极,电解时电解质质量不变,水量减少,应选用的电解质是
(3)以碳棒为阳极,铁棒为阴极,电解时电解质质量和水量都减少,则应选用的电解质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)甲池为_________ (填“原电池”、“电解池”或“电镀池”),A电极为_________ (填“正极”、“负极”、“阴极”或“阳极”),其电极反应式为__________ 。
(2)乙池中C极为_________ (填“正极”、“负极”、“阴极”或“阳极”),其电极反应式为__________ 。当池中D极质量增重21.6g时,甲池中B电极理论上消耗O2的体积为_________ L(标准状况)。
(3)丙池中F电极为_______ (填“正极”“负极”、“阴极”或“阳极”),该池的总反应的化学方程式为__________ 。
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,F极增重1.28 g,若不考虑溶液体积变化,则此时溶液的pH为_______ 。

请回答下列问题:
(1)甲池为
(2)乙池中C极为
(3)丙池中F电极为
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,F极增重1.28 g,若不考虑溶液体积变化,则此时溶液的pH为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】目前市场上的电池种类繁多,性能也各不相同。根据电化学原理回答问题:
(1)镍一镉电池是一种新型的封闭式体积小的可充电电池。其工作原理如图甲所示。放电时,镉电极反应式为___________ ,充电时,阳离子移向_________ 极(填“a”或“b”)。

(2)燃料电池具有能量转化率高、对环境友好等优点。燃料电池的介质有多种形式,如酸性溶液、碱性溶液、熔融氧化物和熔融碳酸盐等。甲烷碱性燃料电池(乙图)和熔融碳酸盐燃料电池(丙图)工作原理分别如图所示:

①在乙图中,a电极反应式为___________ 。
②在丙图中,d电极反应式为_________ 。
(3)以 -空气电池为电源,用情性电极作电极材料电解氯化钠溶液,如图丁所示,该电池工作时,
-空气电池为电源,用情性电极作电极材料电解氯化钠溶液,如图丁所示,该电池工作时, 装置中
装置中 电极反应式为
电极反应式为_________ ,b、c电极析出物质的物质的量比为________ (不考虑析出物质的溶解)。

(4)如图戊所示,用左池(总反应式为 ,未配平)电解硫酸铜溶液。左池每消耗
,未配平)电解硫酸铜溶液。左池每消耗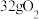 ,理论上在右池
,理论上在右池_______ (填“石墨”或“Ag”)极会析出_____ g 。
。

(1)镍一镉电池是一种新型的封闭式体积小的可充电电池。其工作原理如图甲所示。放电时,镉电极反应式为

(2)燃料电池具有能量转化率高、对环境友好等优点。燃料电池的介质有多种形式,如酸性溶液、碱性溶液、熔融氧化物和熔融碳酸盐等。甲烷碱性燃料电池(乙图)和熔融碳酸盐燃料电池(丙图)工作原理分别如图所示:

①在乙图中,a电极反应式为
②在丙图中,d电极反应式为
(3)以
 -空气电池为电源,用情性电极作电极材料电解氯化钠溶液,如图丁所示,该电池工作时,
-空气电池为电源,用情性电极作电极材料电解氯化钠溶液,如图丁所示,该电池工作时, 装置中
装置中 电极反应式为
电极反应式为
(4)如图戊所示,用左池(总反应式为
 ,未配平)电解硫酸铜溶液。左池每消耗
,未配平)电解硫酸铜溶液。左池每消耗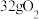 ,理论上在右池
,理论上在右池 。
。
您最近一年使用:0次




