填空:
(1)向煮沸的蒸馏水中逐滴加入饱和 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体,制备
胶体,制备 胶体的化学方程式为:
胶体的化学方程式为:_______ 。
(2)写出 溶于水的电离方程式:
溶于水的电离方程式:_______ 。
(3)将表面附有铁锈(成分是 )的铁钉放入稀硫酸中,开始反应的离子方程式是
)的铁钉放入稀硫酸中,开始反应的离子方程式是_______ ;反应片刻后,可观察到有气体产生,其离子方程式是_______ 。
(4)向 溶液逐滴加入
溶液逐滴加入 溶液至过量,反应的离子方程式依次为
溶液至过量,反应的离子方程式依次为____ ,____ 。
(1)向煮沸的蒸馏水中逐滴加入饱和
 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体,制备
胶体,制备 胶体的化学方程式为:
胶体的化学方程式为:(2)写出
 溶于水的电离方程式:
溶于水的电离方程式:(3)将表面附有铁锈(成分是
 )的铁钉放入稀硫酸中,开始反应的离子方程式是
)的铁钉放入稀硫酸中,开始反应的离子方程式是(4)向
 溶液逐滴加入
溶液逐滴加入 溶液至过量,反应的离子方程式依次为
溶液至过量,反应的离子方程式依次为
更新时间:2022-10-13 19:09:02
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有以下物质:a. 溶液,b.液氨,c.
溶液,b.液氨,c. 固体,d.
固体,d. 固体,e.Fe
固体,e.Fe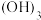 胶体,f.铜,g.
胶体,f.铜,g. ,h.
,h. ,i.熔融
,i.熔融 ,J.稀硫酸
,J.稀硫酸 .澄清石灰水 l.蔗糖
.澄清石灰水 l.蔗糖 .酒精
.酒精
(1)①以上物质中属于非电解质的是_______ (填字母,下同),属于电解质的有_______ ,能导电的有_______ 。
②写出 在水溶液中电离方程式:
在水溶液中电离方程式:_______ 。
③在足量 的水溶液中加入少量
的水溶液中加入少量 的水溶液,发生反应的离子方程式为
的水溶液,发生反应的离子方程式为_______ 。
④在含 的水溶液中缓缓通少量
的水溶液中缓缓通少量 ,该过程的离子反应方程式为
,该过程的离子反应方程式为_______ 。
(2)向煮沸的蒸馏水中逐滴加入饱和 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体。
胶体。
①制取 胶体的离子方程式为
胶体的离子方程式为_______ 。
②下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉
B.胶体的电泳
C.丁达尔效应
区分胶体和溶液的方法是_______ (填字母,下同);“卢水点豆腐”,利用的性质是_______ ;工厂采用高压静电除尘,利用的胶体性质是_______ 。
 溶液,b.液氨,c.
溶液,b.液氨,c. 固体,d.
固体,d. 固体,e.Fe
固体,e.Fe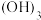 胶体,f.铜,g.
胶体,f.铜,g. ,h.
,h. ,i.熔融
,i.熔融 ,J.稀硫酸
,J.稀硫酸 .澄清石灰水 l.蔗糖
.澄清石灰水 l.蔗糖 .酒精
.酒精(1)①以上物质中属于非电解质的是
②写出
 在水溶液中电离方程式:
在水溶液中电离方程式:③在足量
 的水溶液中加入少量
的水溶液中加入少量 的水溶液,发生反应的离子方程式为
的水溶液,发生反应的离子方程式为④在含
 的水溶液中缓缓通少量
的水溶液中缓缓通少量 ,该过程的离子反应方程式为
,该过程的离子反应方程式为(2)向煮沸的蒸馏水中逐滴加入饱和
 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体。
胶体。①制取
 胶体的离子方程式为
胶体的离子方程式为②下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉
B.胶体的电泳
C.丁达尔效应
区分胶体和溶液的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】无机化合物可根据其组成和性质进行分类:
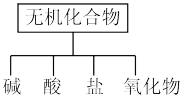
(1)上图所示的物质分类方法名称是_______ 。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥ 的后面(任意写一种)。
(3)写出⑨的水溶液与①的水溶液反应的离子反应方程式:_______ 。
(4)实验室由⑩制备O2的化学反应方程式 :_______ 。写出制备④的胶体的化学反应方程式:_______ ,再向胶体中逐滴滴加①的溶液至过量,有何现象_______ 。

(1)上图所示的物质分类方法名称是
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥ 的后面(任意写一种)。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ② | ③ ④Fe(OH)3 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O2 | ⑨NH3 ⑩H2O2 |
(4)实验室由⑩制备O2的化学反应方程式 :
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Fe2O3是一种重要的工业原料。
(1)取少量Fe2O3粉末(红棕色),加入适量盐酸,发生反应的离子方程式为________________ 。
用上述溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,反应的化学方程式为______________________ 。
(3)在小烧杯中加入20mL 蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸直至溶液呈________ 色,即可制得Fe(OH)3胶体。电泳实验时,____________ (填“阳”或“阴”)极颜色加深。
(4)已知强酸氢碘酸(HI)具有较强的还原性。取上述烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的HI稀溶液,边滴边振荡,会出现一系列变化。先出现红褐色沉淀,原因是__________________ 。随后沉淀溶解,溶液呈黄色,最后溶液颜色加深。若此时向该溶液中加淀粉溶液,溶液变蓝,请写出Fe(OH)3与HI反应的离子方程式_________________________ 。
(5)已知:氧化性:Cl2>Br2>Fe3+>I2则
向FeBr2溶液中通入等物质的量的 Cl2的总离子方程式为______________________ 。
向FeI2溶液中通入等物质的量的 Cl2的总离子方程式为_______________________ 。
(1)取少量Fe2O3粉末(红棕色),加入适量盐酸,发生反应的离子方程式为
用上述溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,反应的化学方程式为
(3)在小烧杯中加入20mL 蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸直至溶液呈
(4)已知强酸氢碘酸(HI)具有较强的还原性。取上述烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的HI稀溶液,边滴边振荡,会出现一系列变化。先出现红褐色沉淀,原因是
(5)已知:氧化性:Cl2>Br2>Fe3+>I2则
向FeBr2溶液中通入等物质的量的 Cl2的总离子方程式为
向FeI2溶液中通入等物质的量的 Cl2的总离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)现有①氯化氢②酒精③液氯④纯碱⑤熔融的氢氧化钠⑥水银⑦二氧化硫⑧一氧化碳⑨澄清石灰水等物质中,属于盐的是___________ (填序号,下同),属于酸性氧化物的是___________ ,能导电的是___________ ,属于电解质的是___________ 。
(2)有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的 ,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。
,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。
①写出甲、乙、丙、丁四种元素组成的化合物在水中的电离方程式_____ 。
②画出甲元素的离子结构示意图_____ 。
(1)现有①氯化氢②酒精③液氯④纯碱⑤熔融的氢氧化钠⑥水银⑦二氧化硫⑧一氧化碳⑨澄清石灰水等物质中,属于盐的是
(2)有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的
 ,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。
,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。①写出甲、乙、丙、丁四种元素组成的化合物在水中的电离方程式
②画出甲元素的离子结构示意图
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求回答问题:
(1)小苏打化学式:_______ ,漂粉精有效成分_______ 。
(2)①写出 在水中的电离方程式
在水中的电离方程式_______ 。
②向FeCl2溶液中滴加氢氧化钠溶液,写出白色沉淀转化为红褐色沉淀的化学方程式:_______ 。
(1)小苏打化学式:
(2)①写出
 在水中的电离方程式
在水中的电离方程式②向FeCl2溶液中滴加氢氧化钠溶液,写出白色沉淀转化为红褐色沉淀的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有下列十种物质:①盐酸;②小苏打;③二氧化碳;④固体烧碱;⑤蔗糖;⑥熔融氢氧化钾;⑦氢氧化铁胶体:⑧ ;⑨铜;⑩硫酸铁溶液;
;⑨铜;⑩硫酸铁溶液;
(1)上述十种物质中,属于电解质的有_____ (填序号,下同),属于非电解质的有_____ ,该状态下能导电的有_____ 。
(2)写出⑧在水溶液中的电离方程式为_____ 。
(3)写出②与④在溶液中反应的离子方程式为_____ 。
(4)写出④与⑧在水溶液中反应的离子方程式为_____ 。
 ;⑨铜;⑩硫酸铁溶液;
;⑨铜;⑩硫酸铁溶液;(1)上述十种物质中,属于电解质的有
(2)写出⑧在水溶液中的电离方程式为
(3)写出②与④在溶液中反应的离子方程式为
(4)写出④与⑧在水溶液中反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】阅读下列材料,回答相应问题。
材料一:
中国氯碱化工行业涌现出一批油化一体化、盐化一体化、煤盐化一体化、盐气化一体化的氯碱企业。
……
盐化一体化,如山东滨化集团等多家企业集团投资盐田和盐化工项目,将建成31300公顷盐田(原盐年产量300万吨)和烧碱年产量60万吨,溴盐年产量3万吨、氧化镁年产量12万吨、氯乙烯年产量20万吨等盐化项目。
……
近几年来,中国氯碱企业在烧碱产品供大于求的市场环境求生存、求发展,提高市场竞争力,纷纷向专业化、特色化发展。中石化江汉油田盐化厂大力开发钠法漂粉精,其生产规模位列世界第三;
……
主要能源煤的价格上涨,将会大大影响生产成本;物流量大,既需要大量燃料煤炭和原料盐(氯化钠)等的运入,又要有烧碱、液氧、盐酸等大量产品需要运出,运输价格的上涨必然提升氯碱产品的生产成本。
——节选自文章《中国烧碱行业发展趋势与对策建议》,部分文字有改动
(1)写出氯化镁的电离方程式:_________ ,从物质分类的角度来看,氯化镁属于_________ (填“酸”、“碱”或“盐”);
(2)写出利用氧化还原反应制备漂粉精的一个化学方程式:___________ ;
(3)为了降低运输成本,能否用铁罐运输盐酸?说明原因:___________ 。
材料二:
离子膜法制碱工艺中,在电解过程中无法透过离子膜进入烧碱系统,而在盐水系统中积累,当浓度超过一定值后,其在阳极放电,消耗电能的同时产生游离态的氧并对阳极产生严重破坏,因此必须去除。我国传统的氯化钡法脱除虽投资少、操作方便,但易产生大量盐泥。
——节选自文章《我国烧碱行业发展现状及能效水平浅析》
(4)写出用氯化钡法脱除盐水中 的离子方程式:
的离子方程式:___________ ;
(5)1807年,英国化学家戴维通过电解烧碱制得金属钠。依据氧化还原反应原理推测该电解反应中___________ (填元素名称)元素化合价升高。而今工业上主要通过电解氯化钠来制备金属钠,请举出一条用氯化钠代替烧碱作电解原料的优势:___________ 。
材料一:
中国氯碱化工行业涌现出一批油化一体化、盐化一体化、煤盐化一体化、盐气化一体化的氯碱企业。
……
盐化一体化,如山东滨化集团等多家企业集团投资盐田和盐化工项目,将建成31300公顷盐田(原盐年产量300万吨)和烧碱年产量60万吨,溴盐年产量3万吨、氧化镁年产量12万吨、氯乙烯年产量20万吨等盐化项目。
……
近几年来,中国氯碱企业在烧碱产品供大于求的市场环境求生存、求发展,提高市场竞争力,纷纷向专业化、特色化发展。中石化江汉油田盐化厂大力开发钠法漂粉精,其生产规模位列世界第三;
……
主要能源煤的价格上涨,将会大大影响生产成本;物流量大,既需要大量燃料煤炭和原料盐(氯化钠)等的运入,又要有烧碱、液氧、盐酸等大量产品需要运出,运输价格的上涨必然提升氯碱产品的生产成本。
——节选自文章《中国烧碱行业发展趋势与对策建议》,部分文字有改动
(1)写出氯化镁的电离方程式:
(2)写出利用氧化还原反应制备漂粉精的一个化学方程式:
(3)为了降低运输成本,能否用铁罐运输盐酸?说明原因:
材料二:
离子膜法制碱工艺中,在电解过程中无法透过离子膜进入烧碱系统,而在盐水系统中积累,当浓度超过一定值后,其在阳极放电,消耗电能的同时产生游离态的氧并对阳极产生严重破坏,因此必须去除。我国传统的氯化钡法脱除虽投资少、操作方便,但易产生大量盐泥。
——节选自文章《我国烧碱行业发展现状及能效水平浅析》
(4)写出用氯化钡法脱除盐水中
 的离子方程式:
的离子方程式:(5)1807年,英国化学家戴维通过电解烧碱制得金属钠。依据氧化还原反应原理推测该电解反应中
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Ca(HCO3)2溶液与KOH溶液反应
(1)KOH不足:_____________
(2)KOH过量:_____________
(1)KOH不足:
(2)KOH过量:
您最近一年使用:0次



