配制步骤
(1)配制100 mL 1.00 mol·L-1氯化钠溶液
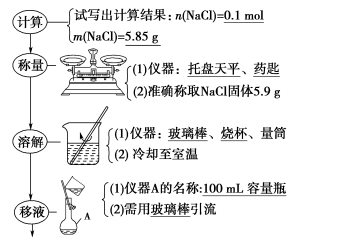
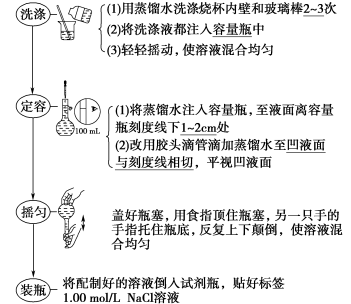
(2)用浓溶液稀释配制稀溶液
浓溶液稀释前后,溶液中溶质的物质的量不变,即得等式为:_______ 。
(3)注意事项:
①回答仪器应注明容量瓶规格,如500ml容量瓶。
②混合溶液不能直接体积相加和。
(1)配制100 mL 1.00 mol·L-1氯化钠溶液


(2)用浓溶液稀释配制稀溶液
浓溶液稀释前后,溶液中溶质的物质的量不变,即得等式为:
(3)注意事项:
①回答仪器应注明容量瓶规格,如500ml容量瓶。
②混合溶液不能直接体积相加和。
22-23高一上·全国·课时练习 查看更多[1]
(已下线)海水中的重要元素--钠和氯——整体认知
更新时间:2022-10-18 08:05:57
|
【知识点】 物质的量浓度计算-溶液稀释的有关计算解读
相似题推荐
填空题
|
容易
(0.94)
【推荐1】某浓硫酸的物质的量浓度为18.4mol/L,密度为1.84g/cm3。试计算:
(1)浓硫酸中溶质的质量分数______ 。
(2)配制100mL3.68mol/L的H2SO4溶液,需浓硫酸多少毫升______ ?
(1)浓硫酸中溶质的质量分数
(2)配制100mL3.68mol/L的H2SO4溶液,需浓硫酸多少毫升
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】回答下列问题:
(1)4g NaOH固体溶解后配制成100mL溶液,其物质的量浓度为___________ ,取出10mL该溶液,它的物质的量浓度为___________ , 将取出的 10mL加水稀释至100mL,其物质的量浓度变为 ___________ 。
(2)在19g某二价金属的氯化物(RCl2)中含Cl-离子0.4mol,则RCl2的摩尔质量为___________ ,R的相对原子质量为___________ 。
(1)4g NaOH固体溶解后配制成100mL溶液,其物质的量浓度为
(2)在19g某二价金属的氯化物(RCl2)中含Cl-离子0.4mol,则RCl2的摩尔质量为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】分类法在化学中起着非常重要的作用,现有下列物质:①Cl2、②NaOH溶液、③Cu、④冰水混合物、⑤ 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
(1)属于纯净物的有_______ ,属于氧化物的有_______ 。
(2)能导电的物质有_______ ,属于电解质的有_______ 。
(3)实验室中制取少量氢氧化铁胶体的离子方程式为_______ 。
(4)已知Cl2与NaOH反应的化学方程式是 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取_______ mL1mol/L的硫酸。
 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:(1)属于纯净物的有
(2)能导电的物质有
(3)实验室中制取少量氢氧化铁胶体的离子方程式为
(4)已知Cl2与NaOH反应的化学方程式是
 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取
您最近一年使用:0次



