分类法在化学中起着非常重要的作用,现有下列物质:①Cl2、②NaOH溶液、③Cu、④冰水混合物、⑤ 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
(1)属于纯净物的有_______ ,属于氧化物的有_______ 。
(2)能导电的物质有_______ ,属于电解质的有_______ 。
(3)实验室中制取少量氢氧化铁胶体的离子方程式为_______ 。
(4)已知Cl2与NaOH反应的化学方程式是 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取_______ mL1mol/L的硫酸。
 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:(1)属于纯净物的有
(2)能导电的物质有
(3)实验室中制取少量氢氧化铁胶体的离子方程式为
(4)已知Cl2与NaOH反应的化学方程式是
 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取
更新时间:2021-02-07 20:39:44
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加 德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol
(2)该气体在标准状况下的体积为____________ L。
(3)该气体溶于水后形成VL溶液,其溶质的物质的量浓度为____ mol·L-1。
(1)该气体的物质的量为
(2)该气体在标准状况下的体积为
(3)该气体溶于水后形成VL溶液,其溶质的物质的量浓度为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】判断下列说法的正误。
1.标准状况下22.4LHCl溶于1L水,盐酸的物质的量浓度为1mol·L-1。(_______)
2.32.2gNa2SO4·10H2O溶于67.8g水中,w(Na2SO4)=32.2%。(_______)
3.31gNa2O溶于水,配成1L溶液,c(Na2O)=0.5mol·L-1。(_______)
4.将10mL1mol·L-1的H2SO4溶液稀释成0.1mol·L-1的H2SO4溶液,可向该溶液中加入90mL水。(_______)
5.洗净的锥形瓶和容量瓶需要放进烘箱中烘干。(_______)
6.用 装置配制0.1mol·L-1的NaOH溶液。(_______)
装置配制0.1mol·L-1的NaOH溶液。(_______)
7.用 装置配制一定物质的量浓度的NaCl溶液。(_______)
装置配制一定物质的量浓度的NaCl溶液。(_______)
8.用 装置配制溶液。(_______)
装置配制溶液。(_______)
1.标准状况下22.4LHCl溶于1L水,盐酸的物质的量浓度为1mol·L-1。(_______)
2.32.2gNa2SO4·10H2O溶于67.8g水中,w(Na2SO4)=32.2%。(_______)
3.31gNa2O溶于水,配成1L溶液,c(Na2O)=0.5mol·L-1。(_______)
4.将10mL1mol·L-1的H2SO4溶液稀释成0.1mol·L-1的H2SO4溶液,可向该溶液中加入90mL水。(_______)
5.洗净的锥形瓶和容量瓶需要放进烘箱中烘干。(_______)
6.用
 装置配制0.1mol·L-1的NaOH溶液。(_______)
装置配制0.1mol·L-1的NaOH溶液。(_______)7.用
 装置配制一定物质的量浓度的NaCl溶液。(_______)
装置配制一定物质的量浓度的NaCl溶液。(_______)8.用
 装置配制溶液。(_______)
装置配制溶液。(_______)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】某浓硫酸的物质的量浓度为18.4mol/L,密度为1.84g/cm3。试计算:
(1)浓硫酸中溶质的质量分数______ 。
(2)配制100mL3.68mol/L的H2SO4溶液,需浓硫酸多少毫升______ ?
(1)浓硫酸中溶质的质量分数
(2)配制100mL3.68mol/L的H2SO4溶液,需浓硫酸多少毫升
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】配制步骤
(1)配制100 mL 1.00 mol·L-1氯化钠溶液
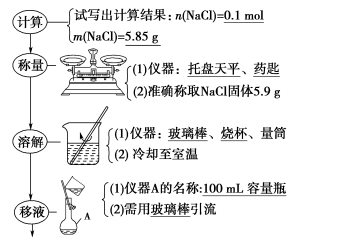
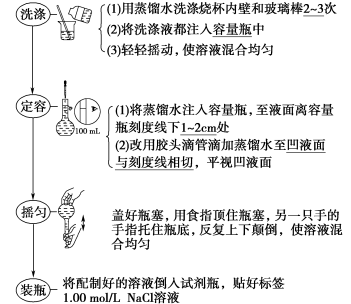
(2)用浓溶液稀释配制稀溶液
浓溶液稀释前后,溶液中溶质的物质的量不变,即得等式为:_______ 。
(3)注意事项:
①回答仪器应注明容量瓶规格,如500ml容量瓶。
②混合溶液不能直接体积相加和。
(1)配制100 mL 1.00 mol·L-1氯化钠溶液


(2)用浓溶液稀释配制稀溶液
浓溶液稀释前后,溶液中溶质的物质的量不变,即得等式为:
(3)注意事项:
①回答仪器应注明容量瓶规格,如500ml容量瓶。
②混合溶液不能直接体积相加和。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有_______ ,属于非电解质的有_______ 。(填序号)
(2)除去③中少量②的化学方程式为_______ 。
(3)现有100 mL⑩溶液中含Fe3+ 5.6g,则溶液中SO 的物质的量浓度是
的物质的量浓度是_______ 。
(4)若在⑦中缓慢加入①的水溶液,产生的现象是_______ 。
(1)上述十种物质中,属于电解质的有
(2)除去③中少量②的化学方程式为
(3)现有100 mL⑩溶液中含Fe3+ 5.6g,则溶液中SO
 的物质的量浓度是
的物质的量浓度是(4)若在⑦中缓慢加入①的水溶液,产生的现象是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】已知有下列物质:①盐酸 ②液态氨气 ③氢氧化钠固体 ④二氧化碳 ⑤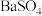 粉末⑥蔗糖晶体 ⑦
粉末⑥蔗糖晶体 ⑦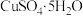 晶体 ⑧酒精 ⑨熔融氯化钠 ⑩石墨。请用序号回答:
晶体 ⑧酒精 ⑨熔融氯化钠 ⑩石墨。请用序号回答:
(1)属于电解质的_______ 。
(2)属于非电解质的_______ 。
(3)上述状态下可导电的是_______ 。
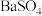 粉末⑥蔗糖晶体 ⑦
粉末⑥蔗糖晶体 ⑦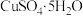 晶体 ⑧酒精 ⑨熔融氯化钠 ⑩石墨。请用序号回答:
晶体 ⑧酒精 ⑨熔融氯化钠 ⑩石墨。请用序号回答:(1)属于电解质的
(2)属于非电解质的
(3)上述状态下可导电的是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
(1)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。从物质的分类角度看,不恰当的一种物质是_____ (填化学式),它属于_____ 类。
(2)现有以下物质:① ②
② ③
③ 固体④
固体④ 胶体⑤乙醇⑥
胶体⑤乙醇⑥ ⑦稀硫酸。上述物质中能导电的是
⑦稀硫酸。上述物质中能导电的是_____ (填序号,下同),属于电解质的是_____ 。
(3)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
①如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是_____ 。(填字母)。

②有同学认为所有酸碱中和反应均可表示为 ,请举出一个例子反驳上述观点(用离子方程式表示)
,请举出一个例子反驳上述观点(用离子方程式表示)_____ 。
(1)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。从物质的分类角度看,不恰当的一种物质是
(2)现有以下物质:①
 ②
② ③
③ 固体④
固体④ 胶体⑤乙醇⑥
胶体⑤乙醇⑥ ⑦稀硫酸。上述物质中能导电的是
⑦稀硫酸。上述物质中能导电的是(3)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
①如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

②有同学认为所有酸碱中和反应均可表示为
 ,请举出一个例子反驳上述观点(用离子方程式表示)
,请举出一个例子反驳上述观点(用离子方程式表示)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】回答下列问题
(1)反应 中的
中的 是
是___________ 剂。
(2)反应 中的Na是
中的Na是___________ 剂。
(1)反应
 中的
中的 是
是(2)反应
 中的Na是
中的Na是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】某校化学兴趣小组根据反应:H2O2+2HI=2H2O+I2探究影响化学反应速率的因素。实验数据如下:
回答下列问题:
(1)反应:H2O2+2HI=2H2O+I2中,氧化剂是___ 。
(2)25℃时,表明增大反应物浓度,化学反应速率___ (填“增大”或“减小”)。
(3)能表明温度对化学反应速率影响的实验编号是①和___ 。
(4)H2O2不稳定,写出H2O2发生分解反应的化学方程式:___ 。
| 实验 编号 | H2O2溶液浓度/(mol·L-1) | HI溶液浓度/(mol·L-1) | 温度/℃ | 反应速率/(mol·L-1·s-1) |
| ① | 0.1 | 0.1 | 25 | 0.0076 |
| ② | 0.1 | 0.2 | 25 | 0.0153 |
| ③ | 0.1 | 0.3 | 25 | 0.0227 |
| ④ | 0.1 | 0.1 | 35 | 0.0304 |
回答下列问题:
(1)反应:H2O2+2HI=2H2O+I2中,氧化剂是
(2)25℃时,表明增大反应物浓度,化学反应速率
(3)能表明温度对化学反应速率影响的实验编号是①和
(4)H2O2不稳定,写出H2O2发生分解反应的化学方程式:
您最近一年使用:0次




