I.化学研究的对象是物质,下列物质:①HCl②NaOH③Cl2④H2O2⑤NH4Cl⑥P4⑦NH3•H2O⑧Na2O2⑨HClO⑩MgCl2。
(1)物质②、④的电子式分别为_______ ,⑨的结构式为_______ 。
(2)只存在离子键的是_______ (填序号,下同)。
(3)含有非极性键的共价化合物的是_______ ,既存在离子键又存在共价键的是_______ 。
II.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:
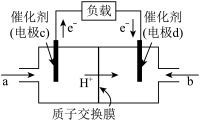
(4)电极d是_______ (填“正极”或“负极”),电极c的电极反应式_______ 。
(5)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为_______ L。
(1)物质②、④的电子式分别为
(2)只存在离子键的是
(3)含有非极性键的共价化合物的是
II.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:

(4)电极d是
(5)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
更新时间:2022-10-02 15:10:36
|
相似题推荐
【推荐1】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 X 为阳离子交换膜。

请按要求回答下列问题:
(1)甲烷燃料电池的负极反应式是_______ 。
(2)石墨(C)极的电极反应式是_______ 。
(3)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁极上生成的气体体积为_____ L;丙装置中阴极析出铜的质量为_______ g。

请按要求回答下列问题:
(1)甲烷燃料电池的负极反应式是
(2)石墨(C)极的电极反应式是
(3)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁极上生成的气体体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】其它燃料电池负极(燃料)电极反应式的书写
(1)烃燃料电池
①酸性介质
CH4:1CH4—8 e—+2H2O= 1CO2+8H+
C2H6:____________
C2H2:___________
②碱性介质
CH4:1CH4—8 e—+ 10OH—= 1 CO32—+ 7 H2O
C2H6:1 C2H6—14e— + 18OH—= 2CO32—+12H2O
C2H2:______________
(2)烃的含氧衍生物燃料电池
①酸性介质
CH3OH:1CH3OH—6e—+1H2O = 1CO2+6 H+
C2H5OH:______________
CH3OCH3:_____________
②碱性介质
CH3OH: 1CH3OH—6e—+8OH —= 1CO32—+ 6 H2O
C2H5OH:___________
CH3OCH3:___________
(3)熔融碳酸盐为电解质

负极(CH4):___________
正极(O2):______________
(1)烃燃料电池
①酸性介质
CH4:1CH4—8 e—+2H2O= 1CO2+8H+
C2H6:
C2H2:
②碱性介质
CH4:1CH4—8 e—+ 10OH—= 1 CO32—+ 7 H2O
C2H6:1 C2H6—14e— + 18OH—= 2CO32—+12H2O
C2H2:
(2)烃的含氧衍生物燃料电池
①酸性介质
CH3OH:1CH3OH—6e—+1H2O = 1CO2+6 H+
C2H5OH:
CH3OCH3:
②碱性介质
CH3OH: 1CH3OH—6e—+8OH —= 1CO32—+ 6 H2O
C2H5OH:
CH3OCH3:
(3)熔融碳酸盐为电解质

负极(CH4):
正极(O2):
您最近一年使用:0次
【推荐3】已知在25℃时,
①

②

③

④

(1)反应②自发进行的条件是_______ (填“低温”或“高温”)。
(2)根据上述数据,计算C-H的键能为_______ kJ/mol。
(3)乙烷—空气燃料电池是一种碱性燃料电池,电解质溶液是体积为1L、物质的量浓度为 的KOH溶液。该燃料电池放电时,负极发生
的KOH溶液。该燃料电池放电时,负极发生_______ (填“氧化”或“还原”)反应,其电极反应式是_______ ;当外电路中通过0.7mol电子时,25℃的电解质溶液pH为_______ (忽略 的水解及溶液体积的变化)。
的水解及溶液体积的变化)。
①


②


③


④


(1)反应②自发进行的条件是
(2)根据上述数据,计算C-H的键能为
(3)乙烷—空气燃料电池是一种碱性燃料电池,电解质溶液是体积为1L、物质的量浓度为
 的KOH溶液。该燃料电池放电时,负极发生
的KOH溶液。该燃料电池放电时,负极发生 的水解及溶液体积的变化)。
的水解及溶液体积的变化)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】目前人类发现和合成的物质已超过1亿种,对于这么多的物质和丰富的化学变化,分类法的作用几乎是无可代替的。请利用分类法结合所学知识完成下列各小题:
(1)现有下列6种微粒: 、
、 、
、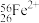 、
、 、
、 、
、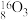 。形成上述6种微粒的核素有
。形成上述6种微粒的核素有_______ 种、元素有_______ 种。
(2)已知有下列物质:①Al②HCl气体③ ④KCl⑤熔融NaOH,其中能导电的是
④KCl⑤熔融NaOH,其中能导电的是_______ (填标号,下同);属于共价化合物的是_______ ;只含有离子键的是_______ 。
(3)用序号按要求回答问题:
下列物质:① ②
② ③
③ ④氩气⑤
④氩气⑤ ⑥NaOH⑦
⑥NaOH⑦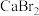 ⑧
⑧ ⑨
⑨ ⑩HBr。
⑩HBr。
只含非极性键的是_______ 含有极性键的离子化合物是_______ 。
(4)写出以下物质的电子式:
_______ 。
(1)现有下列6种微粒:
 、
、 、
、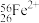 、
、 、
、 、
、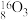 。形成上述6种微粒的核素有
。形成上述6种微粒的核素有(2)已知有下列物质:①Al②HCl气体③
 ④KCl⑤熔融NaOH,其中能导电的是
④KCl⑤熔融NaOH,其中能导电的是(3)用序号按要求回答问题:
下列物质:①
 ②
② ③
③ ④氩气⑤
④氩气⑤ ⑥NaOH⑦
⑥NaOH⑦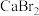 ⑧
⑧ ⑨
⑨ ⑩HBr。
⑩HBr。只含非极性键的是
(4)写出以下物质的电子式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)在①NH4Cl ②H2 ③CaCl2 ④O2 ⑤Na2O2 ⑥H2O2 ⑦D2 ⑧O3 ⑨12C ⑩14C(填序号,下同)只含有离子键的是______________ ,属于同素异形体的是____________ ,属于离子化合物的是_________________ 。
(2)联氨(又称肼 N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
①联氨分子的电子式为_____________ ,结构式为________________ 。
②实验室中可用次氯酸钠溶液与氨反应制备联氨(其中某一产物为 NaCl),反应的化学方程式为______________ 。
(2)联氨(又称肼 N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
①联氨分子的电子式为
②实验室中可用次氯酸钠溶液与氨反应制备联氨(其中某一产物为 NaCl),反应的化学方程式为
您最近一年使用:0次



