Ⅰ.德国化学家凯库勒认为:苯分子是由6个碳原子以单双键相互交替结合而成的环状结构。为了验证凯库勒有关苯环的观点,甲同学设计了如下实验方案。
①按如图所示装置连接好各仪器;②检验装置的气密性;③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹 、
、 、
、 ;④待烧瓶a中收集满气体后,将导管b的下端插入烧杯D的水中,挤压预先装有水的胶头滴管,观察实验现象。回答下列问题。
;④待烧瓶a中收集满气体后,将导管b的下端插入烧杯D的水中,挤压预先装有水的胶头滴管,观察实验现象。回答下列问题。

(1)A中所发生的有机反应的化学方程式为_______ 。
(2)装置B的作用是_______ 。
(3)反应完毕后,将装置A内的液体进行下列实验操作就可得到较纯净的溴苯:①蒸馏,②水洗,③用干燥剂干燥,④用10% 溶液洗,⑤水洗。正确的操作顺序是_______(填序号)。
溶液洗,⑤水洗。正确的操作顺序是_______(填序号)。
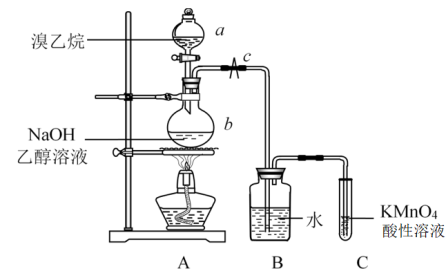
II.已知溴乙烷(C2H5Br)是无色液体,沸点38.4℃,密度比水大,难溶于水,可溶于多种有机溶剂。在溴乙烷与NaOH乙醇溶液的消去反应中可以观察到有气体生成。有人设计了如图所示的装置,用KMnO4酸性溶液是否褪色来检验生成的气体是否是乙烯。
请回答下列问题:
(4)仪器a的名称为_______ 。
(5)实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若_______ ,则证明装置A不漏气。
(6)仪器b中发生反应的化学方程式为_______ 。
(7)装置A中产生的气体通入装置C之前要先通过装置B,装置B的作用为_______ 。
(8)检验乙烯除用KMnO4酸性溶液外还可选用的试剂有_______ 。
①按如图所示装置连接好各仪器;②检验装置的气密性;③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹
 、
、 、
、 ;④待烧瓶a中收集满气体后,将导管b的下端插入烧杯D的水中,挤压预先装有水的胶头滴管,观察实验现象。回答下列问题。
;④待烧瓶a中收集满气体后,将导管b的下端插入烧杯D的水中,挤压预先装有水的胶头滴管,观察实验现象。回答下列问题。
(1)A中所发生的有机反应的化学方程式为
(2)装置B的作用是
(3)反应完毕后,将装置A内的液体进行下列实验操作就可得到较纯净的溴苯:①蒸馏,②水洗,③用干燥剂干燥,④用10%
 溶液洗,⑤水洗。正确的操作顺序是_______(填序号)。
溶液洗,⑤水洗。正确的操作顺序是_______(填序号)。| A.②③①④⑤ | B.②④⑤③① | C.④②③⑤① | D.②④①③⑤ |
II.已知溴乙烷(C2H5Br)是无色液体,沸点38.4℃,密度比水大,难溶于水,可溶于多种有机溶剂。在溴乙烷与NaOH乙醇溶液的消去反应中可以观察到有气体生成。有人设计了如图所示的装置,用KMnO4酸性溶液是否褪色来检验生成的气体是否是乙烯。

请回答下列问题:
(4)仪器a的名称为
(5)实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若
(6)仪器b中发生反应的化学方程式为
(7)装置A中产生的气体通入装置C之前要先通过装置B,装置B的作用为
(8)检验乙烯除用KMnO4酸性溶液外还可选用的试剂有
更新时间:2022-09-30 14:35:24
|
【知识点】 物质性质实验方案的设计解读
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是用浓硝酸、铜片、水等试剂探究浓、稀硝酸的强氧化性并观察还原产物的实验装置。
I.浓硝酸的强氧化性实验:将铜片置于具支试管的底部,在分液漏斗中加入约 5 mL 浓硝酸,往具支试管中放入约 2 mL 浓硝酸,用排水法收集产生的气体。

(1)具支试管中发生反应的化学方程式:_____ 。
(2)实验中观察到能证明浓硝酸具有强氧化性的现象_____ 。
II.稀硝酸的强氧化性实验
(3)上述反应完成后,欲进一步证明稀硝酸也具有强氧化性,紧接的简便、合理的实验操作是___ 。
(4)能证明稀硝酸与铜反应产生 NO 的实验现象是_____ (填写序号)。
A.c 中收集到无色气体
B.c 中收集到的无色气体接触空气后变为红棕色
C.b 中产生的无色气体接触空气后变为红棕色
III.实验反思
(5)利用该装置先进行铜与浓硝酸反应,再进行铜与稀硝酸反应的实验,其好处是_____ 。
IV.问题讨论:用等质量的铜片与等体积的浓硝酸、稀硝酸(硝酸均过量)反应时,发现反应后所得溶液前者呈绿色,后者呈蓝色。对此有两种看法:
①两者颜色不同的原因是因为 Cu2+浓度差异引起的。
②前者溶液呈绿色,是因为生成的红棕色 NO2 溶解于溶液中引起的。
(6)你认为上述看法_____ (填“①”或“②”)合理。
I.浓硝酸的强氧化性实验:将铜片置于具支试管的底部,在分液漏斗中加入约 5 mL 浓硝酸,往具支试管中放入约 2 mL 浓硝酸,用排水法收集产生的气体。

(1)具支试管中发生反应的化学方程式:
(2)实验中观察到能证明浓硝酸具有强氧化性的现象
II.稀硝酸的强氧化性实验
(3)上述反应完成后,欲进一步证明稀硝酸也具有强氧化性,紧接的简便、合理的实验操作是
(4)能证明稀硝酸与铜反应产生 NO 的实验现象是
A.c 中收集到无色气体
B.c 中收集到的无色气体接触空气后变为红棕色
C.b 中产生的无色气体接触空气后变为红棕色
III.实验反思
(5)利用该装置先进行铜与浓硝酸反应,再进行铜与稀硝酸反应的实验,其好处是
IV.问题讨论:用等质量的铜片与等体积的浓硝酸、稀硝酸(硝酸均过量)反应时,发现反应后所得溶液前者呈绿色,后者呈蓝色。对此有两种看法:
①两者颜色不同的原因是因为 Cu2+浓度差异引起的。
②前者溶液呈绿色,是因为生成的红棕色 NO2 溶解于溶液中引起的。
(6)你认为上述看法
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某小组同学采用以下装置验证SO2的性质:

(夹持及加热装置略,试管1:紫色石蕊溶液,试管2:H2S溶液,试管3:品红溶液,试管4:酸性KMnO4溶液,试管5:BaCl2溶液)。
(1)写出圆底烧瓶中发生反应的化学方程式_______ 。
(2)经过实验,观察到如下实验现象(填写字母):
①试管1中现象_______ 。
②试管2中现象_______ ,写出反应的化学方程式:_______ 。
③试管3中现象_______ ,说明SO2具有漂白性,证明该漂白的可逆性的实验操作是_______ 。
A.溶液变为红色 B.溶液变为白色 C.溶液变为无色 D.溶液先变为红色后变为无色 E.出现淡黄色沉淀 F.出现红褐色沉淀
(3)试管4中现象说明SO2还具有的性质是_______ ,反应离子方程式_______ 。
(4)实验的尾气SO2可以用NaOH溶液吸收,反应的化学方程式是_______ 。

(夹持及加热装置略,试管1:紫色石蕊溶液,试管2:H2S溶液,试管3:品红溶液,试管4:酸性KMnO4溶液,试管5:BaCl2溶液)。
(1)写出圆底烧瓶中发生反应的化学方程式
(2)经过实验,观察到如下实验现象(填写字母):
①试管1中现象
②试管2中现象
③试管3中现象
A.溶液变为红色 B.溶液变为白色 C.溶液变为无色 D.溶液先变为红色后变为无色 E.出现淡黄色沉淀 F.出现红褐色沉淀
(3)试管4中现象说明SO2还具有的性质是
(4)实验的尾气SO2可以用NaOH溶液吸收,反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】如图所示,a中放置附着氧化铜粉末的石棉绒,向a中持续通入气态物质X,可以观察到石棉绒上黑色粉末变成红色固态物质,同时c处的U形管中有无色液体生成(假设X气体全部反应,各处反应均完全)。

(1)X是________
A.H2 B.CO C.H2和CO D.CH3CH2OH蒸气
(2)写出 a 处反应的化学方程式:_______ 。
(3)c处液体主要成分的结构简式为______ ; 检验该物质的操作步骤是_______ ,其现象为______ 。

(1)X是
A.H2 B.CO C.H2和CO D.CH3CH2OH蒸气
(2)写出 a 处反应的化学方程式:
(3)c处液体主要成分的结构简式为
您最近一年使用:0次



