亚硝酸钠(NaNO2)常用作肉类食品的防腐剂。某实验小组将NO和NO2的混合气体通入Na2CO3溶液中,并经一系列操作制得NaNO2固体,然后对其性质进行探究。
【查阅资料】
①NaNO2具有较强的氧化性和较弱的还原性,其水溶液显碱性。
② 与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
【性质探究】将制取的NaNO2固体配制成约0.1mol/L NaNO2溶液,进行实验I和实验II。
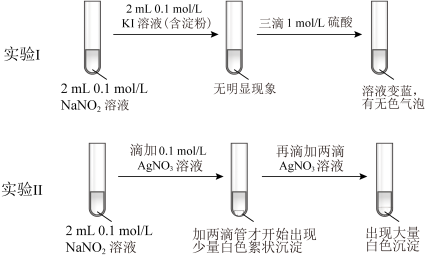
请回答下列问题:
(1)NaNO2溶液显碱性的原因是_______ (用离子方程式表示)。
(2)根据实验I,推测酸性条件下 氧化I- 的离子方程式是
氧化I- 的离子方程式是_______ 。
(3)甲同学认为依据实验I的现象可以得出结论:该条件下 能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有
能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有 。请补充完整实验III的实验方案:取2mL 0.1mol/L
。请补充完整实验III的实验方案:取2mL 0.1mol/L_______ 溶液于试管中,加入_______ ,溶液没有变蓝。
(4)①由实验II的现象得出结论:白色沉淀的生成与_______ 有关。
②仅用实验II的试剂,设计实验方案进一步证实了上述结论,实验操作及现象是_______ 。
(5)常温下AgNO2微溶于水,在沸水中可溶。除去AgNO2沉淀中的少量Ag2O杂质的方法如下:加入适量水,加热溶解,_______ ,过滤,洗涤,干燥。
【查阅资料】
①NaNO2具有较强的氧化性和较弱的还原性,其水溶液显碱性。
②
 与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
与Ag+反应,可生成AgNO2白色沉淀或无色配离子。【性质探究】将制取的NaNO2固体配制成约0.1mol/L NaNO2溶液,进行实验I和实验II。

请回答下列问题:
(1)NaNO2溶液显碱性的原因是
(2)根据实验I,推测酸性条件下
 氧化I- 的离子方程式是
氧化I- 的离子方程式是(3)甲同学认为依据实验I的现象可以得出结论:该条件下
 能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有
能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有 。请补充完整实验III的实验方案:取2mL 0.1mol/L
。请补充完整实验III的实验方案:取2mL 0.1mol/L(4)①由实验II的现象得出结论:白色沉淀的生成与
②仅用实验II的试剂,设计实验方案进一步证实了上述结论,实验操作及现象是
(5)常温下AgNO2微溶于水,在沸水中可溶。除去AgNO2沉淀中的少量Ag2O杂质的方法如下:加入适量水,加热溶解,
更新时间:2022-10-21 19:57:23
|
【知识点】 化学实验探究
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题。文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响。

(1)实验前:①先用0.1 mol·L-1H2SO4洗涤Fe粉,其目的是_________ ,然后用蒸馏水洗涤至中性;②将KNO3溶液的pH调至2.5;③为防止空气中的O2对脱氮的影响,应向KNO3溶液中通入________ (写化学式)。
(2)如图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应的离子方程式_____________ 。t1时刻后,若反应仍在进行,溶液中 的浓度在增大,Fe2+的浓度却没有增大,可能的原因是
的浓度在增大,Fe2+的浓度却没有增大,可能的原因是__________ 。
(3)该课题组对影响脱氮速率的因素提出了如下假设,请你完成假设二和假设三
假设一:溶液的pH;假设二:__________________ ;假设三:__________________ ;
(4)请你设计实验验证上述假设一,写出实验步骤及结论。(已知:溶液中的 浓度可用离子色谱仪测定)
浓度可用离子色谱仪测定)__________________ 。

(1)实验前:①先用0.1 mol·L-1H2SO4洗涤Fe粉,其目的是
(2)如图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应的离子方程式
 的浓度在增大,Fe2+的浓度却没有增大,可能的原因是
的浓度在增大,Fe2+的浓度却没有增大,可能的原因是(3)该课题组对影响脱氮速率的因素提出了如下假设,请你完成假设二和假设三
假设一:溶液的pH;假设二:
(4)请你设计实验验证上述假设一,写出实验步骤及结论。(已知:溶液中的
 浓度可用离子色谱仪测定)
浓度可用离子色谱仪测定)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】化学实验是研究物质性质的主要手段,某化学兴趣小组做以下实验
I.为研究X单质的性质,特设计如图所示装置进行实验。装置III中夹持装置已略去。其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)写出装置I中发生反应的离子方程式___________ 。
(2)写出IV中发生反应的离子方程式___________ 。
II.证明过氧化钠可在呼吸面具和潜水艇中做供氧剂(C中盛放的是过氧化钠)。

(3)写出过氧化钠与二氧化碳反应的化学方程式___________
(4)D中盛放的试剂是___________
III.验证铝及化合物性质
(5)铝与碱反应的离子方程式:___________ 。
(6)偏铝酸钠中通入过量的二氧化碳方程式:___________ 。
I.为研究X单质的性质,特设计如图所示装置进行实验。装置III中夹持装置已略去。其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)写出装置I中发生反应的离子方程式
(2)写出IV中发生反应的离子方程式
II.证明过氧化钠可在呼吸面具和潜水艇中做供氧剂(C中盛放的是过氧化钠)。

(3)写出过氧化钠与二氧化碳反应的化学方程式
(4)D中盛放的试剂是
III.验证铝及化合物性质
(5)铝与碱反应的离子方程式:
(6)偏铝酸钠中通入过量的二氧化碳方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硝酸是强酸之一,且是一种重要的化工原料,同时硝酸的形成也是氮循环的一环。某实验小组用如下实验装置模拟工业上制取硝酸:
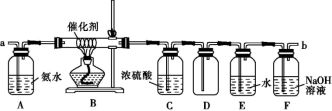
(1)提供氧气,要使装置B中充满反应物的操作是___________ 。
(2)写出装置B中发生反应的化学方程式:___________ 。
(3)装置C的作用是___________ 。
(4)装置F中发生的主要反应:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。实验后装置F中NaNO2和NaNO3物质的量浓度较大的是___________ 。
(5)现有硝酸和Cu粉,请设计制备Cu(NO3)2溶液的最佳方案:___________ 。

(1)提供氧气,要使装置B中充满反应物的操作是
(2)写出装置B中发生反应的化学方程式:
(3)装置C的作用是
(4)装置F中发生的主要反应:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。实验后装置F中NaNO2和NaNO3物质的量浓度较大的是
(5)现有硝酸和Cu粉,请设计制备Cu(NO3)2溶液的最佳方案:
您最近一年使用:0次



