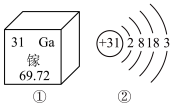
2019年是元素周期表年,镓是门捷列夫曾经预言的金属(类铝)。下图①是镓元素在元素周期表中的部分信息,②是镓原子的结构示意图。请回答:
A.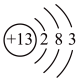 B.
B. 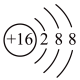 C.
C.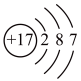 D.
D.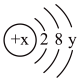
(1)镓原子的核电荷数为_______ ,镓元素的相对原子质量为_______ 。自然界中的镓共有两种稳定的同位素,其中69Ga的丰度为64.0%,则另一种镓的同位素质量数为_______ 。
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是_______ (填元素符号);微粒B的电子式为_______ ,则镓离子与B形成的化合物为_______ (填化学式)。
(3)D为某微粒的结构示意图,已知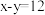 ,则x=
,则x=_______ ;写出C和D组成的化合物在水溶液中的电离方程式:_______ 。
(4)氮化镓(GaN)是第三代半导体材料,一般采用 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为_______ 。

A.
 B.
B.  C.
C. D.
D.
(1)镓原子的核电荷数为
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是
(3)D为某微粒的结构示意图,已知
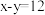 ,则x=
,则x=(4)氮化镓(GaN)是第三代半导体材料,一般采用
 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
更新时间:2022-11-07 23:32:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有关 Cl-微粒,回答下列问题:
Cl-微粒,回答下列问题:
(1)所含质子数_______ ;中子数_______ ;电子数_______ ;质量数_______ 。
(2)该微粒的结构示意图_______ 。
(3)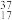 Cl、
Cl、 Cl之间的关系是
Cl之间的关系是_______ 。
 Cl-微粒,回答下列问题:
Cl-微粒,回答下列问题:(1)所含质子数
(2)该微粒的结构示意图
(3)
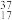 Cl、
Cl、 Cl之间的关系是
Cl之间的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列问题:
(1)某元素原子M层电子数是K、L层电子数之和的一半,该原子的结构示意图是___________ 。
(2)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(3)某分子中有5个原子核,共有10个电子,这种分子的结构式是___________ 。
(4)CaC2是离子化合物,含有Ca2+和C 两种离子,其中C
两种离子,其中C 的电子式
的电子式___________ 。
(1)某元素原子M层电子数是K、L层电子数之和的一半,该原子的结构示意图是
(2)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(3)某分子中有5个原子核,共有10个电子,这种分子的结构式是
(4)CaC2是离子化合物,含有Ca2+和C
 两种离子,其中C
两种离子,其中C 的电子式
的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表列出了9种元素在元素周期表中的位置示意图。
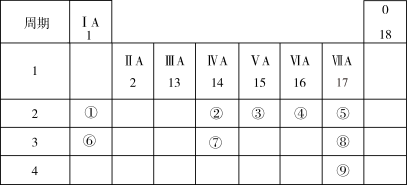
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______________ 。
(2)画出元素⑧形成的简单离子的结构示意图_______________ 。
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______________ 。
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______________ 。
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是______________ (填化学式),写出元素⑤的单质与水反应的化学方程式_______________ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______________ 。

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】155年前门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。如图为现代元素周期表的一部分,请回答下列问题:(以下问题均用相应的化学用语表达 )

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是___________ 。
(2)由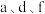 三种元素形成的化合物含有的化学键有
三种元素形成的化合物含有的化学键有___________ (填写化学键类型),属于___________ 化合物。
(3)元素b、c形成的简单气态氢化物中较稳定的是___________ (写具体的化学式,下同);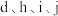 的简单离子半径由大到小的顺序排列为
的简单离子半径由大到小的顺序排列为___________ 。
(4)用电子式表示元素g与e的化合物形成的过程___________ 。
(5)在含有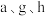 简单阳离子的
简单阳离子的 溶液中,逐滴滴加
溶液中,逐滴滴加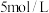 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算
溶液的体积关系如图所示。由图中数据分析计算
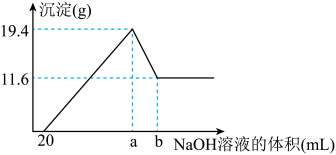
①沉淀减少时发生的离子方程式:___________ 。
②a点的数值为:___________ mL。

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是
(2)由
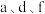 三种元素形成的化合物含有的化学键有
三种元素形成的化合物含有的化学键有(3)元素b、c形成的简单气态氢化物中较稳定的是
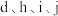 的简单离子半径由大到小的顺序排列为
的简单离子半径由大到小的顺序排列为(4)用电子式表示元素g与e的化合物形成的过程
(5)在含有
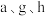 简单阳离子的
简单阳离子的 溶液中,逐滴滴加
溶液中,逐滴滴加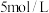 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算
溶液的体积关系如图所示。由图中数据分析计算
①沉淀减少时发生的离子方程式:
②a点的数值为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列为元素周期表中的一部分:

已知:⑤的氢化物常温下为气体,该气体可使湿润的红色石蕊试纸变蓝。
用化学式或元素符号回答下列问题:
(1) ④在周期表中的位置_______ 。
(2) ①②③中,最高价氧化物对应的水化物碱性最强的物质的电子式为_________ 。
(3) ①②⑥的简单离子半径由大到小的顺序是___________ 。(填离子符号)
(4) 用一个化学方程式证明Cl元素与⑦非金属性的强弱:____________ 。
(5) ①和⑥形成的一种化合物A中含有一种10电子微粒和一种18电子微粒,则A中含有的化学键类型为______ 。
(6) ⑥、⑦分别形成的氢化物沸点高的是_______ (填化学式)。原因是_______ 。
(7) ①、③分别形成的最高价氧化物对应的水化物相互反应的离子方程式为_________ 。

已知:⑤的氢化物常温下为气体,该气体可使湿润的红色石蕊试纸变蓝。
用化学式或元素符号回答下列问题:
(1) ④在周期表中的位置
(2) ①②③中,最高价氧化物对应的水化物碱性最强的物质的电子式为
(3) ①②⑥的简单离子半径由大到小的顺序是
(4) 用一个化学方程式证明Cl元素与⑦非金属性的强弱:
(5) ①和⑥形成的一种化合物A中含有一种10电子微粒和一种18电子微粒,则A中含有的化学键类型为
(6) ⑥、⑦分别形成的氢化物沸点高的是
(7) ①、③分别形成的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(1)在最高价氧化物的水化物中,酸性最强的化合物的名称 是______ ,碱性最强的化合物的化学式 是_______ 。
(2)⑤⑦形成化合物的电子式___ 。②形成的最高价氧化物的结构式____ 。
(3)最高价氧化物是两性氧化物的元素 其元素符号是____ ;写出它的氢氧化物与 ⑧的最高价氧化物的水化物反应的离子方程式
⑧的最高价氧化物的水化物反应的离子方程式________ 。
(4)⑥的单质与⑤的最高价氧化物的水化物反应的离子方程式是______ 。
(5)②和⑦可形成原子数1∶2的液态化合物甲,并能溶解⑦的单质,用电子式表示甲的形成过程:____________ 。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | ① | ② | ③ | ④ | |||
3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在最高价氧化物的水化物中,酸性最强的化合物的
(2)⑤⑦形成化合物的电子式
(3)最高价氧化物是两性氧化物的
 ⑧的最高价氧化物的水化物反应的离子方程式
⑧的最高价氧化物的水化物反应的离子方程式(4)⑥的单质与⑤的最高价氧化物的水化物反应的离子方程式是
(5)②和⑦可形成原子数1∶2的液态化合物甲,并能溶解⑦的单质,用电子式表示甲的形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】制冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到制冷目的。人们曾采用过乙醚、NH3、CH3Cl等作制冷剂,但它们不是有毒,就是易燃、于是科学家根据元素性质的递变规律来开发新的制冷剂。
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期______ >______ >H2O、HF。
(2)化合物的毒性: PH3>NH3 ; H2S______ H2O; CCl4_____ CF4 (选填>或<)。于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,新制冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的制冷剂氟里昂CF2Cl2终于诞生了。求助于周期表中元素及其化合物的________ 变化趋势来开发制冷剂的科学思维方法是值得借鉴的。(填写字母,多选扣分)①毒性 ②沸点 ③易燃性 ④水溶性 ⑤颜色
A、①③⑤ B、①②③ C、 ②③④ D、③④⑤
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期
(2)化合物的毒性: PH3>NH3 ; H2S
(3)已知CCl4的沸点为76.8℃,CF4的沸点为-128℃,新制冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的制冷剂氟里昂CF2Cl2终于诞生了。求助于周期表中元素及其化合物的
A、①③⑤ B、①②③ C、 ②③④ D、③④⑤
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填写下列空白:
(1)写出表示含有6个质子、8个中子的原子的化学符号:____
(2)周期表中所含元素种数最多的纵行是第____ 纵行。
(3)周期表中原子序数为87的元素的位置____ 。
(4)由 ,D,T和
,D,T和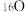 ,
,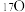 ,
,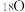 共可以组成
共可以组成____ 种水分子。
(5)氰(CN2)的化学性质和卤素( ,如
,如 )很相似,化学上称为拟卤素,试写出(CN2)与水反应的化学方程式:
)很相似,化学上称为拟卤素,试写出(CN2)与水反应的化学方程式:__ 。
(1)写出表示含有6个质子、8个中子的原子的化学符号:
(2)周期表中所含元素种数最多的纵行是第
(3)周期表中原子序数为87的元素的位置
(4)由
 ,D,T和
,D,T和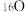 ,
,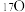 ,
,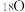 共可以组成
共可以组成(5)氰(CN2)的化学性质和卤素(
 ,如
,如 )很相似,化学上称为拟卤素,试写出(CN2)与水反应的化学方程式:
)很相似,化学上称为拟卤素,试写出(CN2)与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)原子序数大于4的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,则:
①A和B周期数之差为________
②A和B的质子数之差为___________ (用m、n表示)
③B和A的族序数之差为_______________ (用含m、n的代数式表示)
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。
如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为______________ ;
当B在A的下一周期时,B的原子序数为______________ ;
如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为______________ ;
当B在A的下一周期时,B的原子序数为______________ 。
①A和B周期数之差为
②A和B的质子数之差为
③B和A的族序数之差为
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。
如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为
当B在A的下一周期时,B的原子序数为
如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
当B在A的下一周期时,B的原子序数为
您最近一年使用:0次



