胶体金( )免疫层析法可用于快速检测新型冠状病毒抗体。利用柠檬酸钠溶液还原氯金酸(
)免疫层析法可用于快速检测新型冠状病毒抗体。利用柠檬酸钠溶液还原氯金酸(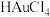 )即可制备得到胶体金。研究发现:柠檬酸钠的用量不同会导致胶体金粒径和颜色的不同。
)即可制备得到胶体金。研究发现:柠檬酸钠的用量不同会导致胶体金粒径和颜色的不同。
(1) 经过反应后可制备得到的胶体金胶粒的个数
经过反应后可制备得到的胶体金胶粒的个数_______ (填写“大于”或“小于”或“等于”) 个,原因是
个,原因是_______ 。
(2)德国化学家席格蒙迪研制出超显微镜,可以观察到胶体金颗粒的形态,胶体金分散质粒子的直径大致范围在_______  之间。
之间。
(3)胶体金免疫层析法的原理是胶体金的胶粒与蛋白质分子的正电荷基团紧密结合,若将胶体金装入U型管中,插入电极后通直流电,发现_______ 极附近颜色加深,产生这一现象的原因是_______ 。
 )免疫层析法可用于快速检测新型冠状病毒抗体。利用柠檬酸钠溶液还原氯金酸(
)免疫层析法可用于快速检测新型冠状病毒抗体。利用柠檬酸钠溶液还原氯金酸(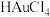 )即可制备得到胶体金。研究发现:柠檬酸钠的用量不同会导致胶体金粒径和颜色的不同。
)即可制备得到胶体金。研究发现:柠檬酸钠的用量不同会导致胶体金粒径和颜色的不同。(1)
 经过反应后可制备得到的胶体金胶粒的个数
经过反应后可制备得到的胶体金胶粒的个数 个,原因是
个,原因是(2)德国化学家席格蒙迪研制出超显微镜,可以观察到胶体金颗粒的形态,胶体金分散质粒子的直径大致范围在
 之间。
之间。(3)胶体金免疫层析法的原理是胶体金的胶粒与蛋白质分子的正电荷基团紧密结合,若将胶体金装入U型管中,插入电极后通直流电,发现
22-23高一上·上海杨浦·期中 查看更多[3]
(已下线)专题01 物质的分类-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(上海专用)上海市华东政法大学附属松江高级中学2022-2023学年高一下学期开学考化学试题上海市复旦大学附属中学2022-2023学年高一上学期期中考试化学试题
更新时间:2022-11-12 14:00:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】将少量饱和FeCl3溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:

甲:饱和FeCl3溶液滴加到冷水中
乙:饱和FeCl3溶液滴加到NaOH溶液中
丙:饱和FeCl3溶液滴加到沸水中
(1)三种分散系的名称分别是:溶液、__ 和胶体。用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论__ 。
(2)向丙中加入电极通电后,Fe(OH)3胶体粒子向电源__ 极的方向移动(填“阴”或“阳”)。
(3)可用如图1所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若___ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。

甲:饱和FeCl3溶液滴加到冷水中
乙:饱和FeCl3溶液滴加到NaOH溶液中
丙:饱和FeCl3溶液滴加到沸水中
(1)三种分散系的名称分别是:溶液、
(2)向丙中加入电极通电后,Fe(OH)3胶体粒子向电源
(3)可用如图1所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知HNO2是一种弱酸,向NaNO2中加入强酸可生成HNO2。HNO2不稳定,易分解成NO和NO2气体。HNO2是一种还原剂,能被常见的强氧化剂氧化;但在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的白色沉淀。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐如NaNO2,则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出___ (填“氧化”或“还原”)性。
(2)下列方法中,不能用来区分NaNO2和NaCl的是___ (填序号)。
A.加入盐酸,观察是否有气泡产生
B.加入AgNO3溶液观察是否有沉淀生成
C.分别在它们的酸性溶液中加入FeCl2溶液,观察溶液颜色变化
(3)在酸性条件下,HNO2与KI反应,I-被氧化为I2,HNO2被还原为NO气体,写出该反应的离子方程式:__ 。
(4)S2O 可以与H2O2、Fe2+反应制备Fe2O3纳米颗粒。
可以与H2O2、Fe2+反应制备Fe2O3纳米颗粒。
①S2O 中S的化合价为
中S的化合价为__ 。
②该反应的离子方程式为:2Fe2++S2O +4H2O2+4OH-=Fe2O3+S2O
+4H2O2+4OH-=Fe2O3+S2O +6H2O
+6H2O
下列关于该反应的说法中正确的是__ (填序号)。
A.该反应中S2O 表现了氧化性
表现了氧化性
B.已知生成的Fe2O3纳米颗粒直径为10纳米,则Fe2O3纳米颗粒为胶体
C.该反应中H2O2作氧化剂
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐如NaNO2,则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.加入盐酸,观察是否有气泡产生
B.加入AgNO3溶液观察是否有沉淀生成
C.分别在它们的酸性溶液中加入FeCl2溶液,观察溶液颜色变化
(3)在酸性条件下,HNO2与KI反应,I-被氧化为I2,HNO2被还原为NO气体,写出该反应的离子方程式:
(4)S2O
 可以与H2O2、Fe2+反应制备Fe2O3纳米颗粒。
可以与H2O2、Fe2+反应制备Fe2O3纳米颗粒。①S2O
 中S的化合价为
中S的化合价为②该反应的离子方程式为:2Fe2++S2O
 +4H2O2+4OH-=Fe2O3+S2O
+4H2O2+4OH-=Fe2O3+S2O +6H2O
+6H2O下列关于该反应的说法中正确的是
A.该反应中S2O
 表现了氧化性
表现了氧化性B.已知生成的Fe2O3纳米颗粒直径为10纳米,则Fe2O3纳米颗粒为胶体
C.该反应中H2O2作氧化剂
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】对于数以千万计的化学物质和十分丰富的化学变化,分类法的作用几乎是无可替代的。某化学兴趣小组对下列四组物质进行研究:
A.HCl、 、
、 、
、
B. 、
、 、
、 、
、
C. 溶液、蒸馏水、
溶液、蒸馏水、 悬浊液、
悬浊液、 胶体
胶体
D.NaOH、KOH、 、
、
(1)完整有表中序号①②的内容;
①___________ ;②___________
(2)写出上表中“不属于该类别的物质”发生反应的离子方程式。
A+B→气体:___________ ;
A+D:___________ ;
(3)该活动小组进行 胶体的制备实验并检验其性质。若将饱和
胶体的制备实验并检验其性质。若将饱和 溶液分别滴入下列液体中,能形成胶体的是___________。
溶液分别滴入下列液体中,能形成胶体的是___________。
(4) 胶体区别于
胶体区别于 溶液最本质的特征是___________。
溶液最本质的特征是___________。
(5)怎样检验制备的物质是否为胶体?___________
A.HCl、
 、
、 、
、
B.
 、
、 、
、 、
、
C.
 溶液、蒸馏水、
溶液、蒸馏水、 悬浊液、
悬浊液、 胶体
胶体D.NaOH、KOH、
 、
、
(1)完整有表中序号①②的内容;
| A组 | B组 | C组 | D组 | |
| 分类标准 | 含氧酸 | ①___________ | 分散系 | ___________ |
| 不属于该类别的物质 | ___________ |  | ②___________ |  |
(2)写出上表中“不属于该类别的物质”发生反应的离子方程式。
A+B→气体:
A+D:
(3)该活动小组进行
 胶体的制备实验并检验其性质。若将饱和
胶体的制备实验并检验其性质。若将饱和 溶液分别滴入下列液体中,能形成胶体的是___________。
溶液分别滴入下列液体中,能形成胶体的是___________。| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
 胶体区别于
胶体区别于 溶液最本质的特征是___________。
溶液最本质的特征是___________。A. 胶体粒子的直径在1~100nm之间 胶体粒子的直径在1~100nm之间 | B. 胶体具有丁达尔效应 胶体具有丁达尔效应 |
C. 胶体是均一的分散系 胶体是均一的分散系 | D. 胶体的分散质能透过滤纸 胶体的分散质能透过滤纸 |
您最近半年使用:0次
【推荐1】H2O是生命之源,对于下列涉及H2O的反应,请回答:
(1)下列某同学关于H2O的认识正确的是_____ (填选项序号)。
A.H2O属于非电解质
B.H2O既有氧化性也有还原性
C.水在Al(OH)3胶体中是分散剂,在雾中是分散质
(2)工业上利用反应C+H2O CO+H2制取水煤气,反应中的水作
CO+H2制取水煤气,反应中的水作_____ (选填“氧化剂”、“还原剂”、“氧化剂和还原剂”,下同)。
(3)单质铁可以和水蒸气发生反应,反应的化学方程式为:_____ ,当标况下产生8.96LH2时,消耗的铁的质量为_____ 。
(4)登山运动员常携带氢化钙作为生氢剂,反应方程式:CaH2+2H2O=Ca(OH)2+2H2↑,反应中的CaH2作_____ ,若反应中消耗4molH2O,反应中转移电子的数目为_____ 。
(1)下列某同学关于H2O的认识正确的是
A.H2O属于非电解质
B.H2O既有氧化性也有还原性
C.水在Al(OH)3胶体中是分散剂,在雾中是分散质
(2)工业上利用反应C+H2O
 CO+H2制取水煤气,反应中的水作
CO+H2制取水煤气,反应中的水作(3)单质铁可以和水蒸气发生反应,反应的化学方程式为:
(4)登山运动员常携带氢化钙作为生氢剂,反应方程式:CaH2+2H2O=Ca(OH)2+2H2↑,反应中的CaH2作
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】某课外活动小组进行 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。
(1)若将 溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)
溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)
(2)根据质量守恒定律,写出制备 胶体的化学反应方程式
胶体的化学反应方程式___________ ;
(3)取少量制得的胶体加入试管中,再加入少量 溶液,观察到的现象
溶液,观察到的现象___________ ;
(4) 胶体区别于
胶体区别于 溶液最本质的特征是___________;(填序号)
溶液最本质的特征是___________;(填序号)
(5)下列应用或事实与胶体的性质没有关系的是___________;(填序号)
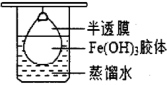
(6)将用(1)用正确方法制得的氢氧化铁胶体,放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察到___________ (填“有”或“无”)丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为___________ 。
 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。(1)若将
 溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)
溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
 胶体的化学反应方程式
胶体的化学反应方程式(3)取少量制得的胶体加入试管中,再加入少量
 溶液,观察到的现象
溶液,观察到的现象(4)
 胶体区别于
胶体区别于 溶液最本质的特征是___________;(填序号)
溶液最本质的特征是___________;(填序号)A. 胶体粒子的直径在1~100nm之间 胶体粒子的直径在1~100nm之间 |
B. 胶体具有丁达尔效应 胶体具有丁达尔效应 |
C. 胶体是均一的分散系 胶体是均一的分散系 |
D. 胶体的分散质粒子能透过滤纸 胶体的分散质粒子能透过滤纸 |
| A.用明矾净化饮用 |
B.在 溶液中滴加NaOH溶液出现红褐色沉淀 溶液中滴加NaOH溶液出现红褐色沉淀 |
| C.在河流入海处易形成沙洲 |
| D.用石膏或盐卤点制豆腐 |

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下面短文,并回答问题。
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射。在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应。产生丁达尔效应的实质是光的散射。
表1分散系对可见光的不同作用:
当入射光的波长略大于分散相粒子的直径时就发生光的散射。可见光的波长在400~760nm的范围,略大于一般胶体粒子的直径(1~100nm),因此当可见光束投射于胶体时,就发生光的散射,产生丁达尔效应。
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象。
(1)产生丁达尔效应的实质是_____ 。
(2)制备Fe(OH)3胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的_____ 溶液,继续煮沸至液体呈_____ 色即可。
(3)胶体区别于其他分散系的本质特征是_____ (填序号)。
A.胶体有丁达尔效应
B.胶体粒子可以透过滤纸
C.胶体的胶粒带有电荷
D.胶体粒子的直径在1~100nm之间
(4)CuSO4溶液无明显丁达尔效应的原因是_____ 。
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射。在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应。产生丁达尔效应的实质是光的散射。
表1分散系对可见光的不同作用:
| 溶液 | 胶体 | 浊液 | |
| 光路示意图 | 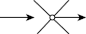 | 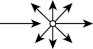 |  |
| 对光的主要作用 | 透射 | 散射 | 反射或折射 |
当入射光的波长略大于分散相粒子的直径时就发生光的散射。可见光的波长在400~760nm的范围,略大于一般胶体粒子的直径(1~100nm),因此当可见光束投射于胶体时,就发生光的散射,产生丁达尔效应。
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象。
(1)产生丁达尔效应的实质是
(2)制备Fe(OH)3胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的
(3)胶体区别于其他分散系的本质特征是
A.胶体有丁达尔效应
B.胶体粒子可以透过滤纸
C.胶体的胶粒带有电荷
D.胶体粒子的直径在1~100nm之间
(4)CuSO4溶液无明显丁达尔效应的原因是
您最近半年使用:0次



