金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
(2)高铁酸钠(Na2FeO4)是一种新型水处理剂。某兴趣小组欲利用废金属屑(主要成分为Fe和Cu,含有少量Fe2O3)制取高铁酸钠并回收金属Cu,其工艺流程如下:_______ (填化学式,下同),滤渣II的主要成分为_______ 。
②在过滤操作中要使用玻璃棒,其作用是_______ 。
③检验滤液I中是否存在Fe3+的试剂是_______ 。
④制备 的反应原理是:
的反应原理是: 。当反应中转移电子总数约为
。当反应中转移电子总数约为 时,则生成Na2FeO4的物质的量为
时,则生成Na2FeO4的物质的量为_______ mol。
(3)纳米铁粉可用于处理废水中的 。酸性条件下,纳米铁粉与废水中
。酸性条件下,纳米铁粉与废水中 反应生成Fe3+与
反应生成Fe3+与 ,其反应的离子方程式是
,其反应的离子方程式是_______ 。
(1)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______。
| A.Mg2+ | B.Fe2+ | C.A13+ | D.Cu2+ |
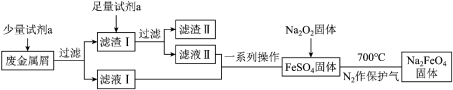
②在过滤操作中要使用玻璃棒,其作用是
③检验滤液I中是否存在Fe3+的试剂是
④制备
 的反应原理是:
的反应原理是: 。当反应中转移电子总数约为
。当反应中转移电子总数约为 时,则生成Na2FeO4的物质的量为
时,则生成Na2FeO4的物质的量为(3)纳米铁粉可用于处理废水中的
 。酸性条件下,纳米铁粉与废水中
。酸性条件下,纳米铁粉与废水中 反应生成Fe3+与
反应生成Fe3+与 ,其反应的离子方程式是
,其反应的离子方程式是
22-23高一上·江西宜春·期中 查看更多[4]
新疆阿克苏市第四高级中学2023-2024学年高三上学期第二次月考化学试卷(已下线)化学(云南,安徽,黑龙江,山西,吉林五省通用B卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)化学(云南,安徽,黑龙江,山西,吉林五省通用A卷)-学易金卷:2023年高考第一次模拟考试卷江西省丰城中学2022-2023学年高一上学期期中考试化学试题(创新班)
更新时间:2022-10-30 16:12:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)宇航员常用过氧化钠作供氧剂,写出对应反应的化学方程__ 、__ 。
(2)新制氯水在阳光照射下容易分解产生无色气体,该反应的化学方程式是__ 。
工业上将氯气通入冷的消石灰制成漂白粉,写出该反应的化学方程式并用双线桥法表示电子转移的方向和数目的__ 。
(3)KAl(SO4)2·12H2O因其溶于水生成__ (化学式)胶体可以吸附杂质,从而达到净水的目的。
(4)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是__ ,当反应中有1molK2FeO4生成时,消耗的Cl2在标准状况下的体积为__ L,转移电子的数目为__ 。
(1)宇航员常用过氧化钠作供氧剂,写出对应反应的化学方程
(2)新制氯水在阳光照射下容易分解产生无色气体,该反应的化学方程式是
工业上将氯气通入冷的消石灰制成漂白粉,写出该反应的化学方程式并用双线桥法表示电子转移的方向和数目的
(3)KAl(SO4)2·12H2O因其溶于水生成
(4)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH
 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钠元素在自然界都以化合物的形式存在。
(1)过氧化钠用于呼吸面具的反应方程式为___________ ,假设每分钟消耗氧气1.6g,若佩戴呼吸面具1小时,需要消耗 的质量
的质量___________ g。
(2)若要除去 溶液中的
溶液中的 ,发生反应的化学方程式为
,发生反应的化学方程式为___________ 。
(3)某课外活动小组为了检验钠与水反应的产物,设计了装置如下图(夹持装置省略)。首先在U形管内加入少量煤油和几小块钠,再从U形管高端加入水(含有酚酞),赶出空气,一会儿后加热铜丝。

①金属钠的变化:与水剧烈反应,在水和煤油的交界处上下浮动并逐渐变小
②U形管中溶液发生的离子反应方程式:___________ 。
③装置B中铜丝的变化:___________ ;该反应的化学方程式为:___________ 。
(1)过氧化钠用于呼吸面具的反应方程式为
 的质量
的质量(2)若要除去
 溶液中的
溶液中的 ,发生反应的化学方程式为
,发生反应的化学方程式为(3)某课外活动小组为了检验钠与水反应的产物,设计了装置如下图(夹持装置省略)。首先在U形管内加入少量煤油和几小块钠,再从U形管高端加入水(含有酚酞),赶出空气,一会儿后加热铜丝。

①金属钠的变化:与水剧烈反应,在水和煤油的交界处上下浮动并逐渐变小
②U形管中溶液发生的离子反应方程式:
③装置B中铜丝的变化:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(1)该反应中氧化剂是_______ (填化学式,下同),还原剂是_______ ,_______ 元素被氧化,还原产物为_______ 。
(2)用单线桥在方程式中标出电子转移情况:_______ 。
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(3)当反应中有1个 离子生成时,转移的电子数是
离子生成时,转移的电子数是_______ 个。
(1)该反应中氧化剂是
(2)用单线桥在方程式中标出电子转移情况:
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(3)当反应中有1个
 离子生成时,转移的电子数是
离子生成时,转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】1.四氧化三铁在强碱性溶液中与次氯酸盐反应,生成高铁(VI)酸盐,其化学反应方程式是_______ 。高铁酸盐的作用之一是净化水,这是因为_______ 、_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填空。
(1)松油醇( )的官能团的名称为
)的官能团的名称为_____________________ 。
(2)苯与浓硫酸和浓硝酸的混合液共热__________________________ 。
(3)1,3—丁二烯制备1,4-二溴-2-丁烯____________________________________ 。
(4)燃烧法是测定有机化合物化学式的一种重要方法。在一定温度下取0.1mol某液态烃A在O2中完全燃烧,生成CO2和水蒸气,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重16.2g,碱石灰增重35.2g。则烃A的分子式____________ ,含三个甲基的烃A同分异构体的数目为___ ,烃A的一种同分异构体,其核磁共振氢谱只有一个吸收峰,写出该同分异构体的结构简式_________________ 。
(5)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____ Fe(OH)3 +____ ClO-+____ OH- =__ FeO42-+___ Cl-+_______ 。
(1)松油醇(
 )的官能团的名称为
)的官能团的名称为(2)苯与浓硫酸和浓硝酸的混合液共热
(3)1,3—丁二烯制备1,4-二溴-2-丁烯
(4)燃烧法是测定有机化合物化学式的一种重要方法。在一定温度下取0.1mol某液态烃A在O2中完全燃烧,生成CO2和水蒸气,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重16.2g,碱石灰增重35.2g。则烃A的分子式
(5)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
您最近一年使用:0次



