1.四氧化三铁在强碱性溶液中与次氯酸盐反应,生成高铁(VI)酸盐,其化学反应方程式是_______ 。高铁酸盐的作用之一是净化水,这是因为_______ 、_______ 。
2007高二·安徽·竞赛 查看更多[1]
更新时间:2021-08-07 16:22:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】
(1)在常温下,发生下列几种反应:
①16H++10Z-+2XO =2X2++5Z2+8H2O
=2X2++5Z2+8H2O
②2A2++B2=2A3++2B-
③2B-+Z2=B2+2Z-
根据上述反应,XO 、Z2、B2、A3+氧化性从强到弱的顺序为:
、Z2、B2、A3+氧化性从强到弱的顺序为:_________________
(2)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO + 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+ 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
①写出并配平该氧化还原反应的化学方程式_____________________ ;
②反应中硝酸体现了______________ ;
③反应中若产生标准状况下11.2L气体,则转移电子的物质的量是________ mol;
(1)在常温下,发生下列几种反应:
①16H++10Z-+2XO
 =2X2++5Z2+8H2O
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-
③2B-+Z2=B2+2Z-
根据上述反应,XO
 、Z2、B2、A3+氧化性从强到弱的顺序为:
、Z2、B2、A3+氧化性从强到弱的顺序为:(2)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO
 + 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+ 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。①写出并配平该氧化还原反应的化学方程式
②反应中硝酸体现了
③反应中若产生标准状况下11.2L气体,则转移电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】 、
、 和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
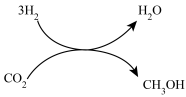
(1)利用 可合成多种化工产品。
可合成多种化工产品。
2021年9月24日我国科学家首次报告了 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为___________ 。
(2)氨氮废水是造成河流及湖泊富营养化的主要因素。
①某氮肥厂产生的氨氮废水中的氮元素多以 和
和 的形式存在,我们可以通过一些化学方法把
的形式存在,我们可以通过一些化学方法把 和
和 转化为
转化为 。
。 在催化剂的作用会和氧气发生反应,该反应的化学方程式为
在催化剂的作用会和氧气发生反应,该反应的化学方程式为___________ 。
②某团队设计处理氨氮废水的流程如下:

过程Ⅰ为硝化过程,在微生物的作用下实现 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应离子方程式为
的总反应离子方程式为___________ 。过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇( )实现
)实现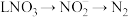 的转化,将
的转化,将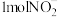 完全转化为
完全转化为 转移电子的物质的量为
转移电子的物质的量为___________ 。
(3)硫酸生产及煤燃烧过程中产生的废气 等会对大气造成污染,可用氨水吸收
等会对大气造成污染,可用氨水吸收 或采用钙基固硫法。
或采用钙基固硫法。 属于
属于___________ (填“电解质”或“非电解质”),氨水吸收少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
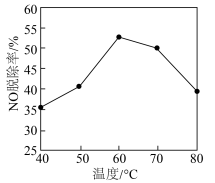
(4)氮的氧化物(NO、 等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的
等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的 溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是___________ 。
 、
、 和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
(1)利用
 可合成多种化工产品。
可合成多种化工产品。2021年9月24日我国科学家首次报告了
 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为(2)氨氮废水是造成河流及湖泊富营养化的主要因素。
①某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 的形式存在,我们可以通过一些化学方法把
的形式存在,我们可以通过一些化学方法把 和
和 转化为
转化为 。
。 在催化剂的作用会和氧气发生反应,该反应的化学方程式为
在催化剂的作用会和氧气发生反应,该反应的化学方程式为②某团队设计处理氨氮废水的流程如下:

过程Ⅰ为硝化过程,在微生物的作用下实现
 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应离子方程式为
的总反应离子方程式为 )实现
)实现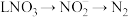 的转化,将
的转化,将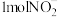 完全转化为
完全转化为 转移电子的物质的量为
转移电子的物质的量为(3)硫酸生产及煤燃烧过程中产生的废气
 等会对大气造成污染,可用氨水吸收
等会对大气造成污染,可用氨水吸收 或采用钙基固硫法。
或采用钙基固硫法。 属于
属于 ,反应的离子方程式为
,反应的离子方程式为(4)氮的氧化物(NO、
 等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的
等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的 溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】砷(As)是第ⅤA族元素,它在自然界中的含量不高,但人类认识它的历史很长,碑的某些化合物具有独特的性质与用途,如 在医药、电子等领域有重要应用,我国科学家研究发现砒霜(
在医药、电子等领域有重要应用,我国科学家研究发现砒霜( )可用来治疗早期幼粒白血病。
)可用来治疗早期幼粒白血病。
(1) 中碑的化合价为
中碑的化合价为_______ ,从物质化学性质角度看, 不可能是
不可能是_______ (填“酸”“碱”或“两”)性氧化物。
(2)某化工厂利用含硫化碑( )的废料制取
)的废料制取 (微溶于水)的流程如下。
(微溶于水)的流程如下。
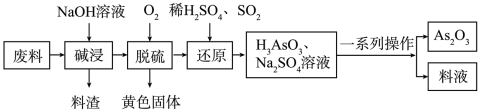
①写出两种能提高“碱浸”速率的方法:_______ ,一系列操作包括加热使 分解成氧化物、
分解成氧化物、_______ 、干燥得到 。
。
②碱浸液中溶质主要为 、
、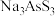 ,脱硫后以
,脱硫后以 的形式存在,写出
的形式存在,写出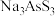 与
与 反应的化学方程式:还原后砷以
反应的化学方程式:还原后砷以 ,形式存在,则通入
,形式存在,则通入 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为_______ 。
 在医药、电子等领域有重要应用,我国科学家研究发现砒霜(
在医药、电子等领域有重要应用,我国科学家研究发现砒霜( )可用来治疗早期幼粒白血病。
)可用来治疗早期幼粒白血病。(1)
 中碑的化合价为
中碑的化合价为 不可能是
不可能是(2)某化工厂利用含硫化碑(
 )的废料制取
)的废料制取 (微溶于水)的流程如下。
(微溶于水)的流程如下。
①写出两种能提高“碱浸”速率的方法:
 分解成氧化物、
分解成氧化物、 。
。②碱浸液中溶质主要为
 、
、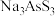 ,脱硫后以
,脱硫后以 的形式存在,写出
的形式存在,写出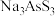 与
与 反应的化学方程式:还原后砷以
反应的化学方程式:还原后砷以 ,形式存在,则通入
,形式存在,则通入 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。
①把FeO、Fe2O3先溶于足量的稀盐酸中、再通入适量的氯气则可制取FeCl3溶液。FeO、Fe2O3溶于足量的稀盐酸中,在上述溶液中通入适量的氯气时发生的反应的离子方程式为 ____________________ 。若要检验溶液中Fe3+存在应选用的试剂是_____________________ 。
②写出FeCl3溶液与金属铜发生反应的化学方程式___________________________________ ,当转移电子数为6.02×1024时,被氧化的物质的质量为_______________
①把FeO、Fe2O3先溶于足量的稀盐酸中、再通入适量的氯气则可制取FeCl3溶液。FeO、Fe2O3溶于足量的稀盐酸中,在上述溶液中通入适量的氯气时发生的反应的离子
②写出FeCl3溶液与金属铜发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Fe3O4一种黑色粉末,又称磁性氧化铁,它的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
▲提出假设:假设1. 黑色粉末是CuO;假设2. 黑色粉末是Fe3O4;
假设3.______________________________ 。
▲设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
⑴若假设1成立,则实验现象是______________________ 。
⑵若所得溶液显血红色,则假设_________ 成立。
⑶为进一步探究,继续向所得溶液加入足量铁粉,若产生______________ 的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
⑷为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若产生________________ 现象,则假设2成立;若产生_____________________ 现象,则假设3成立。
▲提出假设:假设1. 黑色粉末是CuO;假设2. 黑色粉末是Fe3O4;
假设3.
▲设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
⑴若假设1成立,则实验现象是
⑵若所得溶液显血红色,则假设
⑶为进一步探究,继续向所得溶液加入足量铁粉,若产生
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
⑷为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若产生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.高铁酸钾(K2FeO4)是兼具杀菌消毒和吸附絮凝功能的高效水处理剂。
(1)K2FeO4在处理污水时,与水体中的___________ 物质反应生成Fe3+。
A.氧化性 B.还原性
(2)Fe3+再水解生成Fe(OH)3胶体,起到吸附絮凝作用,这与胶体的___________ 有关。
A.丁达尔现象 B.电泳 C.聚沉
Ⅱ.电解法制备K2FeO4:装置如图所示,原理为 。
。
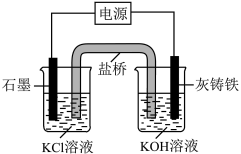
(3)灰铸铁材料作___________极。
(4)电解时,左侧烧杯中溶液的pH___________ 。
A.升高 B.降低 C.不变
(5)写出电解时石墨电极反应式___________ 。
(1)K2FeO4在处理污水时,与水体中的
A.氧化性 B.还原性
(2)Fe3+再水解生成Fe(OH)3胶体,起到吸附絮凝作用,这与胶体的
A.丁达尔现象 B.电泳 C.聚沉
Ⅱ.电解法制备K2FeO4:装置如图所示,原理为
 。
。
(3)灰铸铁材料作___________极。
| A.正 | B.负 | C.阴 | D.阳 |
(4)电解时,左侧烧杯中溶液的pH
A.升高 B.降低 C.不变
(5)写出电解时石墨电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】阅读下面两条科普信息,回答有关问题:
一个体重50kg的健康人身体中含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收:
在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿:该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛CH2O表示)。
(1)这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径。这说明维生素C具有______ 性,铁离子具有_______ 性,第二则则信息中CO2是_________ 剂。
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
__ Fe(NO3)3 +__ NaOH+ __ Cl2 → __ Na2FeO4+ __ NaNO3 + __ NaCl + __ H2O
①配平上述反应,并分析_______ 元素被氧化,当生成3mol还原产物时,转移电子的总数为______ ;
②铁酸钠除了能消毒外,还可以用于净水,原因是_____________________ 。
一个体重50kg的健康人身体中含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收:
在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿:该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛CH2O表示)。
(1)这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径。这说明维生素C具有
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
①配平上述反应,并分析
②铁酸钠除了能消毒外,还可以用于净水,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁是人体中必需微量元素中含量最多,体内缺失会引起贫血。含FeO42-离子的盐具有强氧化性,能杀菌消毒,如高铁酸钾是一种新型、高效的消毒剂及绿色净水剂。铁及其化合物之间的相互转化可用下式表示: ,请回答下列有关问题:
,请回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净。可选用的试剂是___________ (选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+→Cu2++5Fe2++2S,
则下列说法正确的是_________ (选填序号);
a.反应中,所有铁元素均被还原
b.从物质的组成来看,黄铜矿属于复盐
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol 电子时,有46 g CuFeS2参加反应
(3)下列是工业制取高铁酸钾的一种方法,请在方框内填上合适的微粒符号并配平该离子方程式:
_______ Fe3+ +______ _________ +______ Cl2→_____ FeO42- + _____ Cl- +___ _____
 ,请回答下列有关问题:
,请回答下列有关问题:(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净。可选用的试剂是
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+→Cu2++5Fe2++2S,
则下列说法正确的是
a.反应中,所有铁元素均被还原
b.从物质的组成来看,黄铜矿属于复盐
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol 电子时,有46 g CuFeS2参加反应
(3)下列是工业制取高铁酸钾的一种方法,请在方框内填上合适的微粒符号并配平该离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在日光照射下,O2、F2和AsF5以2:1:2(物质的量比)混合反应,只生成离子化合物X,X中阳离子为O ,此化学反应方程式为
,此化学反应方程式为___ ,其中O2为___ 剂,F2为___ 剂。而阴离子的空间构型为___ 构型,其中心原子的杂化轨道类型为___ 。X是一种强氧化剂,它可氧化Br2,生成离子化合物Y(其中Br的质量分数为55.93%)和一种助燃气。Y也可用Br2、BrF5和AsF5混合后通过化合反应制得,且X与Y的阴离子相同,写出该反应的化学方程式___ 。此反应中Br2是___ 剂,BrF5是___ 剂。Y中阳离子的空间构型为___ 型,其中心原子的杂化轨道类型为___ 。
 ,此化学反应方程式为
,此化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氰化物电镀的废液中含多种金属离子与氰离子(CN-)的络离子,如Cu(CN) 。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:
。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:
(1)氰离子和次氯酸根的反应可按氰离子中的氮呈负氧化态(负价),碳呈正氧化态(正价)进行_______ 。
□CN-+□ClO-+□OH-=□+□+□+□H2O
(2)_______
□Cu(CN) +□ClO-+□OH-=□+□+□+□+□
+□ClO-+□OH-=□+□+□+□+□
在本反应中的得失电子数相等,是_______ 个电子?
 。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:
。废液排放前,必须将剧毒的氰离子完全氧化。在废液中加入漂白粉可将这些络离子完全氧化而从废液中除去。完成下列反应方程式:(1)氰离子和次氯酸根的反应可按氰离子中的氮呈负氧化态(负价),碳呈正氧化态(正价)进行
□CN-+□ClO-+□OH-=□+□+□+□H2O
(2)
□Cu(CN)
 +□ClO-+□OH-=□+□+□+□+□
+□ClO-+□OH-=□+□+□+□+□在本反应中的得失电子数相等,是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一,氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O。投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式:KOCN+KOH+Cl2—CO2+N2+KCl+H2O,_______ 。
(2)若处理上述废水100L,使KCN完全转化为无毒物质,至少需要投放液氯多少克?_______
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出:
①(CN)2与KOH溶液反应的化学方程式:_______ 。
②在NaBr和KSCN的混合溶液中滴加少量(CN)2,反应的离子方程_______ 。
(1)某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O。投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式:KOCN+KOH+Cl2—CO2+N2+KCl+H2O,
(2)若处理上述废水100L,使KCN完全转化为无毒物质,至少需要投放液氯多少克?
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出:
①(CN)2与KOH溶液反应的化学方程式:
②在NaBr和KSCN的混合溶液中滴加少量(CN)2,反应的离子方程
您最近一年使用:0次

 恰好完全沉淀,写出反应的离子方程式:
恰好完全沉淀,写出反应的离子方程式:

