某同学做了以下探究实验:在甲、乙两只塑料袋中分别放入4粒成熟程度接近的生葡萄,向甲中又放进一粒熟葡萄,将两只塑料袋袋口扎紧。经过一段时间的观察,该同学发现两只塑料袋中的生葡萄变熟所需时间长短不同。
(1)请指出哪只塑料袋中的生葡萄先成熟,并说明理由_________ 。
(2)结合所学化学知识,设计简单易行的葡萄保鲜方案_________ 。
(1)请指出哪只塑料袋中的生葡萄先成熟,并说明理由
(2)结合所学化学知识,设计简单易行的葡萄保鲜方案
更新时间:2022-11-25 20:06:04
|
相似题推荐
【推荐1】回答下列问题
(1)烷烃的通式是:_______ ,烷烃分子中的碳原子数目每增加一个,其相对分子质量增加_______ 。
(2)乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请问:乙烯的结构式_______ ,鉴别甲烷和乙烯的试剂是_______ (填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列反应中,属于取代反应的是_______ ,属于加成反应的是_______ ,属于氧化反应的是_______ 。(填序号
A.工业由乙烯制乙醇 B.乙烷在光照下与氯气反应
C.甲烷在空气中燃烧 D.乙烯使酸性高锰酸钾溶液褪色
(1)烷烃的通式是:
(2)乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请问:乙烯的结构式
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列反应中,属于取代反应的是

A.工业由乙烯制乙醇 B.乙烷在光照下与氯气反应
C.甲烷在空气中燃烧 D.乙烯使酸性高锰酸钾溶液褪色
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列实验操作或对实验事实的描述中正确的说法有_______ 。
①分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
②除去甲烷中混有的少量乙烯,可以让混合物通过盛有酸性KMnO4溶液的洗气装置
③将无水乙醇和3mol·L-1 H2SO4混合加热到170℃,可制得乙烯
④只用溴水就可将苯、四氯化碳、乙醇、己烯四种液体区别开来
⑤用分液法分离苯和硝基苯的混合物
①分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
②除去甲烷中混有的少量乙烯,可以让混合物通过盛有酸性KMnO4溶液的洗气装置
③将无水乙醇和3mol·L-1 H2SO4混合加热到170℃,可制得乙烯
④只用溴水就可将苯、四氯化碳、乙醇、己烯四种液体区别开来
⑤用分液法分离苯和硝基苯的混合物
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】烯烃与酸性 溶液反应被氧化的部分与氧化产物的对应关系如下表:
溶液反应被氧化的部分与氧化产物的对应关系如下表:
(1)苯乙烯与酸性 溶液反应后所得氧化产物为
溶液反应后所得氧化产物为___________ 。
(2)现有某烃A的分子式为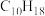 ,经催化加氢后得到化合物B,其分子式为
,经催化加氢后得到化合物B,其分子式为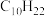 ,A与酸性
,A与酸性 溶液作用可得如下三种化合物:
溶液作用可得如下三种化合物: 、
、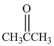 、
、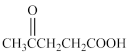 ,则A的结构简式为___________。
,则A的结构简式为___________。
(3)现有某烃C的分子式为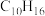 ,经催化加氢得到产物D,其分子式为
,经催化加氢得到产物D,其分子式为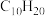 ,C与酸性
,C与酸性 溶液作用可得到等物质的量的两种含碳化合物:
溶液作用可得到等物质的量的两种含碳化合物: 与
与 ,经分析有关数据知D内含六元碳环。试写出C的结构简式:
,经分析有关数据知D内含六元碳环。试写出C的结构简式:___________ 。
 溶液反应被氧化的部分与氧化产物的对应关系如下表:
溶液反应被氧化的部分与氧化产物的对应关系如下表:| 烯烃被氧化的部分 | 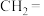 | 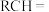 |  |
| 氧化产物 |  |  | 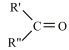 |
 溶液反应后所得氧化产物为
溶液反应后所得氧化产物为(2)现有某烃A的分子式为
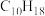 ,经催化加氢后得到化合物B,其分子式为
,经催化加氢后得到化合物B,其分子式为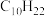 ,A与酸性
,A与酸性 溶液作用可得如下三种化合物:
溶液作用可得如下三种化合物: 、
、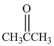 、
、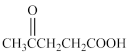 ,则A的结构简式为___________。
,则A的结构简式为___________。A. 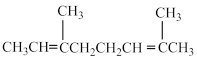 | B. 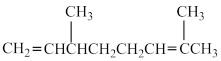 |
C.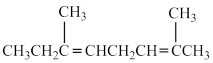 | D.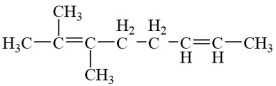 |
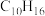 ,经催化加氢得到产物D,其分子式为
,经催化加氢得到产物D,其分子式为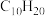 ,C与酸性
,C与酸性 溶液作用可得到等物质的量的两种含碳化合物:
溶液作用可得到等物质的量的两种含碳化合物: 与
与 ,经分析有关数据知D内含六元碳环。试写出C的结构简式:
,经分析有关数据知D内含六元碳环。试写出C的结构简式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将物质与其用途连线
第一组:_________ ;第二组:__________ 。
第一组 | 第二组 |
物质 用途 A.乙烯 a.作消毒剂 B.次氯酸钠 b.制乙醇 C.甲烷 c.作干燥剂 D.浓硫酸 d.作燃料 | 物质 用途 A.酒精 a.清除水垢 B.醋酸 b.作医用消毒剂 C.二氧化硫 c.作供氧剂 D.过氧化钠 d.制硫酸 |
第一组:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】烯烃是烃类物质中非常重要的一类烃,应用非常广泛。请回答下列问题:
(1)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱图表明分子中含有碳碳双键,核磁共振氢谱图表明分子中只有1种类型的氢原子。
①A的结构简式为__ ;
②A分子中的碳原子是否处于同一平面?__ (填“是”或者“不是”)
(2)烯烃与高锰酸钾酸性溶液反应的氧化产物有如下关系:
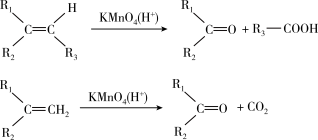
①乙烯是结构最简单的烯烃,写出实验室制取乙烯的反应方程式__ ,要除去混在甲烷中的乙烯,能否通过酸性高锰酸钾溶液来达到实验目的?__ (填“能”或“不能”),理由是__ 。乙烯是一种基本的化工原料,它的产量可用来衡量一个国家石油化工发展的水平,除此之外乙烯还可用作__ 。
②已知某烯烃的分子式为C5H10,与高锰酸钾酸性溶液反应的氧化产物之一为CO2,则满足条件的烯烃有___ 种结构(用数字作答);若与高锰酸钾酸性溶液反应的氧化产物为丙酮和乙酸,则满足条件的烯烃结构简式为___ 。
(1)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱图表明分子中含有碳碳双键,核磁共振氢谱图表明分子中只有1种类型的氢原子。
①A的结构简式为
②A分子中的碳原子是否处于同一平面?
(2)烯烃与高锰酸钾酸性溶液反应的氧化产物有如下关系:

①乙烯是结构最简单的烯烃,写出实验室制取乙烯的反应方程式
②已知某烯烃的分子式为C5H10,与高锰酸钾酸性溶液反应的氧化产物之一为CO2,则满足条件的烯烃有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据要求填写:
(1)金属钠在空气中燃烧,火焰呈__ 色,化学方程式:_______________________ ;
(2)将过氧化钠固体放入试管中加入少量水,再加入几滴酚酞试液,溶液变红色但很快褪色,原因是:_____________________________________ ,过氧化钠固体与水反应的化学方程式:______________________________________________ ;
(3)苏打和小苏打分别和同浓度的盐酸反应,反应较快且剧烈的是______ (填化学式),小苏打与盐酸反应的离子方程式为:________________________________________ ;
(4)金属钠和金属钾分别和水反应试验中,其中反应较剧烈的反应的化学方程式:___________________________________________ ;
(1)金属钠在空气中燃烧,火焰呈
(2)将过氧化钠固体放入试管中加入少量水,再加入几滴酚酞试液,溶液变红色但很快褪色,原因是:
(3)苏打和小苏打分别和同浓度的盐酸反应,反应较快且剧烈的是
(4)金属钠和金属钾分别和水反应试验中,其中反应较剧烈的反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
(1)设计实验检验FeSO4溶液的变质程度
①将上述方案补充完整。
②若要使部分变质的FeSO4复原,方法是___________ (写离子反应方程式) 。
(2)利用部分变质的FeSO4溶液制备Fe2O3

①请在( )内填写所需试剂或条件___________ 、___________ 、___________ ,在□内填写含铁物质的化学式___________ 、___________ (以离子形式存在的可写离子符号)。
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的物质的量浓度为___________ 。
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由___________ 。
(1)设计实验检验FeSO4溶液的变质程度
| 实验方案 | 实验现象 | 离子方程式 | 实验结论 | |
| 步骤1 | 取待检测液于试管中,向其中滴加KSCN溶液 | FeSO4溶液部分变质 | ||
| 步骤2 | ||||
②若要使部分变质的FeSO4复原,方法是
(2)利用部分变质的FeSO4溶液制备Fe2O3

①请在( )内填写所需试剂或条件
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的物质的量浓度为
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
| 实验方案 | 实验现象 |
| 取适量 Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某化学兴趣小组利用铁粉、锌粉、0.1mol•L-1FeCl3溶液、0.1mol•L-1FeCl2溶液、KSCN溶液和新制氯水来探究Fe2+、Fe3+的氧化性、还原性。
(1)用上述所给物质写出体现Fe2+具有还原性的化学方程式:_______ 。
(2)设计实验方案,完成下列表格。
①处的现象为_______ ;①处加入铁粉后反应的离子方程式为__ ;②处的现象为_______ ;
(3)取一定量氯化亚铁固体,配制成0.1mol•L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_______ 。
(4)该兴趣小组为探究“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,该反应的离子方程式为___ 。
(1)用上述所给物质写出体现Fe2+具有还原性的化学方程式:
(2)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
| 探究Fe3+具有氧化性 | 取少量0.1mol/LFeCl3溶液中加入足量铁粉,再加入少量KSCN溶液 | 加入铁粉后,溶液颜色变为①___;加入KSCN溶液后,溶液②____ |
①处的现象为
(3)取一定量氯化亚铁固体,配制成0.1mol•L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(4)该兴趣小组为探究“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,该反应的离子方程式为
您最近一年使用:0次



