下表为 、
、 、
、 的部分电离能(
的部分电离能( )数值。
)数值。
分析上表中各元素电离能的变化,回答下列问题:
(1) 、
、 、
、 元素的第一电离能从大到小的顺序是
元素的第一电离能从大到小的顺序是__________
(2)为什么同一元素的各级电离能逐级增大?__________
(3)上表中所呈现的电离能变化规律与三种元素的原子结构有什么关联?__________
 、
、 、
、 的部分电离能(
的部分电离能( )数值。
)数值。| 电离能 | 元素 | ||
 |  |  | |
 | 496 | 738 | 577 |
 | 4562 | 1451 | 1817 |
 | 6912 | 7733 | 2745 |
 | 9543 | 10540 | 11575 |
(1)
 、
、 、
、 元素的第一电离能从大到小的顺序是
元素的第一电离能从大到小的顺序是(2)为什么同一元素的各级电离能逐级增大?
(3)上表中所呈现的电离能变化规律与三种元素的原子结构有什么关联?
更新时间:2022-11-27 16:12:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某化学研究员设计了一种结构有趣的“糖葫芦”分子,结构如图。回答下列问题:
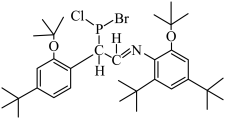
(1)该“糖葫芦”分子所含的元素C、N、O、P中,N的第一电离能最大,原因是___________ ;C、N、O均能形成 键,P只能形成
键,P只能形成 键不能形成
键不能形成 键,原因是
键,原因是___________ ;该分子中一定不存在的作用力是___________ (填字母)。
a.离子键 b. 键 c.
键 c. 键
键
(2)分子式为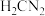 的物质有多种,他们分别是氰胺、碳化亚胺、M、R等物质。
的物质有多种,他们分别是氰胺、碳化亚胺、M、R等物质。
①氰胺的电子式为___________ ,分子中最多有___________ 个原子共面。
②碳化二亚胺的结构简式为HN=C=NH,该分子中N和C的杂化方式分别为___________ 、___________ 。
③M、R的分子结构均为三元环,M分子中的两个N原子杂化方式不同,R中的两个N原子杂化方式相同,分别写出M、R的结构简式:___________ 、___________ 。

(1)该“糖葫芦”分子所含的元素C、N、O、P中,N的第一电离能最大,原因是
 键,P只能形成
键,P只能形成 键不能形成
键不能形成 键,原因是
键,原因是a.离子键 b.
 键 c.
键 c. 键
键(2)分子式为
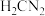 的物质有多种,他们分别是氰胺、碳化亚胺、M、R等物质。
的物质有多种,他们分别是氰胺、碳化亚胺、M、R等物质。①氰胺的电子式为
②碳化二亚胺的结构简式为HN=C=NH,该分子中N和C的杂化方式分别为
③M、R的分子结构均为三元环,M分子中的两个N原子杂化方式不同,R中的两个N原子杂化方式相同,分别写出M、R的结构简式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】开发太阳能资源,寻求经济发展的新动力是目前各国政府均很重视的工作。请回答下列问题:
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的核外电子排布式:_______________________________________ 。
(2)多元化合物薄膜太阳能电池的材料主要为无机盐,这些无机盐包括砷化镓、硫化镉、硫化锌及铜、铟、镓、硒等。
①请比较元素的第一电离能:As_________ P(填“>”“<”或“=”)。
②二氧化硒分子的立体构型为________________ 。
(3)镍可形成配合物Ni(CO)5,Ni(CO)5在一定条件下发生分解反应:Ni(CO)5(s) Ni(s)+5CO(g),反应产物中Ni形成的金属晶体内部原子堆积方式与铜相同,则Ni金属晶体晶胞空间利用率为
Ni(s)+5CO(g),反应产物中Ni形成的金属晶体内部原子堆积方式与铜相同,则Ni金属晶体晶胞空间利用率为________________ ,则Ni原子配位数为________________ 。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的核外电子排布式:
(2)多元化合物薄膜太阳能电池的材料主要为无机盐,这些无机盐包括砷化镓、硫化镉、硫化锌及铜、铟、镓、硒等。
①请比较元素的第一电离能:As
②二氧化硒分子的立体构型为
(3)镍可形成配合物Ni(CO)5,Ni(CO)5在一定条件下发生分解反应:Ni(CO)5(s)
 Ni(s)+5CO(g),反应产物中Ni形成的金属晶体内部原子堆积方式与铜相同,则Ni金属晶体晶胞空间利用率为
Ni(s)+5CO(g),反应产物中Ni形成的金属晶体内部原子堆积方式与铜相同,则Ni金属晶体晶胞空间利用率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
I.用元素符号表示
(1)将钠、镁、铝各2g分别投入盛足量0.05mol/L盐酸烧杯中,实验结果:____ 与盐酸反应最剧烈;_____ 与盐酸反应转移电子最多。钠、镁、铝中第一电离能由小到大的顺序是_____ 。
(2)向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明____ 元素得电子能力强,反应的离子方程式为_______ 。实验结论:随原子序数增大,同周期元素失电子能力依次_______ (填“增强”或“减弱”,下同),得电子能力依次_______ 。
II.利用如图装置可验证同主族元素非金属性的变化规律。
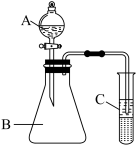
(3)仪器A的名称为_______ 。
(4)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是_______ ,此装置存在的不足之处是_______ 。
I.用元素符号表示
(1)将钠、镁、铝各2g分别投入盛足量0.05mol/L盐酸烧杯中,实验结果:
(2)向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明
II.利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器A的名称为
(4)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1)Se在周期表的位置为_____ ,硅的基态原子电子排布式为_____ ,基态Ga原子核外电子占据的最高能级为_____ ,铜的基态原子价电子排布图为______ 。
(2)P、S、Ga电负性从大到小的顺序为____________________ 。
(3)与Al元素在元素周期表中处于对角线的铍,在性质上具有相似性,请写出铍的氧化物与氢氧化钠溶液反应的离子方程式_______________________
(4)As元素的第一电离能_____ Se元素的第一电离能(填“大于”、“小于”或“等于”),原因是_______________ 。
(5)太阳电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是_________________________
(1)Se在周期表的位置为
(2)P、S、Ga电负性从大到小的顺序为
(3)与Al元素在元素周期表中处于对角线的铍,在性质上具有相似性,请写出铍的氧化物与氢氧化钠溶液反应的离子方程式
(4)As元素的第一电离能
(5)太阳电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是
您最近一年使用:0次
【推荐2】金属氢化物是具有良好发展前景的储氢材料。
(1)LiH中,离子半径:Li+_________ H-(填“>”、“=”或“<”)。
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_________ (填元素符号)。
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是_____ 。
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是_____________________ ;只含有σ键的是__________ ;含有由两个原子的s轨道重叠形成的σ键的是________ ;不存在化学键的是________ ;含有离子键和非极性键的是_________ 。
(1)LiH中,离子半径:Li+
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是
您最近一年使用:0次



