回答下列问题:
(1)钢铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题。
①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中正极的电极反应式为_______ 。
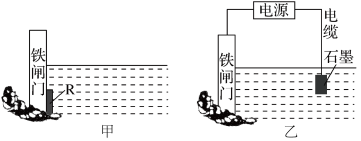
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料 可以采用
可以采用_______  填写字母序号
填写字母序号 。
。
A.铜 B.钠 C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,此种防护方法叫_______ 。
(2)在实际生产中,可在铁件的表面上镀铜防止铁被腐蚀。装置示意图如下图:
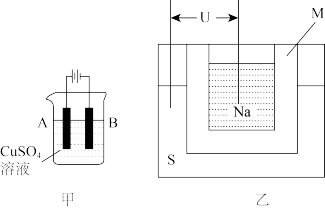
①甲图为电镀装置,镀件与电源的_______ 极连接,写出B电极反应式为_______ 。
② 图是一种钠硫高能电池的结构示意图,
图是一种钠硫高能电池的结构示意图, 由
由 和
和 制得,其作用是导电和隔膜,该电池总反应为
制得,其作用是导电和隔膜,该电池总反应为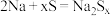 。该电池正极的电极反应式为
。该电池正极的电极反应式为_______ 。
(1)钢铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题。

①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中正极的电极反应式为
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料
 可以采用
可以采用 填写字母序号
填写字母序号 。
。A.铜 B.钠 C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,此种防护方法叫
(2)在实际生产中,可在铁件的表面上镀铜防止铁被腐蚀。装置示意图如下图:

①甲图为电镀装置,镀件与电源的
②
 图是一种钠硫高能电池的结构示意图,
图是一种钠硫高能电池的结构示意图, 由
由 和
和 制得,其作用是导电和隔膜,该电池总反应为
制得,其作用是导电和隔膜,该电池总反应为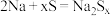 。该电池正极的电极反应式为
。该电池正极的电极反应式为
更新时间:2022-12-05 21:59:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一
Ⅰ.如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于电化学腐蚀。

(1)红墨水柱两边的液面变为左低右高,则___________ (填“a”或“b”)边盛有食盐水。
(2)b试管中铁发生的是___________ 腐蚀。
Ⅱ.下面两个图都是金属防护的例子。
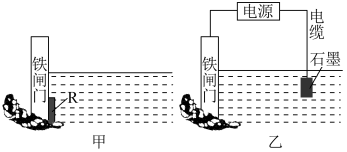
(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用___________ (从下面选项中选择),此方法叫做___________ 保护法。
A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的___________ 极。
(5)采取以上两种方法,___________ (填“甲”或“乙”)种能使铁闸门保护得更好。
Ⅰ.如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于电化学腐蚀。

(1)红墨水柱两边的液面变为左低右高,则
(2)b试管中铁发生的是
Ⅱ.下面两个图都是金属防护的例子。

(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的
(5)采取以上两种方法,
您最近一年使用:0次
【推荐2】电化学原理在金属防腐、物质制备方面有重要的作用。
I.将裹有锌片的铁钉放入溶有琼脂的饱和NaCl溶液中,滴入少量酚酞(如下图甲所示),回答下列问题。
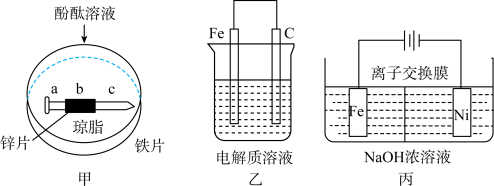
(1)一段时间后a处可能出现的现象是_______ ,请结合电化学原理解释原因________ 。
(2)某同学为验证选择的铁钉未被腐蚀,取少量溶液于试管,分别进行如表实验,能证明铁钉未被腐蚀的实验是___________ (填序号)
(3)钢铁的吸氧腐蚀简单示意图如上图乙所示,该图某处稍作修改即可成为钢铁电化学防护的简单示意图,请作出修改并标出电子流动方向___________ 。
II. 是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其电解制法如上图丙所示。通电后,铁电极附近生成紫红色的
是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其电解制法如上图丙所示。通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。
,镍电极有气泡产生。
已知: 只在强碱性条件下稳定,易被
只在强碱性条件下稳定,易被 还原。
还原。
(4)Fe电极发生的电极反应为:___________ 。
(5)电解过程中,须将阴极产生的气体及时排出,其原因是___________ 。
(6)该电解装置应使用___________ 离子交换膜(填“阳”或“阴”),当阴极产生112mL(标准状况)的气体时,通过离子交换膜的离子有___________ mol。
I.将裹有锌片的铁钉放入溶有琼脂的饱和NaCl溶液中,滴入少量酚酞(如下图甲所示),回答下列问题。

(1)一段时间后a处可能出现的现象是
(2)某同学为验证选择的铁钉未被腐蚀,取少量溶液于试管,分别进行如表实验,能证明铁钉未被腐蚀的实验是
| 序号 | ① | ② | ③ | ④ |
| 滴入试剂 |  溶液 溶液 | 淀粉KI溶液 | KSCN溶液 |  溶液 溶液 |
| 实验现象 | 产生沉淀 | 无蓝色出现 | 无红色出现 | 无蓝色沉淀 |
(3)钢铁的吸氧腐蚀简单示意图如上图乙所示,该图某处稍作修改即可成为钢铁电化学防护的简单示意图,请作出修改并标出电子流动方向
II.
 是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其电解制法如上图丙所示。通电后,铁电极附近生成紫红色的
是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其电解制法如上图丙所示。通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。
,镍电极有气泡产生。已知:
 只在强碱性条件下稳定,易被
只在强碱性条件下稳定,易被 还原。
还原。(4)Fe电极发生的电极反应为:
(5)电解过程中,须将阴极产生的气体及时排出,其原因是
(6)该电解装置应使用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.铝合金和钢铁是国家重要的金属材料。回答下列问题:
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有___________ (填序号)。A变为D所需的能量为E1,D变为E所需的能量为E2,则E1___________ E2(填“>”“<”或“=”),理由是___________ 。
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为___________ 。
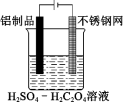
Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

通过上述实验分析回答:
(3)上述实验①、②探究___________ 对铁的腐蚀快慢的影响,写出实验②碳电极上的电极反应式___________ ;
(4)上述四个实验中___________ (用编号表示)发生吸氧腐蚀,上述四个实验铁腐蚀由快到慢的顺序为___________ (用编号表示)。
(1)下列是气态铝原子或离子的电子排布式,其中处于激发态的有
A.1s22s22p63s23p1 B.1s22s22p63s13px13py1 C.1s22s22p63s13px13pz1
D.1s22s22p63s2 E.1s22s22p63s1 F.1s22s22p63s13p1
(2)利用电解法可在铝制品表面形成致密的氧化物保护膜,不仅可以增加美观,而且可以延长铝制品使用时间。制取氧化物保护膜的装置如下图所示,阳极的电极反应方程式为

Ⅱ.钢铁在潮湿空气中容易生锈,某兴趣小组查阅资料可知,钢铁腐蚀的快慢与温度、电解质溶液的pH值、氧气浓度以及钢铁中的含碳量有关,为此设计了下列实验。

| 编号 | ① | ② | ③ | ④ |
| A | 100 mL饱和NaCl溶液 | 100 mL饱和NaCl溶液 | 100 mLpH = 2 CH3COOH | 100 mLpH = 5 H2SO4 |
| B | m g铁粉 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 | m g铁粉和n g碳粉混合物 |
| 锥形瓶中压强随时间变化 | 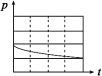 | 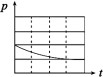 | 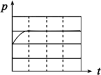 |  |
通过上述实验分析回答:
(3)上述实验①、②探究
(4)上述四个实验中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)在下图的8个装置中,属于原电池的是____________ 。
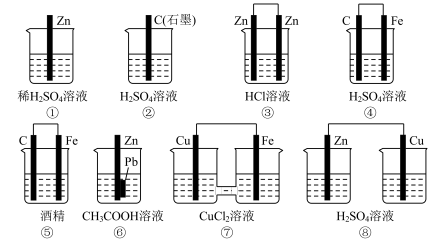
(2)依据氧化还原反应:2Ag+(aq)+Zn(s)===Zn2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
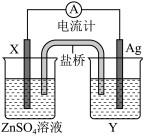
①电极X的材料是______ ;电解质溶液Y是________ ;
②银电极为电池的______ 极,发生的电极反应为__________________ ;
(3)航天飞机常采用燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。如图是甲烷燃料电池原理示意图,回答下列问题:
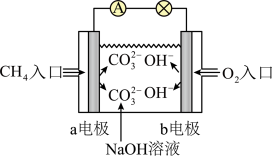
①电池的负极是____ (填“a”或“b”),该极的电极反应是____________ 。
②消耗标准状况下5.6 L O2时,有____ mol电子发生转移。
③开始放电时,正极附近溶液的pH__________ (填“增大”“减小”或“不变”)
④以铜为电极,用此电池作电源,电解以下溶液,开始阶段发生反应Cu+2H2O===Cu(OH)2+H2↑的有______________ 。
A.稀H2SO4 B.NaOH溶液 C.Na2SO4溶液
D.CuSO4溶液 E.NaCl溶液

(2)依据氧化还原反应:2Ag+(aq)+Zn(s)===Zn2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

①电极X的材料是
②银电极为电池的
(3)航天飞机常采用燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②消耗标准状况下5.6 L O2时,有
③开始放电时,正极附近溶液的pH
④以铜为电极,用此电池作电源,电解以下溶液,开始阶段发生反应Cu+2H2O===Cu(OH)2+H2↑的有
A.稀H2SO4 B.NaOH溶液 C.Na2SO4溶液
D.CuSO4溶液 E.NaCl溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铅蓄电池是重要的二次电池。已知:铅蓄电池总的化学方程式为: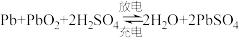 ,回答下列问题:
,回答下列问题:
(1)铅蓄电池负极材料是________ ,充电时,PbSO4在_________ (填“阳极”、“阴极”或“两个电极”)上_________ (填“生成或除去”)。
(2)铅蓄电池在充电时阳极接电源的_______ (正极/负极),放电时负极的电极反应式为__________ 。
(3)用铅蓄电池作为电源,电解饱和食盐水,电极均为惰性电极,电解饱和食盐水总反应的化学方程式为________ 。当铅蓄电池负极生成2molPbSO4时,_______ (阴极/阳极)产生_______ molH2.。
(4)电解饱和食盐水工业生产中,采用了_____ (阴/阳)离子交换膜,该交换膜的作用是_____ 。
A、避免氯气和氢氧化钠作用生成次氯酸而影响烧碱的质量
B、防止氯气和氢气混合引起爆炸
C、让氯离子从该电极通过
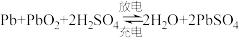 ,回答下列问题:
,回答下列问题:(1)铅蓄电池负极材料是
(2)铅蓄电池在充电时阳极接电源的
(3)用铅蓄电池作为电源,电解饱和食盐水,电极均为惰性电极,电解饱和食盐水总反应的化学方程式为
(4)电解饱和食盐水工业生产中,采用了
A、避免氯气和氢氧化钠作用生成次氯酸而影响烧碱的质量
B、防止氯气和氢气混合引起爆炸
C、让氯离子从该电极通过
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(一)铅蓄电池是典型的二次电池,电池总反应式为:Pb+PbO2+2H2SO4 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________________________ 。当外电路通过1 mol电子时,理论上负极板的质量增加______ g。
(二)某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若用HNO3(浓)作电解质溶液,电极为铜片和铝片,正极上发生的电极反应式为________________ ;
(2)若电解质溶液为0.5mol/LNaOH溶液,电极为镁片和铝片,则负极的电极反应式为____________ 。
 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是(二)某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若用HNO3(浓)作电解质溶液,电极为铜片和铝片,正极上发生的电极反应式为
(2)若电解质溶液为0.5mol/LNaOH溶液,电极为镁片和铝片,则负极的电极反应式为
您最近一年使用:0次



