原子轨道
(1)概念:量子力学把电子在原子核外的一个_______ 称为一个原子轨道。
(2)形状
①s电子的原子轨道呈_______ 形,能层序数越_______ ,原子轨道的半径越_______ 。
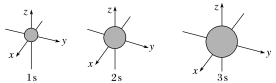
②p电子的原子轨道呈_______ 形,能层序数越_______ ,原子轨道的半径越_______ 。
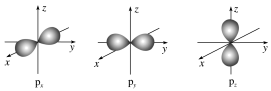
(1)概念:量子力学把电子在原子核外的一个
(2)形状
①s电子的原子轨道呈

②p电子的原子轨道呈

21-22高二下·全国·单元测试 查看更多[1]
(已下线)【知识图鉴】单元讲练测选择性必修2第1章01讲核心
更新时间:2022-12-27 15:59:56
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】浓硫酸有许多重要的性质,工业上可以通过硫铁矿(主要成分是FeS2)制取。
(1)硫原子核外电子占有______ 种能量不同的轨道。H2SO4属于______ 晶体。
(2)非金属性:S____ O(选填“>”、“<”或“=”)。试用一个实验事实说明___________________ 。
(3)接触法制硫酸工业中,其主要反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g) 2SO3(g)+190kJ该反应的平衡常数表达式是K=
2SO3(g)+190kJ该反应的平衡常数表达式是K=_____________ ,该反应450℃时的平衡常数______ 500℃时的平衡常数(选填“大于”、“小于”或“等于”)。
(4)在一个固定容积为10L的密闭容器中充入0.40mol SO2和0.20 O2,半分钟后达到平衡,测得容器中含SO3 0.36mol,则v(SO2)=____ mol· ·min
·min ;若继续通入0.40mol SO2和0.20mol O2,则平衡
;若继续通入0.40mol SO2和0.20mol O2,则平衡______ 移动(选填“向正反应方向”、“向逆反应反向”或“不”)。
(5)该热化学方程式的意义是______________________________________________ 。
(1)硫原子核外电子占有
(2)非金属性:S
(3)接触法制硫酸工业中,其主要反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g)
 2SO3(g)+190kJ该反应的平衡常数表达式是K=
2SO3(g)+190kJ该反应的平衡常数表达式是K=(4)在一个固定容积为10L的密闭容器中充入0.40mol SO2和0.20 O2,半分钟后达到平衡,测得容器中含SO3 0.36mol,则v(SO2)=
 ·min
·min ;若继续通入0.40mol SO2和0.20mol O2,则平衡
;若继续通入0.40mol SO2和0.20mol O2,则平衡(5)该热化学方程式的意义是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ ,能量最低的是_______ (填序号)。
a.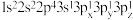 b.
b.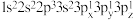
c.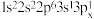 d.
d.
(3)Fe3+与Fe2+的离子半径大小关系为Fe3+_______ Fe2+(填“大于”或“小于”)
(4)下列各组多电子原子的能级能量比较不正确的是_______
①2p=3p ②4s>2s ③4p>4f ④4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
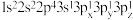 b.
b.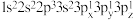
c.
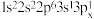 d.
d.
(3)Fe3+与Fe2+的离子半径大小关系为Fe3+
(4)下列各组多电子原子的能级能量比较不正确的是_______
①2p=3p ②4s>2s ③4p>4f ④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】第三代半导体材料的优异性能和对新兴产业的巨大推动作用,使得发达国家都把发展第三代半导体材料及其相关器件等列为半导体重要新兴技术领域,投入巨资支持发展。第三代半导体材料有氮化镓、碳化硅等。请回答下列问题:
(1)硅原子占据电子的能级符号有________________ ,其中占据电子的能量最高的能级符号为________ ,该能层已经容纳了________ 个电子。
(2)N原子中,有电子占据的最高能层符号为________ ,该能层已经容纳的电子数为______ 个。
(3)镓为元素周期表中第31号元素,位于元素周期表第四周期。镓原子具有________ 个能层,每个能层已经容纳的电子数之比为______________ 。
(1)硅原子占据电子的能级符号有
(2)N原子中,有电子占据的最高能层符号为
(3)镓为元素周期表中第31号元素,位于元素周期表第四周期。镓原子具有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求回答下列问题:
(1)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
(2)Cu2+基态核外电子排布式为___________ 。
(3)Zn原子核外电子排布式为___________ 。
(4)氮原子价层电子的轨道表达式(电子排布图)为___________ 。
(5)Fe基态原子核外电子排布式为___________ 。
(1)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为
(2)Cu2+基态核外电子排布式为
(3)Zn原子核外电子排布式为
(4)氮原子价层电子的轨道表达式(电子排布图)为
(5)Fe基态原子核外电子排布式为
您最近一年使用:0次
【推荐2】下表为元素周期表前三周期的一部分:

(1)判断 W___________ Z ___________ R ___________ (写元素符号)。
(2)X的简单氢化物分子中的化学键类型为:___________
(3)下图是X的基态原子的电子排布图,其中有一个是错误的,它不能作为基态原子的电子排布图是因为它违反了___________ 。
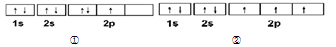
(4)以上五种元素中,___________ (填元素符号)元素第一电离能最大。___________ 元素电负性最大

(1)判断 W
(2)X的简单氢化物分子中的化学键类型为:
(3)下图是X的基态原子的电子排布图,其中有一个是错误的,它不能作为基态原子的电子排布图是因为它违反了

(4)以上五种元素中,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)某元素原子的基态电子排布式为[Ar]3d104s24p1,该元素处于元素周期表的位置______ 。
(2)Ti基态原子的电子排布式为______ ,Ti元素位于____ 区,基态Ti原子核外有_____ 种不同运动状态的电子。
(3)铝原子核外电子云有_____ 种不同的伸展方向,其基态电子有_____ 种空间运动状态。
(4)基态Fe2+与Fe3+离子中未成对的电子数之比为______ 。与H2O分子互为等电子体一种阴离子为______ (填化学式)。
(1)某元素原子的基态电子排布式为[Ar]3d104s24p1,该元素处于元素周期表的位置
(2)Ti基态原子的电子排布式为
(3)铝原子核外电子云有
(4)基态Fe2+与Fe3+离子中未成对的电子数之比为
您最近一年使用:0次



