三张有重要历史意义的周期表
(1)门捷列夫周期表:门捷列夫周期表又称_______ 周期表,重要特征是从第_______ 周期开始每个周期截成_______ 截,第_______ 族分_______ 族,第_______ 族称为过渡元素。
(2)维尔纳周期表
维尔纳周期表是_______ ,每个周期一行,各族元素、过渡金属、稀有气体、镧系和锕系,各有各的位置,同族元素_______ ,它确定了前_______ 个周期的元素种类。
(3)玻尔元素周期表
玻尔元素周期表特别重要之处是把21~28、39~46等元素用_______ 框起,这说明他已经认识到,这些框内元素的原子新增加的_______ 是填入_______ 的,他已经用原子结构解释元素周期系了,玻尔元素周期表确定了第_______ 周期为_______ 种元素。
(1)门捷列夫周期表:门捷列夫周期表又称
(2)维尔纳周期表
维尔纳周期表是
(3)玻尔元素周期表
玻尔元素周期表特别重要之处是把21~28、39~46等元素用
21-22高二下·全国·单元测试 查看更多[1]
(已下线)【知识图鉴】单元讲练测选择性必修2第1章01讲核心
更新时间:2022-12-27 15:59:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)元素p为26号元素,请写出其原子的三价阳离子的电子排布式:______________ 。
(2)e与a反应的产物的分子中中心原子的杂化形式为__________ ,该分子是__________ (填“极性”或“非极性”)分子。
(3)请写出f的氢化物在水中所存在氢键的表达式:(任写两种即可)_________________________ 。
(4)o、p两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________ ;
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

请问晶胞中i原子的配位数为________ ,一个晶胞中i原子的数目为________ 。

试回答下列问题:
(1)元素p为26号元素,请写出其原子的三价阳离子的电子排布式:
(2)e与a反应的产物的分子中中心原子的杂化形式为
(3)请写出f的氢化物在水中所存在氢键的表达式:(任写两种即可)
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

请问晶胞中i原子的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铜是人类最早发现的金属,也是人类广泛使用的一种金属。铜及其化合物在工业、工程技术和工艺上有着广泛的应用。
(1)早期发现的天然准晶颗粒由Cu、Fe、Al三种金属元素组成。Fe元素位于元素周期表的____ 区。基态Al原子的L层电子排布图为___________ 。
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到,同时可得到乙酸。乙醛中碳原子的杂化轨道类型为_________ ,1mol乙酸分子中含有的σ键的数目为____________ 。
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。一价铜离子的电子排布式为____ 。碳、硼、氮元素的电负性由大到小的顺序是_____ 。(用元素符号表示)
(4)在络离子[Cu(NH3)4]2+中NH3的VSEPR模型为_________ 。
(5)铜银合金晶体具有面心立方最密堆积结构。在晶胞中,Cu原子位于面心,Ag原子位于顶点,若该晶胞边长为r pm,则合金的密度为____ g·cm-3(设阿伏伽德罗常数的值为NA)。
(1)早期发现的天然准晶颗粒由Cu、Fe、Al三种金属元素组成。Fe元素位于元素周期表的
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到,同时可得到乙酸。乙醛中碳原子的杂化轨道类型为
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。一价铜离子的电子排布式为
(4)在络离子[Cu(NH3)4]2+中NH3的VSEPR模型为
(5)铜银合金晶体具有面心立方最密堆积结构。在晶胞中,Cu原子位于面心,Ag原子位于顶点,若该晶胞边长为r pm,则合金的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是元素周期表的一部分:

(1)写出元素①的元素符号___________ ,与①同周期的主族元素中,第一电离能比①大的有___________ 种。该周期的某种元素基态原子的核外电子排布式为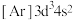 ,则该元素在元素周期表中的位置为
,则该元素在元素周期表中的位置为___________ 。
(2)基态锑(Sb)原子的价电子排布式为___________ 。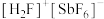 (氟酸锑)是一种超强酸,
(氟酸锑)是一种超强酸, 离子的空间构型为
离子的空间构型为___________ ,写出一种与 互为等电子体的分子
互为等电子体的分子___________ 。
(3)处于分界线的元素Al可形成多种化合物。
 中三种元素的基态原子的第一电离能从大到小的顺序是
中三种元素的基态原子的第一电离能从大到小的顺序是___________ (填元素符号)。
 中铝的杂化方式为
中铝的杂化方式为___________ ,其中阴离子的立体结构为___________ ,
(4)下列说法正确的是___________
a. 、SiC,
、SiC, 是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiC
是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiC
b.基态P原子中,电子占据的最高能级符号为M
c.Sb位于p区
d.升温实现液氨→氨气→氮气和氢气变化的阶段中,微粒间破坏的主要的作用力依次是氢键、极性共价键
(5)周期表中元素的性质呈现出周期性变化。元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示,其中除氮元素外,其他元素的
变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大的原因是
自左而右依次增大的原因是___________ ;氮元素的 呈现异常的原因是
呈现异常的原因是___________ 。


(1)写出元素①的元素符号
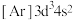 ,则该元素在元素周期表中的位置为
,则该元素在元素周期表中的位置为(2)基态锑(Sb)原子的价电子排布式为
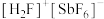 (氟酸锑)是一种超强酸,
(氟酸锑)是一种超强酸, 离子的空间构型为
离子的空间构型为 互为等电子体的分子
互为等电子体的分子(3)处于分界线的元素Al可形成多种化合物。
 中三种元素的基态原子的第一电离能从大到小的顺序是
中三种元素的基态原子的第一电离能从大到小的顺序是 中铝的杂化方式为
中铝的杂化方式为(4)下列说法正确的是
a.
 、SiC,
、SiC, 是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiC
是空间构型均为正四面体的三种物质,键角与其他两种物质不同的是SiCb.基态P原子中,电子占据的最高能级符号为M
c.Sb位于p区
d.升温实现液氨→氨气→氮气和氢气变化的阶段中,微粒间破坏的主要的作用力依次是氢键、极性共价键
(5)周期表中元素的性质呈现出周期性变化。元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示,其中除氮元素外,其他元素的
变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大的原因是
自左而右依次增大的原因是 呈现异常的原因是
呈现异常的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素在周期表中的位置,反映了元素的原子结构和性质。如图是元素周期表的一部分,请按照要求回答下列问题:
(1)①的元素符号是______ ,元素②位于周期表中的第______ 周期第______ 族。
(2)②、③两种元素中,非金属性较强的是______ (填元素符号)
(3)①、②、④三种元素中,原子半径最大的是______ (填元素符号)。
(4)④、⑤两种元素中最高价氧化物对应的水化物,属于两性氢氧化物的是______ (填化学式)。
(5)常温下,将元素⑥的单质通入 溶液中可制得漂白液,其有效成分是
溶液中可制得漂白液,其有效成分是 ,请写出该反应的离子方程式
,请写出该反应的离子方程式______
| 族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | |||||
(2)②、③两种元素中,非金属性较强的是
(3)①、②、④三种元素中,原子半径最大的是
(4)④、⑤两种元素中最高价氧化物对应的水化物,属于两性氢氧化物的是
(5)常温下,将元素⑥的单质通入
 溶液中可制得漂白液,其有效成分是
溶液中可制得漂白液,其有效成分是 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是____ ,只有负价而无正价的是______ ,还原性最强的单质是______ ,氧化性最强的单质是___ 。
(2)最高价氧化物的水化物中,既能和盐酸又能和氢氧化钠反应的是___ ,酸性最强的是____ ,碱性最强的是_____ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的_____ 。
(4)在A、B、C、D、E、F、G、H中,原子半径最大的是______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | F | H | I |
(2)最高价氧化物的水化物中,既能和盐酸又能和氢氧化钠反应的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在A、B、C、D、E、F、G、H中,原子半径最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】判断
1.24g镁原子的最外层电子数为NA。(_______)
2.由于晶体硅熔点高、硬度大,故可用于制作半导体材料。(_______)
3.过滤时,漏斗下端紧贴烧杯内壁。(_______)
4.在冶金工业的烟道废气中,常混有大量的SO2和CO,它们都是大气的污染物,在773K和催化剂(铝矾土)的作用下,使二者反应可收回大量的硫磺.请写出该反应的化学方程式:SO2+2CO═2CO2+S.请判断该反应式写的是否正确。(_______)
5.1.00molNaCl中,所有Na+的最外层电子总数为8×6.02×1023。(_______)
6.蛋白质的盐析过程是一个可逆过程,据此可以分离和提纯蛋白质。(_______)
7.1mol甲苯中有6molC﹣H共价键。(_______)
8.现行的元素周期表共18个纵行,18个族,七个周期。(_______)
9.金属阳离子一定只具有氧化性。(_______)
10.向试管中滴加液体时,胶头滴管紧贴试管内壁。(_______)
1.24g镁原子的最外层电子数为NA。(_______)
2.由于晶体硅熔点高、硬度大,故可用于制作半导体材料。(_______)
3.过滤时,漏斗下端紧贴烧杯内壁。(_______)
4.在冶金工业的烟道废气中,常混有大量的SO2和CO,它们都是大气的污染物,在773K和催化剂(铝矾土)的作用下,使二者反应可收回大量的硫磺.请写出该反应的化学方程式:SO2+2CO═2CO2+S.请判断该反应式写的是否正确。(_______)
5.1.00molNaCl中,所有Na+的最外层电子总数为8×6.02×1023。(_______)
6.蛋白质的盐析过程是一个可逆过程,据此可以分离和提纯蛋白质。(_______)
7.1mol甲苯中有6molC﹣H共价键。(_______)
8.现行的元素周期表共18个纵行,18个族,七个周期。(_______)
9.金属阳离子一定只具有氧化性。(_______)
10.向试管中滴加液体时,胶头滴管紧贴试管内壁。(_______)
您最近一年使用:0次



