下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是____ ,只有负价而无正价的是______ ,还原性最强的单质是______ ,氧化性最强的单质是___ 。
(2)最高价氧化物的水化物中,既能和盐酸又能和氢氧化钠反应的是___ ,酸性最强的是____ ,碱性最强的是_____ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的_____ 。
(4)在A、B、C、D、E、F、G、H中,原子半径最大的是______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | F | H | I |
(2)最高价氧化物的水化物中,既能和盐酸又能和氢氧化钠反应的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在A、B、C、D、E、F、G、H中,原子半径最大的是
更新时间:2019-04-21 10:29:34
|
相似题推荐
【推荐1】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
(1)上述元素属于第三周期,且可以做半导体材料的是_______ (填字母代号)。
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ·mol-1):
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_______ 。
②表中Y可能为以上13种元素中的_______ (填写字母)元素。用元素符号表示X和l形成化合物的电子式是_______ 。
(3)以上13种元素中,_______ (填写字母)元素原子失去核外第一个电子需要的能量最多。
(4)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中元素c位于_______ 区。
| b | |||||||||||||||||||
| h | j | ||||||||||||||||||
| a | c | f | i | l | m | ||||||||||||||
| e | g | ||||||||||||||||||
| d | k | ||||||||||||||||||
(1)上述元素属于第三周期,且可以做半导体材料的是
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ·mol-1):
| 锂 | X | Y | |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量
②表中Y可能为以上13种元素中的
(3)以上13种元素中,
(4)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中元素c位于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分。请按要求回答下列问题:
(1)氧元素在周期表中的位置是___________ ,⑦的最高价氧化物对应水化物的化学式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(3)写出由上述所列元素形成的18电子的双原子分子的化学式___________ 。
(4)已知X为第四周期第IIIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIA族元素,写出Y的原子序数b=___________ (用含a的代数式表示)。
(5)下列说法不正确的是___________。
(6)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | ⑧ | ||||||
(2)上述所列元素最高价氧化物对应水化物碱性最强的是
(3)写出由上述所列元素形成的18电子的双原子分子的化学式
(4)已知X为第四周期第IIIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIA族元素,写出Y的原子序数b=
(5)下列说法不正确的是___________。
| A.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| B.元素最高正价与最低负价绝对值相等的元素一定处于第IVA族 |
| C.第5周期第VIIA族元素的原子序数为53 |
| D.周期表中当某元素的周期序数大于其主族序数时,该元素可能属于金属或非金属 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
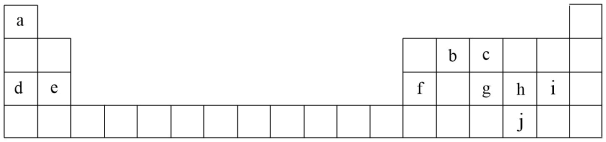
(1)元素c代表的元素是(写元素符号)_______
(2)请写出元素e在元素周期表中所在的位置_______
(3)请画出元素f的简单离子结构示意图_______ 。请写出单质f与d的最高价氧化物对应水化物的离子反应方程式_______ 。
(4)元素a和b能构成最简单的有机化合物(用结构式表示)_______ 。请写出元素a和b构成的最简单有机化合物与i单质发生的第一步化学反应方程式_______ 。
(5)元素h的最高价氧化物对应的水化物呈_______ (酸性、中性或碱性);请写出元素h的最高价氧化物对应的水化物与单质b的化学反应方程式_______ 。

(1)元素c代表的元素是(写元素符号)
(2)请写出元素e在元素周期表中所在的位置
(3)请画出元素f的简单离子结构示意图
(4)元素a和b能构成最简单的有机化合物(用结构式表示)
(5)元素h的最高价氧化物对应的水化物呈
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素是组成我们生活的世界中一切物质的“原材料”。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是___________ 。
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:
(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5。其余元素的信息如图所示:
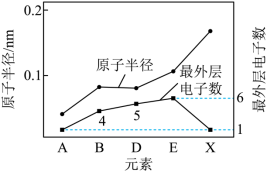
①E在周期表中的位置是___________ 。
②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是___________ 。
③用电子式表示化合物XZ的形成过程是:___________ 。
④X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为___________ 。
⑤下列可以判断X和Y元素原子失电子能力强弱的是___________ (填字母序号)。
a.单质的熔点X比Y低
b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少
d.最高价氧化物的水化物的碱性X比Y强
⑥E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:___________ 。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:

(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5。其余元素的信息如图所示:

①E在周期表中的位置是
②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是
③用电子式表示化合物XZ的形成过程是:
④X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为
⑤下列可以判断X和Y元素原子失电子能力强弱的是
a.单质的熔点X比Y低
b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少
d.最高价氧化物的水化物的碱性X比Y强
⑥E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4)反应的产物,以其产物为原料制备氯气:室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。分析实验并回答相应问题。
(1)M的化学式是_____ ,组成草酸的三种元素中,非金属性最强的是_____ (填元素符号)。
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为_____ ,向滤液中加入盐酸时又产生无色无味气体,该反应的离子方程式为______ 。
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是_____ 。
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为_____ 。
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:______ 。
(1)M的化学式是
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了A~R9种元素在周期表中的位置:
请回答下列问题。
(1)这9种元素中化学性质最不活泼的是___________ (用元素符号表示)。
(2)画出G的原子结构示意图___________ 。
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的化学方程式是___________ ;
(4)A、B、C三种元素按原子半径由大到小的顺序排列为___________ (用元素符号表示);
(5)F元素氢化物的电子式是___________ ,该氢化物在常温下跟A发生反应的化学方程式是___________ 。
(6)H元素与A元素形成的化合物高温灼烧时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | GG | R | |||
| 4 | B | H | ||||||
请回答下列问题。
(1)这9种元素中化学性质最不活泼的是
(2)画出G的原子结构示意图
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的化学方程式是
(4)A、B、C三种元素按原子半径由大到小的顺序排列为
(5)F元素氢化物的电子式是
(6)H元素与A元素形成的化合物高温灼烧时,火焰呈
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①〜⑩种元素,填写下列空白(涉及具体元素对应化学符号表示):
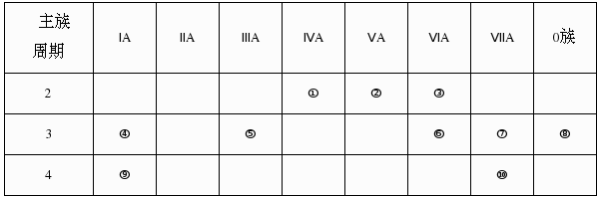
(1)在这些元素中,化学性质最不活泼的是_______ (填元素符号)元素⑩在周期表中的位置______ 。形成化合物最多的元素______ (填序号)
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的电子式是:______ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:_________________ .
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是________ 。
(5)元素③的氢化物的结构式为_____ ;该氢化物在一定条件下可以生成另一种③的氢化物和③的单质。

(1)在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(5)元素③的氢化物的结构式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下图中的曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质):
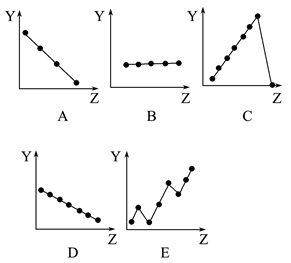
把与元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素原子的价电子数___________ ;
(2)第三周期元素的最高正化合价___________ ;
(3)F-、Na+、Mg2+、Al3+四种离子的离子半径___________ ;
(4)第二周期元素的原子半径(不包括稀有气体)___________ ;
(5)第二周期元素的第一电离能___________ 。

把与元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素原子的价电子数
(2)第三周期元素的最高正化合价
(3)F-、Na+、Mg2+、Al3+四种离子的离子半径
(4)第二周期元素的原子半径(不包括稀有气体)
(5)第二周期元素的第一电离能
您最近一年使用:0次



