下图中的曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质):
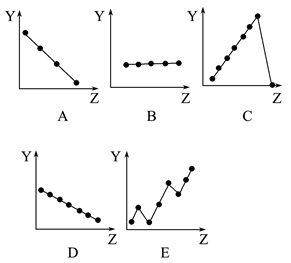
把与元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素原子的价电子数___________ ;
(2)第三周期元素的最高正化合价___________ ;
(3)F-、Na+、Mg2+、Al3+四种离子的离子半径___________ ;
(4)第二周期元素的原子半径(不包括稀有气体)___________ ;
(5)第二周期元素的第一电离能___________ 。

把与元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素原子的价电子数
(2)第三周期元素的最高正化合价
(3)F-、Na+、Mg2+、Al3+四种离子的离子半径
(4)第二周期元素的原子半径(不包括稀有气体)
(5)第二周期元素的第一电离能
更新时间:2018-02-10 13:56:58
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)下面是 4 种粒子的结构示意图:
A.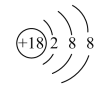 B.
B.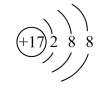 C.
C.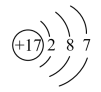 D.
D. 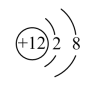
图中粒子共能表示________ 种元素,
图中表示的阳离子是________ (用离子符号表示),
图中B 所表示的元素在元素周期表中的位置________ 。
(2)在 1﹣18 号的短周期主族元素中,图中的字母代表一种元素,回答下列问题:
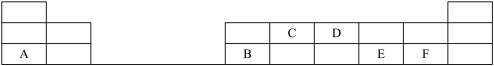
①写出 D 气态氢化物的电子式________ ;
②写出 C 的最高价氧化物的结构式________ ;
③E 和 F 分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_________ ;
④A 最高价氧化物的水化物所含化学键为____ ,其水溶液与 B 反应的离子方程式为________ ;
(3) X、Y、Z、M、N、Q 皆为短周期主族元素,其原子半径与主要化合价的关系如图所示。下列说法正确的是______

A.金属性:N>Q
B.简单离子半径:Q>N>X
C.最高价氧化物对应水化物的酸性:M>Y>N
D.原子序数:Z>M>X>Y
A.
 B.
B. C.
C. D.
D. 
图中粒子共能表示
图中表示的阳离子是
图中B 所表示的元素在元素周期表中的位置
(2)在 1﹣18 号的短周期主族元素中,图中的字母代表一种元素,回答下列问题:

①写出 D 气态氢化物的电子式
②写出 C 的最高价氧化物的结构式
③E 和 F 分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)
④A 最高价氧化物的水化物所含化学键为
(3) X、Y、Z、M、N、Q 皆为短周期主族元素,其原子半径与主要化合价的关系如图所示。下列说法正确的是

A.金属性:N>Q
B.简单离子半径:Q>N>X
C.最高价氧化物对应水化物的酸性:M>Y>N
D.原子序数:Z>M>X>Y
您最近半年使用:0次
【推荐2】按要求回答下列问题:
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
A通常显___________ 价,B的基态原子核外电子排布式为___________ 。
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:___________ (填元素符号)。
②同主族内不同元素的X值变化的特点是___________ ;同周期内,随着原子序数的增大,X值的变化总趋势是___________ 。周期表中X值的这种变化特点体现了元素性质的___________ 变化规律。
③X值较小的元素集中在元素周期表的___________ (填字母)。
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是___________ (填字母)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
电离能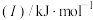 |  | 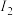 | 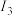 | 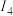 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:
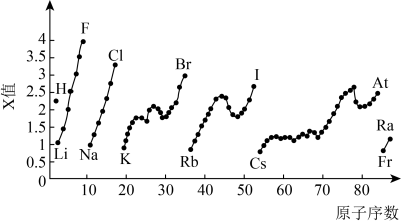
②同主族内不同元素的X值变化的特点是
③X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。
(1)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗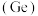 。加上之前发现的碳
。加上之前发现的碳 铅
铅 、锡
、锡 ,这一族的元素趋于完善。已知常温下锡、锗在空气中不反应而铅表面生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
,这一族的元素趋于完善。已知常温下锡、锗在空气中不反应而铅表面生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为_______ ;根据锗在周期表中处于金属和非金属分界线附近,预测锗单质的一种用途是_______ 。
②硅和锗单质分别与 反应时,反应较难进行的是
反应时,反应较难进行的是_______ (填“硅”或“锗”)。
(2)又已知锡、铅两种元素的主要化合价是 价和
价和 价,其中
价,其中 价锡元素和
价锡元素和 价铅元素的化合物均是不稳定的,
价铅元素的化合物均是不稳定的, 价锡元素有强还原性,
价锡元素有强还原性, 价铅元素的化合物有强氧化性,
价铅元素的化合物有强氧化性, 还原性比
还原性比 还原性强。根据以上叙述,写出下列反应的化学方程式:
还原性强。根据以上叙述,写出下列反应的化学方程式:
①氯气与锡共热_______ ;
②能说明 还原性比
还原性比 还原性强的离子方程式为
还原性强的离子方程式为_______ 。
(3)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓 。
。
①由镓的性质推知,镓与铝同主族,冶炼金属镓通常采用的方法是_______ 。
②已知 难溶于水,为判断
难溶于水,为判断 是否为两性氢氧化物,设计实验时,需要选用的试剂有
是否为两性氢氧化物,设计实验时,需要选用的试剂有 溶液、
溶液、_______ 和_______ 。
(1)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗
 。加上之前发现的碳
。加上之前发现的碳 铅
铅 、锡
、锡 ,这一族的元素趋于完善。已知常温下锡、锗在空气中不反应而铅表面生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
,这一族的元素趋于完善。已知常温下锡、锗在空气中不反应而铅表面生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:①锗的原子序数为
②硅和锗单质分别与
 反应时,反应较难进行的是
反应时,反应较难进行的是(2)又已知锡、铅两种元素的主要化合价是
 价和
价和 价,其中
价,其中 价锡元素和
价锡元素和 价铅元素的化合物均是不稳定的,
价铅元素的化合物均是不稳定的, 价锡元素有强还原性,
价锡元素有强还原性, 价铅元素的化合物有强氧化性,
价铅元素的化合物有强氧化性, 还原性比
还原性比 还原性强。根据以上叙述,写出下列反应的化学方程式:
还原性强。根据以上叙述,写出下列反应的化学方程式:①氯气与锡共热
②能说明
 还原性比
还原性比 还原性强的离子方程式为
还原性强的离子方程式为(3)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓
 。
。①由镓的性质推知,镓与铝同主族,冶炼金属镓通常采用的方法是
②已知
 难溶于水,为判断
难溶于水,为判断 是否为两性氢氧化物,设计实验时,需要选用的试剂有
是否为两性氢氧化物,设计实验时,需要选用的试剂有 溶液、
溶液、
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】参考下表中物质的熔点回答有关问题:
(1)上述物质中,可能属于分子晶体的是____________ ;
(2)卤离子的半径大小顺序是_________ ;
(3)上述金属卤化钠随着___________ 的增大,熔点依次降低;
(4)根据(3)中得出的结论和有关数据,判断Rb+的半径____________ Cs+的半径。(填“大于”或“小于”)。
| 物质 | NaF | NaCl | NaBr | NaI | KCl | RbCl | CsCl | SiCl4 |
| 熔点(℃) | 995 | 801 | 755 | 651 | 775 | 715 | 646 | -70.4 |
(1)上述物质中,可能属于分子晶体的是
(2)卤离子的半径大小顺序是
(3)上述金属卤化钠随着
(4)根据(3)中得出的结论和有关数据,判断Rb+的半径
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】卤族元素在性质上具有相似性与递变性。为了验证卤族部分元素递变规律,设计如图装置进行实验。请回答下列问题。
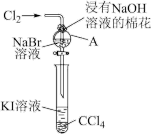
(1)A中发生反应的化学方程式是_______ 。
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是_______ 。
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应_______  填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为_______ 。
(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱_______ 。
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为_______ 。
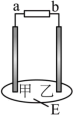
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是
(8)下图是用强光照射广口瓶中新制氯水时传感器所获得数据的图像,下列各项代表纵坐标的物理量,其中与图像不相符的是

(9)下列变化不需要破坏化学键的是

(1)A中发生反应的化学方程式是
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
| A.Cl-、Br-、I-的还原性逐渐增强 | B.Cl2、Br2、I2的熔点逐渐升高 |
| C.HCl、HBr、HI的酸性逐渐减弱 | D.HCl、HBr、HI的稳定性逐渐减弱 |
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应
 填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是

| A.b是阳极,a是阴极 | B.a是正极,b是负极 |
| C.乙是正极,甲是负极 | D.乙是阳极,甲是阴极 |

| A.溶液中氯离子的浓度 | B.溶液的 pH |
| C.瓶中氧气的体积分数 | D.溶液的导电能力 |
| A.液态水变为水蒸气 | B.HCl 气体溶于水 |
| C.NaHCO3 受热分解 | D.NaCl 熔化 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y.W原子的最外层没有p电子,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子中p电子数比Y原子多2个.
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:__________________ .
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为__________ (用分子式表示).
(3)四种元素原子半径的由大到小为_________ (填元素符号).
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为
(3)四种元素原子半径的由大到小为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素单质及其化合物有广泛用途,请根据周期表中第3周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是___________ 。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为___________ ,氧化性最弱的简单阳离子是___________ 。
(3)已知:
工业制镁时,电解MgCl2而不电解MgO的原因是___________ ;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是___________ 。
a.NH3 b.HI c.SO2 d.CO2
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列曲线表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的性质);

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数( )
(2)ⅦA族元素氢化物的沸点( )
(3)第三周期元素单质的熔点( )
(4)第三周期元素的最高正化合价( )
(5)IA族元素单质熔点( )
(6)F-、 Na+、Mg2+、 Al3+四种离子的离子半径( )
(7)某短周期元素的原子半径( )
(8)某短周期元素的第一电离能( )
(9)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量。从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推,现有5种元素,A、B、 C、 D、 E,其I1~I3分别如下表,根据表中数据判断其中最有可能是稀有气体元素的是____ ,最活泼的金属元素是_____ 。

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数
(2)ⅦA族元素氢化物的沸点
(3)第三周期元素单质的熔点
(4)第三周期元素的最高正化合价
(5)IA族元素单质熔点
(6)F-、 Na+、Mg2+、 Al3+四种离子的离子半径
(7)某短周期元素的原子半径
(8)某短周期元素的第一电离能
(9)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量。从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推,现有5种元素,A、B、 C、 D、 E,其I1~I3分别如下表,根据表中数据判断其中最有可能是稀有气体元素的是
| 元 素 | I1/eV | I2/eV | I3/eV |
| A | 13.0 | 23.9 | 40.0 |
| B | 4.3 | 31.9 | 47.8 |
| C | 5.7 | 47.4 | 71.8 |
| D | 7.7 | 15.1 | 80.3 |
| E | 21.6 | 41.1 | 65.2 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】能源、材料已成为当今科学研究的热点。请回答下列问题:
(1)单质A的燃烧热大,可作燃料。已知A为短周期元素,其气态原子逐个失去1~4个电子所需能量(电离能)如表所示。若该原子核外电子有三层,则该元素位于周期表______ 族,写出A燃烧后形成的氧化物的电子式:______ .
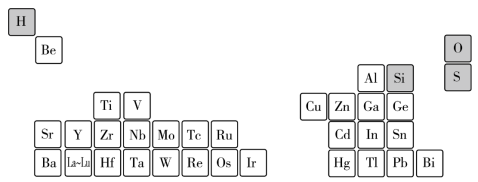
(2)如图是超导材料元素在周期表中的分布,上述元素的短周期元素中原子半径最大的是______ (填元素符号),其原子最外层有______ 种运动状态不同的电子,写出其最高价氧化物对应水化物在水溶液中的电离方程式:______ 。
(3)上述主族元素中有两种原子可以形成的五核分子,其化学键键长和键角都相等,则该分子的空间构型为______ ,该物质为______ 分子(选填“极性”或“非极性”)。
(4)铁单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,且每生成1mol该易燃气体放出37.68kJ热量,请写出此反应的热化学方程式:______ 。
(5)取适量Al、Mg合金样品置于烧杯中,加入20mL 1mol/L的NaOH溶液,恰好完全反应。下列叙述正确的是______ (选填编号)。
a.Mg作负极,Al作正极
b.若加入的是20mL 1mol/L的盐酸,则放出的氢气的物质的量减少2/3
c.若把NaOH中的H换成D(D为重氢),生成的氢气中D与H物质的量之比为1:2。
(1)单质A的燃烧热大,可作燃料。已知A为短周期元素,其气态原子逐个失去1~4个电子所需能量(电离能)如表所示。若该原子核外电子有三层,则该元素位于周期表
| I1 | I2 | I3 | I4 | … | |
| 电离能(kJ/mol) | 738 | 1451 | 7733 | 10540 | … |
(2)如图是超导材料元素在周期表中的分布,上述元素的短周期元素中原子半径最大的是

(3)上述主族元素中有两种原子可以形成的五核分子,其化学键键长和键角都相等,则该分子的空间构型为
(4)铁单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,且每生成1mol该易燃气体放出37.68kJ热量,请写出此反应的热化学方程式:
(5)取适量Al、Mg合金样品置于烧杯中,加入20mL 1mol/L的NaOH溶液,恰好完全反应。下列叙述正确的是
a.Mg作负极,Al作正极
b.若加入的是20mL 1mol/L的盐酸,则放出的氢气的物质的量减少2/3
c.若把NaOH中的H换成D(D为重氢),生成的氢气中D与H物质的量之比为1:2。
您最近半年使用:0次
【推荐2】如图是元素周期表前五周期的一部分,X、Y、Z、R、W、J是其中的6种元素。
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1)基态R原子的核外电子排布的轨道表示式为__ 。
(2)在化合物YZ2中Y的化合价为__ ;Y2-与Na+的半径大小为__ 。
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是__ ;第一电离能:X__ Y(填“<“>或“=”),其理由是__ 。
(4)以上6种元素组成的双原子分子中,最稳定单质的电子式为__ ;HX3溶液的酸性与醋酸相近,HX3溶液与NaOH溶液反应的离子方程式为__ 。
X | Y | Z | |
R | |||
W | |||
J |
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1)基态R原子的核外电子排布的轨道表示式为
(2)在化合物YZ2中Y的化合价为
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是
(4)以上6种元素组成的双原子分子中,最稳定单质的电子式为
您最近半年使用:0次
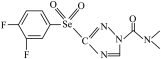
【推荐3】科技的发展为新能源开发和新材料研制开拓出更大的空间。中科院科学家最近合成了一种新型材料,其结构简式为:___________ 种空间伸展方向;基态硒原子的价层电子排布式是___________ ;氟、氧、氮三种元素的第一电离能由大到小的顺序___________ (用元素符号表示)。
(2)该分子中含有氮、氧、氟三种电负性很大的原子,也含有氢原子,它___________ (填“能”或“不能”)形成分子内或者分子间氢键,其原因是___________ 。
(3)硒能形成两种常见的氧化物,分子式为___________ 。
(4)常压下,氨气在300℃时约有10%分解,水蒸气在2000℃时约有5%分解,从物质结构的角度看,其原因是___________ 。
(2)该分子中含有氮、氧、氟三种电负性很大的原子,也含有氢原子,它
(3)硒能形成两种常见的氧化物,分子式为
(4)常压下,氨气在300℃时约有10%分解,水蒸气在2000℃时约有5%分解,从物质结构的角度看,其原因是
您最近半年使用:0次



