下表是元素周期表的一部分。请按要求回答下列问题:
(1)氧元素在周期表中的位置是___________ ,⑦的最高价氧化物对应水化物的化学式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(3)写出由上述所列元素形成的18电子的双原子分子的化学式___________ 。
(4)已知X为第四周期第IIIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIA族元素,写出Y的原子序数b=___________ (用含a的代数式表示)。
(5)下列说法不正确的是___________。
(6)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | ⑧ | ||||||
(2)上述所列元素最高价氧化物对应水化物碱性最强的是
(3)写出由上述所列元素形成的18电子的双原子分子的化学式
(4)已知X为第四周期第IIIA族元素,其原子序数为a,Y与X位于同一周期,且为第IIA族元素,写出Y的原子序数b=
(5)下列说法不正确的是___________。
| A.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| B.元素最高正价与最低负价绝对值相等的元素一定处于第IVA族 |
| C.第5周期第VIIA族元素的原子序数为53 |
| D.周期表中当某元素的周期序数大于其主族序数时,该元素可能属于金属或非金属 |
更新时间:2024-04-03 22:42:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表是学习化学的重要工具,它隐含许多信息和规律。
(1)请在图中用实线补全元素周期表的边界_________________________
(2)写出c在周期表中对应的位置________ ,并画出其原子结构示意图___________ 。
(3)相同大小的a、b两种元素的单质分别投入水中,反应较剧烈的是_______ (用化学式表示,下同),其与水反应的化学方程式为_________ 。
(4)比较d元素和e元素原子半径的大小_________ (用“>”连接)。
| He | |||||||||||||||||
| d | e | ||||||||||||||||
| a | c | ||||||||||||||||
| b | |||||||||||||||||
(1)请在图中用实线补全元素周期表的边界
(2)写出c在周期表中对应的位置
(3)相同大小的a、b两种元素的单质分别投入水中,反应较剧烈的是
(4)比较d元素和e元素原子半径的大小
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表是化学学习的重要工具。根据所学知识完成下列问题。
(1)元素周期表中,第三周期原子半径最大的金属元素是___________ (填写元素符号),元素的最高价氧化物对应的水化物中酸性最强是___________ (填写化学式)。
(2)在下列变化中,化学键没有破坏的是____________ (填写序号,下同),仅发生离子键破坏的是___________ ,仅发生共价键破坏的是_________ ,既发生共价键破坏又发生离子键破坏的是_________ 。
①I2的升华 ②烧碱熔化 ③NaCl溶于水 ④HCl溶于水 ⑤O2溶于水 ⑥Na2O2溶于水
(1)元素周期表中,第三周期原子半径最大的金属元素是
(2)在下列变化中,化学键没有破坏的是
①I2的升华 ②烧碱熔化 ③NaCl溶于水 ④HCl溶于水 ⑤O2溶于水 ⑥Na2O2溶于水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,回答下列问题:
(1)写出元素符号:②________ ,⑦_______ 。
(2)①的原子结构示意图为_________ ,⑤的离子结构示意图为________ 。
(3)元素⑨的最高价氧化物对应的水化物的电子式为________ 。
(4)元素④、⑧、⑩的氢化物的沸点由高到低的顺序为_________ (填化学式)。
(5)写出元素③和⑥形成的化合物与元素⑤的最高价氧化物对应的水化物反应的化学方程式_____________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 四 | ⑨ | ⑩ |
(1)写出元素符号:②
(2)①的原子结构示意图为
(3)元素⑨的最高价氧化物对应的水化物的电子式为
(4)元素④、⑧、⑩的氢化物的沸点由高到低的顺序为
(5)写出元素③和⑥形成的化合物与元素⑤的最高价氧化物对应的水化物反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如下。

已知:H3PO4能电离出PO43-。
(1)Li在元素周期表中的位置是________ 。
(2)LiFePO4中,铁元素的化合价为________ 价。
(3)将反应Ⅰ补充完整:____Fe2+ + 2H+ + ____H2O2 =____Fe3+ + 2H2O 。____
(4)反应Ⅲ的化学方程式是_________ 。

已知:H3PO4能电离出PO43-。
(1)Li在元素周期表中的位置是
(2)LiFePO4中,铁元素的化合价为
(3)将反应Ⅰ补充完整:____Fe2+ + 2H+ + ____H2O2 =____Fe3+ + 2H2O 。
(4)反应Ⅲ的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
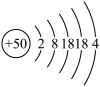
【推荐2】锡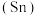 是很早便被发现和使用的金属。其原子结构示意图如下。已知
是很早便被发现和使用的金属。其原子结构示意图如下。已知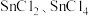 均易水解,且
均易水解,且 易被氧化。
易被氧化。
完成下列填空:
(1)锡为主族元素,在元素周期表中的位置是__________ 。有一种锡的单质具有金刚石型结构,则该单质内存在的化学键是_________________ 。
(2)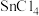 分子的空间构型为
分子的空间构型为____ ,归纳表中四卤化锡的熔、沸点的变化规律并解释原因___________ 。
(3) 能与
能与 反应生成钠盐,写出反应的化学方程式
反应生成钠盐,写出反应的化学方程式__________________________________ 。
(4)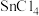 是无色液体,放入大量水中并加热,生成
是无色液体,放入大量水中并加热,生成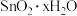 ,写出该过程的化学方程式
,写出该过程的化学方程式______ 。
(5)配置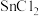 溶液需要先将
溶液需要先将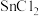 溶解于
溶解于__________ 中再稀释,最后需加入少量的________ 。
(6)马口铁是在铁表面镀一层锡。一个马口铁罐装的桔子罐头发生了“涨罐”和马口铁罐穿孔的现象。经检测罐头内食物没有腐败,则罐头内导致“涨罐”的气体可能是__________ ,说明理由___________ 。
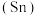 是很早便被发现和使用的金属。其原子结构示意图如下。已知
是很早便被发现和使用的金属。其原子结构示意图如下。已知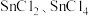 均易水解,且
均易水解,且 易被氧化。
易被氧化。
完成下列填空:
(1)锡为主族元素,在元素周期表中的位置是
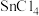 |  | 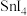 | |
熔点/ | -33 | 31 | 144.5 |
沸点/ | 114.1 | 202 | 364 |
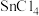 分子的空间构型为
分子的空间构型为(3)
 能与
能与 反应生成钠盐,写出反应的化学方程式
反应生成钠盐,写出反应的化学方程式(4)
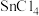 是无色液体,放入大量水中并加热,生成
是无色液体,放入大量水中并加热,生成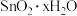 ,写出该过程的化学方程式
,写出该过程的化学方程式(5)配置
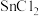 溶液需要先将
溶液需要先将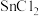 溶解于
溶解于(6)马口铁是在铁表面镀一层锡。一个马口铁罐装的桔子罐头发生了“涨罐”和马口铁罐穿孔的现象。经检测罐头内食物没有腐败,则罐头内导致“涨罐”的气体可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下面是元素周期表的一-部分,参照元素①~⑧在表中的位置,请用化学用语回答下列问题:
(1)②⑦⑧的最高价含氧酸的酸任由强到弱的顺序是(填化学式)___ 。
(2)在①④⑤⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:___ 。
(3)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:__ 。
(4)②的简单气态氢化物与氧气组成燃料电池,用氢氧化钠做电解质溶液,写出其负极的电极反应式:___ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)②⑦⑧的最高价含氧酸的酸任由强到弱的顺序是(填化学式)
(2)在①④⑤⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(3)由②和④组成的化合物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(4)②的简单气态氢化物与氧气组成燃料电池,用氢氧化钠做电解质溶液,写出其负极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。

(1)④是___________ (用元素符号表示)。
(2)①、③、④元素中的两种元素可形成含10个电子的分子,请写出其中一种10个电子的分子的化学式___________ 。
(3)画出⑤的原子结构示意图:___________ 。
(4)⑧的单质与氢氧化钠溶液反应的离子方程式为___________ 。
Ⅱ.据《中国质量报》报道,我国首次将星载铷(Rb)钟应用于海洋二号卫星,已知 (铷)的原子序数为37。回答下列有关铷的问题:
(铷)的原子序数为37。回答下列有关铷的问题:
(1) Rb在元素周期表中的位置是___________ 。
(2)取少量铷单质加入水中,发生反应的离子方程式___________ 。

(1)④是
(2)①、③、④元素中的两种元素可形成含10个电子的分子,请写出其中一种10个电子的分子的化学式
(3)画出⑤的原子结构示意图:
(4)⑧的单质与氢氧化钠溶液反应的离子方程式为
Ⅱ.据《中国质量报》报道,我国首次将星载铷(Rb)钟应用于海洋二号卫星,已知
 (铷)的原子序数为37。回答下列有关铷的问题:
(铷)的原子序数为37。回答下列有关铷的问题:(1) Rb在元素周期表中的位置是
(2)取少量铷单质加入水中,发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。元素周期表与元素周期律在化学学习研究中有很重要的作用。
(1)下表是元素周期表的一部分
i.元素④的过氧化物的电子式为______ ,其最高价氧化物对应的水化物含有的化学键类型为______ ,⑩元素最高价氧化物对应的水化物的化学式是______ 。
ii.元素①、②、③的简单氢化物的稳定性最强的是______ (用化学式表示,下同),②、⑧简单氢化物熔点高的是______ ,④、⑤最高价氧化物的水化物碱性更强的是______ ,④、⑤、⑧、⑨的简单离子半径由大到小的顺序______ 。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置______ 。
ii.关于铷的下列说法中不正确的是______ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(1)下表是元素周期表的一部分
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
i.元素④的过氧化物的电子式为
ii.元素①、②、③的简单氢化物的稳定性最强的是
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置
ii.关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如表是元素周期表的一部分,回答下列有关问题。
(1)写出下列元素符号:①___________
(2)画出原子的结构示意图:④___________
(3)在①—⑫元素中,金属性最强的元素是___________ ,非金属性最强的元素是___________ ,最不活泼的元素是___________ 。(均填元素符号)
(4)第三周期中原子半径最大的元素是___________ (填序号),跟它同周期原子半径最小的元素是___________ (填序号),它们可以形成___________ (填“离子”或“共价”)化合物,用电子式表示其形成过程如下:___________ 。
(5)在①~⑩元素的最高价氧化物对应的水化物中,呈两性的是___________ 。写出其与另两种水溶液之间相互反应的离子方程式___________ ,___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
(3)在①—⑫元素中,金属性最强的元素是
(4)第三周期中原子半径最大的元素是
(5)在①~⑩元素的最高价氧化物对应的水化物中,呈两性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】X、Y、L、M为核电荷数依次增大的前20号主族元素。X的原子半径最小,Y、L 与M三种元素的质子数均为5的倍数。回答下列问题:
(1)X与Y组成的化合物属于______ (填“共价”或“离子”)化合物.
(2)X与M组成的物质电子式为_____ ,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为___________ 。
(3)Y在周期表中的位置是_______ ,其含氧酸的化学式为_________ 。
(4)下列说法正确的是______ 。
A.L可能是Ne,也可能是P
B.L在氯气中燃烧现象为白色烟雾
C.L与X形成的化合物分子构型为平面三角形
D.L有多种氧化物以及含氧酸
(1)X与Y组成的化合物属于
(2)X与M组成的物质电子式为
(3)Y在周期表中的位置是
(4)下列说法正确的是
A.L可能是Ne,也可能是P
B.L在氯气中燃烧现象为白色烟雾
C.L与X形成的化合物分子构型为平面三角形
D.L有多种氧化物以及含氧酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】V2﹣、W3﹣、X2+、Y2﹣、Z﹣是由短周期元素形成的简单离子,其中V2﹣、W3﹣、X2+均是10电子的微粒,Y2﹣、Z﹣与Ar原子具有相同的电子数。(请用化学用语回答下列问题)
(1)V2﹣的离子结构示意图为_________________ 。
(2)V、W、X的原子半径由小到大的顺序是________________ 。
(3)元素Y、Z气态氢化物的热稳定性比较(填化学式):______________ 。
(4)将Z的单质通入石蕊溶液中发生的颜色变化如下图,请在方框内填写出导致该阶段颜色变化的主要粒子符号。________ 、________ 、________ 。

(1)V2﹣的离子结构示意图为
(2)V、W、X的原子半径由小到大的顺序是
(3)元素Y、Z气态氢化物的热稳定性比较(填化学式):
(4)将Z的单质通入石蕊溶液中发生的颜色变化如下图,请在方框内填写出导致该阶段颜色变化的主要粒子符号。

您最近一年使用:0次





