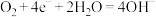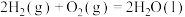1g正丁烷(C4H10)燃烧生成CO2和液态的水,放出49.6KJ热量,则其热化学方程式为
| A.2C4H10+13O2=8CO2+10H2O;△H=-5753.6KJ/mol |
| B.2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l);△H=-49.6KJ/mol |
| C.2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l);△H=-2876.8KJ/mol |
| D.C4H10(g)+13/2O2(g)=4CO2(g)+5H2O(l);△H=-2876.8KJ/mol |
更新时间:2022-10-31 20:03:18
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知H2(g)的燃烧热ΔH=-286kJ·mol-1,CH4(g)的燃烧热ΔH=-890kJ·mol-1,现有H2与CH4的混合气体89.6L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),若实验测得反应放热为2352kJ,则原混合气体中H2与CH4的物质的量之比是( )
| A.1:1 | B.1:3 | C.1:4 | D.2:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知: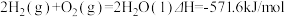 ①
①
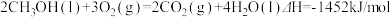 ②
②
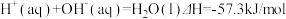
下列说法正确的是
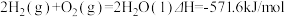 ①
①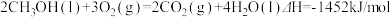 ②
②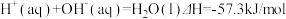
下列说法正确的是
| A.H2(g)的燃烧热为571.6kJ/mol |
| B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
C.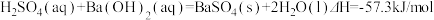 |
D.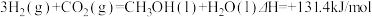 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值。已知反应;
①

②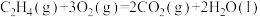

其他数据如下表:
下列说法正确的是
①


②
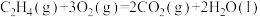

其他数据如下表:
| 化学键 | C=O | O=O | C-H | O-H | C=C |
键能/( ) ) | 798 | x | 413 | 463 | 610 |
A.a<b,且 的燃烧热为 的燃烧热为 |
B.上表中 |
C.  |
| D.当有4NA个C-H键断裂时,该反应放出热量一定为a kJ |
您最近一年使用:0次
【推荐2】下列说法正确的是( )
| A.在稀溶液中,1molH2SO4(aq)与1molBa(OH)2(aq)完全反应所放出的热量为中和热 |
| B.乙炔(C2H2)的燃烧热为1299.6kJ·mol-1,则2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)的ΔH=-2599.2kJ·mol-1 |
| C.等质量的硫蒸气和硫粉分别完全燃烧,前者放出的热量更多 |
| D.中和热化学方程式为:H+(l)+OH-(l)=H2O(l)ΔH=-57.3KJ/mol |
您最近一年使用:0次

 O2(g)=ZnO(s)
O2(g)=ZnO(s)