X、Y、Z、W、R是短周期元素,原子序数依次增大。非金属X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为_______ ;元素Z的离子结构示意图为_______ 。
(2)用电子式表示元素R氢化物的形成过程:_______ ;
(3)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为_______ 。
(4)元素W位于周期表的位置:_______ ,其非金属性比R弱,用原子结构的知识解释原因:_______ 。
(5)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与过量该氧化物反应的离子方程式:_______ 。
(1)元素X的最高价氧化物的电子式为
(2)用电子式表示元素R氢化物的形成过程:
(3)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为
(4)元素W位于周期表的位置:
(5)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与过量该氧化物反应的离子方程式:
更新时间:2022-12-19 07:38:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有A、B、C、D四种短周期主族元素,其相关性质信息如下。
请回答下列问题:
(1)元素D在元素周期表中的位置为___________ 。
(2)元素A和元素B形成的某种分子中含有18个电子,则该分子的电子式为___________ 。
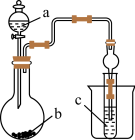
(3)若用如下装置证明元素C的非金属性强于D的非金属性,a、b、c均为化学药品,a为稀硫酸,那么c为___________ ,试管内发生的反应的离子方程式为___________ 。
| 元素编号 | 元素性质与原子结构 |
| A | 常温下,有 、 、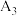 型两种气体单质存在 型两种气体单质存在 |
| B | 形成的常见离子核外电子数为0 |
| C | 最外层电子数是次外层的两倍 |
| D | 氧化物常被用来制造“光纤” |
(1)元素D在元素周期表中的位置为
(2)元素A和元素B形成的某种分子中含有18个电子,则该分子的电子式为
(3)若用如下装置证明元素C的非金属性强于D的非金属性,a、b、c均为化学药品,a为稀硫酸,那么c为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表表示的是元素周期表中短周期元素,根据要求回答下列问题:
(1)④⑥元素气态氢化物的稳定性比较______ >_______ (写化学式);
(2)③号元素与其他元素可形成10个电子的阳离子和阴离子,其离子符号分别为______ 、______ 。
(3)用电子式表示⑧和③元素形成A2B型化合物的过程_____________________
(4)用电子式表示⑤和⑥元素形成A2B型化合物的过程________________________
| ⑧ | |||||||
| ① | ② | ③ | ④ | ||||
| ⑤ | ⑥ | ⑦ | |||||
(1)④⑥元素气态氢化物的稳定性比较
(2)③号元素与其他元素可形成10个电子的阳离子和阴离子,其离子符号分别为
(3)用电子式表示⑧和③元素形成A2B型化合物的过程
(4)用电子式表示⑤和⑥元素形成A2B型化合物的过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有6种短周期元素的性质或原子结构如下表:
完成下列空白(涉及W、U、R、T、X、Y、Z时,用元素符号表示):
(1)元素T的原子共有______ 个电子;元素X的一种核素可测定文物年代,这种核素的
符号是___________ 。
(2)用电子式表示:
①气态化合物XR2_________________ ;
②元素W、R形成的10电子分子的形成过程______________________________ 。
(3)用离子方程式表示:
①元素Y与元素W形成的离子YW4+与NaOH溶液共热的反应______________ ;
②元素U的单质与NaOH溶液反应_______________________________________ 。
(4)元素Z与元素T相比,非金属性较强的是________ ,下列表述中能证明这一事实的
是_______ (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)探寻物质的性质差异性是学习的重要方法之一。在T、X、Y、Z四种元素的最高价
氧化物的水化物中,化学性质明显不同于其他三种的是______ (用分子式表示),
理由是____________________ 。
| 元素编号 | 元素性质或原子结构 |
| W | 周期表中原子半径最小的元素 |
| U | 地壳中含量最多的金属元素 |
| R | 单质为空气的主要成分 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(1)元素T的原子共有
符号是
(2)用电子式表示:
①气态化合物XR2
②元素W、R形成的10电子分子的形成过程
(3)用离子方程式表示:
①元素Y与元素W形成的离子YW4+与NaOH溶液共热的反应
②元素U的单质与NaOH溶液反应
(4)元素Z与元素T相比,非金属性较强的是
是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(5)探寻物质的性质差异性是学习的重要方法之一。在T、X、Y、Z四种元素的最高价
氧化物的水化物中,化学性质明显不同于其他三种的是
理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学选择如图装置(省略夹持仪器)对该方法进行模拟实验: 的顺序连接仪器,检查装置
的顺序连接仪器,检查装置___________ 。按 而不是
而不是 连接仪器的原因是
连接仪器的原因是___________ 。
2.下列关于铜与硝酸反应的叙述中,正确的是____。
3.先通入空气,再打开 中分液漏斗的活塞,观察到B中出现红棕色气体,此时,所获得的氮氧化物中一定含有
中分液漏斗的活塞,观察到B中出现红棕色气体,此时,所获得的氮氧化物中一定含有___________ 气体。
4.装置 除了能用于脱硝效果外,还可用于
除了能用于脱硝效果外,还可用于___________ 、___________ 。
5.常温常压下,以一定流速和比例混合 、空气等气体进行模拟实验,现测得
、空气等气体进行模拟实验,现测得 入口体积分数为
入口体积分数为 ,出口体积分数为
,出口体积分数为 ,则脱硝百分率为
,则脱硝百分率为___________  (因混合气体中
(因混合气体中 所占比例很小,可忽略脱硝前后气体总体积的变化,计算结果保留小数点后1位)。
所占比例很小,可忽略脱硝前后气体总体积的变化,计算结果保留小数点后1位)。
6.“封管实验”具有简易、方便、节约、绿色等优点,下列关于两个“封管实验”(夹持装置未画出)的说法错误的是___________。
 的顺序连接仪器,检查装置
的顺序连接仪器,检查装置 而不是
而不是 连接仪器的原因是
连接仪器的原因是2.下列关于铜与硝酸反应的叙述中,正确的是____。
| A.氮元素全部被还原 | B.若为稀硝酸,反应不进行 |
C. 是氧化产物 是氧化产物 | D.若为浓硝酸,还原产物为 |
 中分液漏斗的活塞,观察到B中出现红棕色气体,此时,所获得的氮氧化物中一定含有
中分液漏斗的活塞,观察到B中出现红棕色气体,此时,所获得的氮氧化物中一定含有4.装置
 除了能用于脱硝效果外,还可用于
除了能用于脱硝效果外,还可用于5.常温常压下,以一定流速和比例混合
 、空气等气体进行模拟实验,现测得
、空气等气体进行模拟实验,现测得 入口体积分数为
入口体积分数为 ,出口体积分数为
,出口体积分数为 ,则脱硝百分率为
,则脱硝百分率为 (因混合气体中
(因混合气体中 所占比例很小,可忽略脱硝前后气体总体积的变化,计算结果保留小数点后1位)。
所占比例很小,可忽略脱硝前后气体总体积的变化,计算结果保留小数点后1位)。6.“封管实验”具有简易、方便、节约、绿色等优点,下列关于两个“封管实验”(夹持装置未画出)的说法错误的是___________。
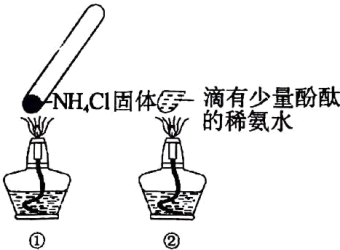
| A.实验①中,适当加热后,可观察到“封管”上端内壁上有固体附着 |
| B.实验②中,加热时“封管”内溶液变为无色,冷却后又变为浅红色 |
| C.两个“封管实验”中都发生了化学反应 |
D.实验②中 体现出的性质与 体现出的性质与 的喷泉实验( 的喷泉实验( ,滴有酚酞的水溶液)完全不同 ,滴有酚酞的水溶液)完全不同 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
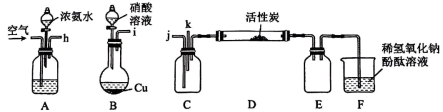
【推荐2】某校化学兴趣小组模拟汽车尾气无害化处理,使用一种高效催化剂将尾气中的CO和NO转变成对环境友好的气体,该小组设计的实验装置如图所示。请回答下列问题:
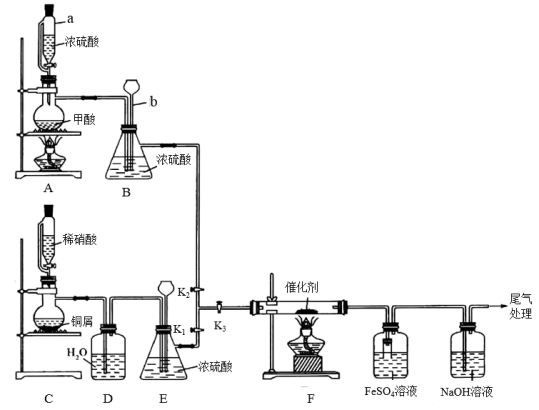
(1)仪器b的名称为__ 。该实验中仪器a与分液漏斗相比,其优点是__ 。
(2)甲酸在浓硫酸、加热条件下反应生成CO和水,这体现了浓硫酸的__ 性。有同学认为装置B前应该增加一个洗气装置,其理由是__ 。
(3)装置C中发生反应的离子方程式是__ 。有同学认为若用酒精灯加热装置C制取NO温度过高时会对本实验造成不利影响,原因是___ (填一条即可)。
(4)装置F中发生反应的化学方程式是___ 。
(5)已知NO气体与FeSO4溶液反应生成可溶性的硫酸亚硝基合铁(II):NO+FeSO4=Fe(NO)SO4,则图中尾气的主要成分是___ (填化学式);在实验中分别利用两种不同的催化剂催化装置F中的反应、且均控制CO过量和其他条件不变,请补充判断两种催化剂催化效率高低的方法和依据:在不同催化利催化下,反应相同时间内__ 。

(1)仪器b的名称为
(2)甲酸在浓硫酸、加热条件下反应生成CO和水,这体现了浓硫酸的
(3)装置C中发生反应的离子方程式是
(4)装置F中发生反应的化学方程式是
(5)已知NO气体与FeSO4溶液反应生成可溶性的硫酸亚硝基合铁(II):NO+FeSO4=Fe(NO)SO4,则图中尾气的主要成分是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表列出了A ~ R 9种元素在周期表中的位置:
请回答下列问题。
(1)这9种元素分别为:A.____ 、B.___ 、C.___ 、D.____ 、E._____ 、F.____ 、G.____ 、H.____ 、R.____ 。其中化学性质最不活泼的是____ (用元素符号作答)。
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_______ 。
(3)A、B、C三种元素按原子半径由大到小的顺序排列为_______ 。(用元素符号表示)
(4)F元素氢化物的化学式是_______ ,该氢化物在常温下与B发生反应的化学方程式是_______ ,所得溶液的pH _______ 7。
(5)H元素与A元素形成的化合物的电子式是___ 。高温灼烧该化合物时,火焰呈___ 色。
(6)G元素最高价氧化物对应的水化物的酸性比H元素最高价氧化物对应的水化物的酸性_____ (“强”或“弱”)。
| 周期 | 族 | ||||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | ||
| 2 | E | F | |||||||
| 3 | A | C | D | G | R | ||||
| 4 | B | H | |||||||
(1)这9种元素分别为:A.
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
(5)H元素与A元素形成的化合物的电子式是
(6)G元素最高价氧化物对应的水化物的酸性比H元素最高价氧化物对应的水化物的酸性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,其中B元素是碳元素。请回答下列问题:

(1)B元素在周期表中的位置:_________________ ;请写出该原子的电子式:___________ ;其原子核外电子能量最高的能级是:_______ 。
(2)比较A、C、D元素简单离子半径的大小:_______ >_______ >_______ (填微粒符号)。
(3)F与D同主族且相邻,请比较D的氢化物和F的氢化物稳定性大小:_______ (用化学式表示)。
(4)E单质常用湿润的淀粉碘化钾试纸检验。有学生对淀粉碘化钾进行了实验探究。在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,立刻会看到溶液变蓝色,这是因为_______ (请结合氧化还原反应知识解释相关现象,下同)。在所形成的蓝色溶液中,再滴加亚硫酸钠溶液,发现蓝色逐渐消失,这是因为_________________ 。据此分析,I2、ClO-、SO42-氧化性有弱到强的顺序排列为____________________ 。

(1)B元素在周期表中的位置:
(2)比较A、C、D元素简单离子半径的大小:
(3)F与D同主族且相邻,请比较D的氢化物和F的氢化物稳定性大小:
(4)E单质常用湿润的淀粉碘化钾试纸检验。有学生对淀粉碘化钾进行了实验探究。在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,立刻会看到溶液变蓝色,这是因为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室从海带浸取液中提取碘单质。
(1)碘的结构与性质
①碘原子核外有5个电子层,最外层有7个电子,碘元素在周期表中的位置是_______ 。
②质子数为53、中子数为78的碘核素表示为_______ 。
③设计简单的实验验证氯的非金属性比碘强:_____ 。(须用试剂:新制氯水、KI溶液,淀粉溶液)
(2)提取碘单质
I.萃取氧化法:向浸取液中加入 ,调节pH为3~4,加入
,调节pH为3~4,加入 ,再加入
,再加入 溶液,反应一段时间后得到
溶液,反应一段时间后得到 的
的 溶液。
溶液。
①调pH时不用盐酸来替代 的主要原因是
的主要原因是_______ 。(填序号)
a.盐酸易挥发使溶液pH变化快, 不易挥发溶液pH缓慢
不易挥发溶液pH缓慢
b. 为弱电解质,反应过程中电离出
为弱电解质,反应过程中电离出 维持溶液的pH
维持溶液的pH
②加入 的作用是
的作用是_______ ,得到 的
的 溶液。
溶液。
II.双氧化法:把浸取液分成A、B两份,在 催化下用
催化下用 把A溶液中的
把A溶液中的 氧化为
氧化为 ,然后与B溶液混合,经盐酸酸化得到碘单质。
,然后与B溶液混合,经盐酸酸化得到碘单质。
③ 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
④A、B两份溶液的体积比为_______ 时,可使碘的提取率最高。
(3)废液的处理:提取碘后的酸性废液中含有少量的 、
、 ,向废液中加入适量
,向废液中加入适量 把
把 氧化成
氧化成 ,然后加入活性炭,过滤后排放。活性炭的作用是
,然后加入活性炭,过滤后排放。活性炭的作用是_______ 。
(1)碘的结构与性质
①碘原子核外有5个电子层,最外层有7个电子,碘元素在周期表中的位置是
②质子数为53、中子数为78的碘核素表示为
③设计简单的实验验证氯的非金属性比碘强:
(2)提取碘单质
I.萃取氧化法:向浸取液中加入
 ,调节pH为3~4,加入
,调节pH为3~4,加入 ,再加入
,再加入 溶液,反应一段时间后得到
溶液,反应一段时间后得到 的
的 溶液。
溶液。①调pH时不用盐酸来替代
 的主要原因是
的主要原因是a.盐酸易挥发使溶液pH变化快,
 不易挥发溶液pH缓慢
不易挥发溶液pH缓慢b.
 为弱电解质,反应过程中电离出
为弱电解质,反应过程中电离出 维持溶液的pH
维持溶液的pH②加入
 的作用是
的作用是 的
的 溶液。
溶液。II.双氧化法:把浸取液分成A、B两份,在
 催化下用
催化下用 把A溶液中的
把A溶液中的 氧化为
氧化为 ,然后与B溶液混合,经盐酸酸化得到碘单质。
,然后与B溶液混合,经盐酸酸化得到碘单质。③
 氧化
氧化 的离子方程式为
的离子方程式为④A、B两份溶液的体积比为
(3)废液的处理:提取碘后的酸性废液中含有少量的
 、
、 ,向废液中加入适量
,向废液中加入适量 把
把 氧化成
氧化成 ,然后加入活性炭,过滤后排放。活性炭的作用是
,然后加入活性炭,过滤后排放。活性炭的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W、Q五种元素,它们在周期表中的相对位置如下表所示(虚线部分表示省略了部分族),回答下列问题:
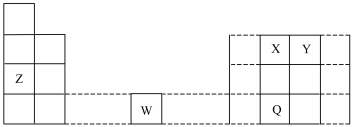
(1)已知元素的第一电离能X>Y,则X原子最高能级电子云轮廓图是_____ 形状;Y的简单氢化物中,Y原子的杂化轨道类型为_____ 。
(2)W核外电子有15种空间运动状态且电子运动状态数目最少,则W原子价层电子排布图为_____ ;五种元素中,第一电离能最小的是元素_____ (填元素名称),X、Y、Q三种元素电负性由大到小的顺序为_____ (用元素符号表示)。
(3)Q形成的氢化物分子的空间结构为_____ ,Z2Y2中化学键类型为_____ 。

(1)已知元素的第一电离能X>Y,则X原子最高能级电子云轮廓图是
(2)W核外电子有15种空间运动状态且电子运动状态数目最少,则W原子价层电子排布图为
(3)Q形成的氢化物分子的空间结构为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有A、B、C、D四种短周期元素,它们的相关结构和性质信息如下表所示,请结合相关信息,完成相关的问题:
(1)表中所述A的单质晶体中微粒间的相互作用有_______ 、_______ 。
(2)B元素的氧化物所对应的晶体属于__________ 晶体(填“分子”、“原子”、“离子”、“金属”),工业上制备B元素单质的化学方程式:________ 。
(3)C元素的气态氢化物的分子为__________ (填“极性”或“非极性”)分子,其溶于水后溶液呈碱性的原因____ (用方程式表示),C元素原子核外最外层电子的轨道表示式为_______ 。
(4)与D同主族的短周期元素,其单质及其化合物与D的单质及其化合物均具有的性质为______ (填序号)。
A 常温下单质跟水剧烈反应并放出氧气 B 气态氢化物具有很强的热稳定性
C 气态氢化物极易溶于水并呈强酸性 D 在HXO中X的化合价均为+1价
| 元素 | 相关结构和性质 |
| A | 其单质的一种晶体虽不是金属晶体,但是电的良导体,且难熔、质软并有润滑性,可用作原子核反应堆的慢化剂、火箭发动机喷管和电极材料等。 |
| B | 其单质既能与强酸溶液反应,又能与强碱溶液反应,其简单离子在第三周期单核离子中半径最小。 |
| C | 是蛋白质的组成元素之一,原子核外有3种不同能量的电子,且未成对电子数最多。 |
| D | 原子核外最外层电子排布式为nsnnp2n+1 |
(2)B元素的氧化物所对应的晶体属于
(3)C元素的气态氢化物的分子为
(4)与D同主族的短周期元素,其单质及其化合物与D的单质及其化合物均具有的性质为
A 常温下单质跟水剧烈反应并放出氧气 B 气态氢化物具有很强的热稳定性
C 气态氢化物极易溶于水并呈强酸性 D 在HXO中X的化合价均为+1价
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。五种元素中A元素原子半径最小;B原子的最外层电子数是内层电子数的2倍;E元素与D元素同主族;E的单质为黄色固体,自然界中游离态的E常出现在火山口附近。
(1)请写出元素符号:B___________ ;D___________ 。
(2)画出E的阴离子结构示意图_______________________ 。
(3)B、C两种元素对应的最高价含氧酸的酸性较强的是_____________ (填化学式)。
(4)A元素的单质和C元素的单质在一定条件下反应,生成化合物X。 X 的电子式为____________ ,向X的水溶液中滴入石蕊试液,会观察到的现象是_____________ 。
(5)用电子式表示化合物BD2的形成过程____________________________ 。
(6)向苛性钠溶液中通入过量的A2E气体时,所发生反应的离子方程式为_________ 。
(7)化合物ED2与氯气的水溶液充分反应可生成两种强酸,该反应的化学方程式为_____________________________________ 。
(1)请写出元素符号:B
(2)画出E的阴离子结构示意图
(3)B、C两种元素对应的最高价含氧酸的酸性较强的是
(4)A元素的单质和C元素的单质在一定条件下反应,生成化合物X。 X 的电子式为
(5)用电子式表示化合物BD2的形成过程
(6)向苛性钠溶液中通入过量的A2E气体时,所发生反应的离子方程式为
(7)化合物ED2与氯气的水溶液充分反应可生成两种强酸,该反应的化学方程式为
您最近一年使用:0次




