化学电源分为一次电池、二次电池和燃料电池,它们在生产生活中具有广泛的应用及发展前景。
(1)一种可充电的“锂—空气电池”的工作原理如图1所示。

①电池放电过程中,金属锂发生______ (填“氧化”或“还原”)反应。
②电池正极的反应式为_______ 。
(2)镍镉电池是二次电池,其工作原理如图2所示(L为小灯泡,K1、K2为开关,a、b为直流电源的两极)。
①断开K2、闭合K1,此时镍镉电池的能量转化形式为______ 。
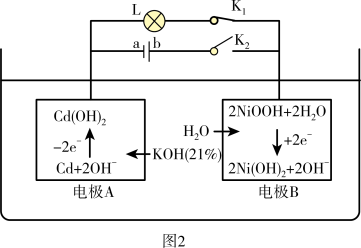
②电极B发生氧化反应过程中,溶液中KOH浓度______ (填“增大”、“减小”或“不变”)。
(3)研究HCOOH燃料电池性能的装置如图3所示,两电极之间用允许K+、H+通过的半透膜隔开。
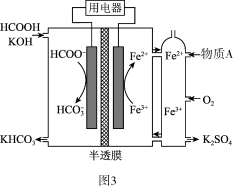
①电池负极的电极反应式为______ ;放电过程中需补充的物质A为______ (填化学式)。
②电池工作时每消耗标准状况下22.4LO2,电路中转移电子的数目为______ NA。
(1)一种可充电的“锂—空气电池”的工作原理如图1所示。

①电池放电过程中,金属锂发生
②电池正极的反应式为
(2)镍镉电池是二次电池,其工作原理如图2所示(L为小灯泡,K1、K2为开关,a、b为直流电源的两极)。
①断开K2、闭合K1,此时镍镉电池的能量转化形式为

②电极B发生氧化反应过程中,溶液中KOH浓度
(3)研究HCOOH燃料电池性能的装置如图3所示,两电极之间用允许K+、H+通过的半透膜隔开。

①电池负极的电极反应式为
②电池工作时每消耗标准状况下22.4LO2,电路中转移电子的数目为
更新时间:2023-01-09 08:55:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求书写方程式
(1)少量铁与稀硝酸反应的离子方程式:_______ 。
(2)Na2S2O3和稀硫酸反应的离子方程式:_______ 。
(3)SO2催化氧化的化学方程式:_______ 。
(4)NO2气体溶于水的化学方程式:_______ 。
(5)工业制备粗硅的化学方程式:_______ 。
(6)负极电极方程式:_______ 。

(1)少量铁与稀硝酸反应的离子方程式:
(2)Na2S2O3和稀硫酸反应的离子方程式:
(3)SO2催化氧化的化学方程式:
(4)NO2气体溶于水的化学方程式:
(5)工业制备粗硅的化学方程式:
(6)负极电极方程式:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,甲、乙两U形管各盛有100mL溶液,请回答下列问题:
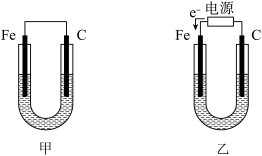
(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生_____________ 腐蚀(填“析氢”或“吸氧”),碳棒上电极反应式__________________________ ;
②甲池铁棒腐蚀的速率比乙池铁棒_____ (填“快”、“慢”或“相等”)。
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式___________________________________ ;
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为___________ mol·L-1。

(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生
②甲池铁棒腐蚀的速率比乙池铁棒
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据原电池原理可以设计原电池,实现多种用途

(1) 可以用如图所示装置吸收SO2并制取硫酸,写出通入SO2和O2的电极的电极反应式及反应的总方程式。
负极________________________________
正极________________________________
总反应_________________________________________ 。
(2) 如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。

试回答下列问题:
①图中通过负载的电子流动方向________ (填“向左”或“向右”)。
②写出氢氧燃料电池工作时电极反应方程式。
正极:_________________________ ,负极:____________________________ ,
③若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,
正极反应式为__________________________________________________ ;
负极反应式为__________________________________________________ 。

(1) 可以用如图所示装置吸收SO2并制取硫酸,写出通入SO2和O2的电极的电极反应式及反应的总方程式。
负极
正极
总反应
(2) 如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流。

试回答下列问题:
①图中通过负载的电子流动方向
②写出氢氧燃料电池工作时电极反应方程式。
正极:
③若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,
正极反应式为
负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】锂电池应用广泛,大致可分为锂金属电池和锂离子电池。锂离子电池工作原理:以石墨/锂钴氧电池为例,其总反应方程式为:LiCoO2+6C Li1-xCoO2+LixC6
Li1-xCoO2+LixC6

试回答下列问题:
(1)连接K1、K2时,a作___ 极。
(2)连接K2、K3时,被还原的物质是___ 。
(3)放电时,负极发生反应的电极反应式是___ 。
(4)锂离子电池的电极废料(含LiCoO2)中的金属可回收利用。
①将电极废料磨碎后用酸浸出,磨碎的目的是___ 。
②将电极废料用盐酸浸出,得到含Li+、Co2+的溶液,并有黄绿色气体生成,则该反应的化学方程式是___ 。
 Li1-xCoO2+LixC6
Li1-xCoO2+LixC6
试回答下列问题:
(1)连接K1、K2时,a作
(2)连接K2、K3时,被还原的物质是
(3)放电时,负极发生反应的电极反应式是
(4)锂离子电池的电极废料(含LiCoO2)中的金属可回收利用。
①将电极废料磨碎后用酸浸出,磨碎的目的是
②将电极废料用盐酸浸出,得到含Li+、Co2+的溶液,并有黄绿色气体生成,则该反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是一种正在投入生产的蓄电系统。电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为 Na2S4和 NaBr。

(1)左侧储罐中的电解质是________________ ,右侧储罐中的电解质是 _________ 。在放电过程中钠离子通过膜的流向是_________________ (填“左→右”或“右→左”)。
(2)电池放电时,正极的电极反应是_______________ ,负极的电极反应是________ 。
(3)该装置也可以用于锂电池。它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因_______________________________ 。

(1)左侧储罐中的电解质是
(2)电池放电时,正极的电极反应是
(3)该装置也可以用于锂电池。它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】我国科学家研发的水系可逆Zn-CO2电池可吸收利用CO2.将两组正离子、负离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的H2O解离成H+和OH—,工作原理如图所示:_____ 。
(2)充电时复合膜中向多孔Pd纳米片极移动的离子是_____ ,放电时正极的电极反应式为_____ 。
(3)下列说法中正确的是_____。
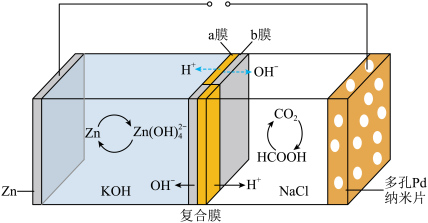
(2)充电时复合膜中向多孔Pd纳米片极移动的离子是
(3)下列说法中正确的是_____。
| A.放电时锌做阳极 |
| B.充电时多孔Pd纳米片极发生还原反应 |
| C.Na2[Zn(OH)4]中只存在离子键和配位键 |
D.Zn(OH) 可在足量稀硫酸中转化为Zn2+ 可在足量稀硫酸中转化为Zn2+ |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的重大贡献。
(1)将纯锌片和纯铜片按图甲、图乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:______ ,该烧杯中铜片上的现象为______ 。
②在相同时间内,两烧杯中产生气泡的速度:甲______ 乙(填“>”“<”或“=”)。
③形成原电池的装置中电子移动的方向是:流向______ (写电极材料的名称)
④当甲中溶液质量增重31.5g时,电极上转移电子数目为______ 。
(2)燃料电池是一种高效、环境友好的发电装置,图丁为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。通甲烷一极的为电池的______ (填“正极”或“负极”),写出负极电极反应式______ 。
(1)将纯锌片和纯铜片按图甲、图乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
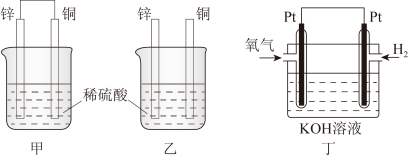
②在相同时间内,两烧杯中产生气泡的速度:甲
③形成原电池的装置中电子移动的方向是:流向
④当甲中溶液质量增重31.5g时,电极上转移电子数目为
(2)燃料电池是一种高效、环境友好的发电装置,图丁为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。通甲烷一极的为电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】正确认识和使用电池有利于我们每一个人的日常生活。
I.电化学法处理SO2是目前研究的热点。利用双氧水氧化吸收SO2可消除SO2污染,设计装置如图所示(已知石墨只起导电作用,质子交换膜只允许H+通过)。

(1)石墨1为________ (填“正极”或“负极”),正极的电极反应式为________________ 。
(2)反应的总方程式为____________________________ 。
(3)放电时H+迁移向_________ 。(填“正极”或“负极”)
(4)某同学关于原电池的笔记中,不合理的有__________ 。
①原电池两电极材料活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-浓硝酸-Cu原电池,Fe是负极
④原电池是将化学能转变为电能的装置
Ⅱ.航天技术中使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。
(1)某碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应为_______ 。
(2)氢氧燃料电池用于航天飞船,电极反应产生的水,经过冷凝后可用作航天员的饮用水,当得到1.8g饮用水时,转移的电子数为_____________ 。
I.电化学法处理SO2是目前研究的热点。利用双氧水氧化吸收SO2可消除SO2污染,设计装置如图所示(已知石墨只起导电作用,质子交换膜只允许H+通过)。

(1)石墨1为
(2)反应的总方程式为
(3)放电时H+迁移向
(4)某同学关于原电池的笔记中,不合理的有
①原电池两电极材料活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-浓硝酸-Cu原电池,Fe是负极
④原电池是将化学能转变为电能的装置
Ⅱ.航天技术中使用的氢氧燃料电池具有高能、轻便和不污染环境等优点。
(1)某碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应为
(2)氢氧燃料电池用于航天飞船,电极反应产生的水,经过冷凝后可用作航天员的饮用水,当得到1.8g饮用水时,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。放电时,该电池总反应式为:Pb+PbO2+2H2SO4  2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
(1)该蓄电池的负极材料是_________ ,放电时发生_________ (填“氧化”或“还原”)反应。
(2)该蓄电池放电时,电解质溶液的酸性_________ (填“增大”、“减小”或“不变”),电解质溶液中阴离子移向_________ (填“正”或“负”)极。
(3)已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。试写出该电池放电时,正极的电极反应_______________________________________ (用离子方程式表示)。
(4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为H2SO4溶液,则氢氧燃料电池的正极反应式为__________________________________ 。该电池工作时,外电路每流过1×103 mol e-,消耗标况下氧气_________ m3。
 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:(1)该蓄电池的负极材料是
(2)该蓄电池放电时,电解质溶液的酸性
(3)已知硫酸铅为不溶于水的白色固体,生成时附着在电极上。试写出该电池放电时,正极的电极反应
(4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为H2SO4溶液,则氢氧燃料电池的正极反应式为
您最近一年使用:0次



