碱性锌锰电池的总反应为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2。下列说法正确的是
| A.Zn为正极,MnO2为负极 |
| B.该电池为二次电池 |
| C.负极的电极反应式为:Zn+2OH--2e-=Zn(OH)2 |
D.工作时电子由MnO2经外电路流向 |
更新时间:2023-01-12 13:23:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组设计的水果电池装置如图所示。该电池工作时,下列说法正确的是
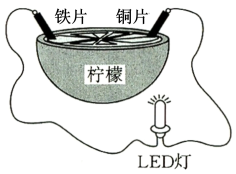

| A.铜片为水果电池的负极 | B.电子由LED灯经导线流向铁片 |
| C.负极的电极反应为:Fe-2e-=Fe2+ | D.可将柠檬替换成盛装酒精的装置 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染,其电池反应为2Zn+O2===2ZnO,原料为锌粒、KOH电解液和空气,则下列叙述正确的是( )
| A.锌为正极,空气进入负极反应 | B.负极反应为Zn+2OH--2e-===ZnO+H2O |
| C.正极发生氧化反应 | D.放电时电子在溶液中从正极向负极移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为某原电池的示意图,下列有关说法正确的是

| A.电子由铜棒流出 |
| B.能量由电能转化为化学能 |
| C.反应一段时间后,溶液变蓝 |
| D.锌片上发生氧化反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】镁锂双盐电池是结合镁离子电池和锂离子电池而设计的新型二次离子电池。其工作原理如图所示,已知放电时,b极转化关系为:VS2→LixVS2。下列有关说法不正确的是
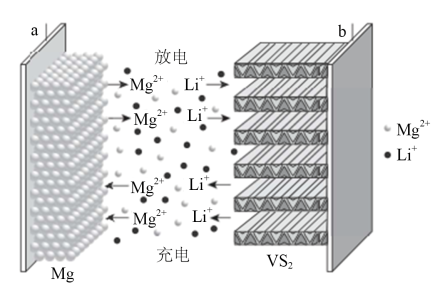

| A.充电或放电时,b极电势均高于a极 |
| B.放电过程中正极质量减少,负极质量增加 |
| C.充电时阳极的电极反应式为LixVS2-xe-=VS2+xLi+ |
D.该电池工作时,负极质量变化mg,理论上通过电路转移的电子数为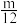 mol mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】普通锌锰干电池的简图如图所示,它是用锌皮制成的锌筒作为电极,中央插一根石墨棒,石墨棒顶端加一铜帽。在石墨棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液。该电池工作时的总反应为Zn+2NH +2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
+2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
 +2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是
+2MnO2= [Zn(NH3)2]2++2MnO(OH)。下列关于锌锰干电池的说法中正确的是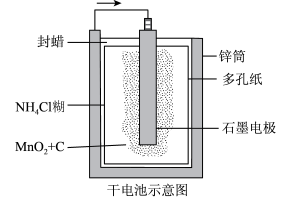
| A.当该电池电压逐渐下降后,利用电解原理能重新充电复原 |
B.电池负极反应为2MnO2+2NH +2e-=Mn2O3+2NH3+H2O +2e-=Mn2O3+2NH3+H2O |
| C.原电池工作时,电子从负极通过外电路流向正极 |
| D.外电路中每通过0.1 mol 电子,锌的质量理论上减少6.5 g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应: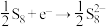 ,
,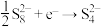 ,
,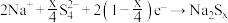
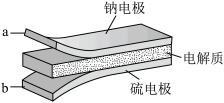
下列叙述错误的是
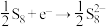 ,
,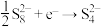 ,
,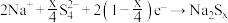

下列叙述错误的是
| A.炭化纤维素纸的作用是增强硫电极导电性能 |
B.放电时负极反应为: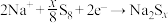 |
C.充电时 从硫电极向钠电极迁移 从硫电极向钠电极迁移 |
D.放电时外电路电子流动的方向是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家发明的一种可控锂水电池的工作原理如图所示。下列有关说法正确的是
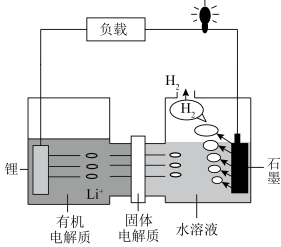
A.正极的电极反应式为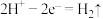 |
| B.电子流向:锂→负载→石墨→固体电解质 |
C.锂电极质量减轻7g,石墨极放出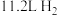 |
D.石墨电极附近溶液 升高 升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】有关如图所示四个常用电化学装置的叙述中,正确的是


A.图I所示电池中, 的作用是作催化剂 的作用是作催化剂 |
| B.图Ⅱ所示电池放电过程中,负极质量不断增加 |
| C.图Ⅲ所示装置工作过程中,电解质溶液质量将增加 |
D.图Ⅳ所示电池中,正极的电极反应式为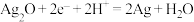 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】物质的性质决定用途,下列两者对应关系中正确的是
| A.汽油和植物油都属于烃,所以汽油和植物油都可以燃烧 |
B.苯的密度小于 ,所以苯不能萃取出溴的 ,所以苯不能萃取出溴的 溶液中的溴 溶液中的溴 |
| C.锌具有还原性和导电性,所以可用作锌锰干电池的负极材料 |
| D.硅胶多孔,吸水能力强,所以可用作食品的脱氧剂 |
您最近一年使用:0次


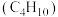 是一种重要的化工原料。丁烷的燃料电池工作原理如图所示,下列说法正确的是
是一种重要的化工原料。丁烷的燃料电池工作原理如图所示,下列说法正确的是

 电子,此时消耗
电子,此时消耗 的质量为
的质量为


