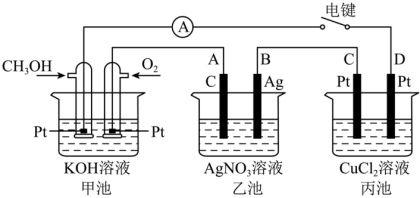
如图是一个化学过程的示意图,回答下列问题:
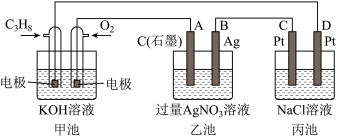
(1)甲池是_______ 装置,电极B的名称是_______ 。
(2)甲装置中通入 的电极反应
的电极反应_______ ,丙装置中D极的产物是_______ (写化学式)。
(3)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的
_______ 。(已知:NaCl溶液足量,电解后溶液体积为200mL)。乙池的PH值将_______ (填“变大”、“变小”或“不变”)
(4)若要使乙池恢复电解前的状态,应向乙池中加入_______ (写物质化学式)。

(1)甲池是
(2)甲装置中通入
 的电极反应
的电极反应(3)一段时间,当乙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的

(4)若要使乙池恢复电解前的状态,应向乙池中加入
更新时间:2023-01-13 18:17:25
|
相似题推荐
【推荐1】完成下列问题
(1)写下列反应的离子方程式
①实验室用二氧化锰和浓盐酸共热制氯气:___________
②向明矾溶液滴加 溶液至
溶液至 刚好沉淀完全:
刚好沉淀完全:___________
(2)25℃时,在等体积的① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液、④纯水中,发生电离的水的物质的量之比是
溶液、④纯水中,发生电离的水的物质的量之比是___________
(3)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示,对图中线间距离窄小的部分,其能量差用 的方式表示。由图可知合成氨反应
的方式表示。由图可知合成氨反应 的
的
___________  ,反应速率最慢的步骤的化学方程式为
,反应速率最慢的步骤的化学方程式为___________

(4)科学家利用电解法在常温常压下实现合成氨,工作时阴极区的微观反应过程如图所示,其中电解液为溶解有三氟甲磺酸锂和乙醇的有机溶液。

①阴极区生成 的电极反应式为
的电极反应式为___________ 。
②下列说法正确的是___________ (填标号)。
A.三氟甲磺酸锂的作用是增强导电性
B.选择性透过膜可允许 和
和 通过,防止
通过,防止 进入装置
进入装置
C.保持电流强度不变,升高溶液的温度,可以加快电解反应的速率
(1)写下列反应的离子方程式
①实验室用二氧化锰和浓盐酸共热制氯气:
②向明矾溶液滴加
 溶液至
溶液至 刚好沉淀完全:
刚好沉淀完全:(2)25℃时,在等体积的①
 溶液、②
溶液、② 溶液、③
溶液、③ 溶液、④纯水中,发生电离的水的物质的量之比是
溶液、④纯水中,发生电离的水的物质的量之比是(3)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示,对图中线间距离窄小的部分,其能量差用
 的方式表示。由图可知合成氨反应
的方式表示。由图可知合成氨反应 的
的
 ,反应速率最慢的步骤的化学方程式为
,反应速率最慢的步骤的化学方程式为
(4)科学家利用电解法在常温常压下实现合成氨,工作时阴极区的微观反应过程如图所示,其中电解液为溶解有三氟甲磺酸锂和乙醇的有机溶液。

①阴极区生成
 的电极反应式为
的电极反应式为②下列说法正确的是
A.三氟甲磺酸锂的作用是增强导电性
B.选择性透过膜可允许
 和
和 通过,防止
通过,防止 进入装置
进入装置C.保持电流强度不变,升高溶液的温度,可以加快电解反应的速率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1.水溶液中电解制备金属钴的装置示意图如图所示。工作时,Ⅱ室溶液的
_______ (填“增大”“减小”或“不变”);电解总反应为_______ 。当生成 时,Ⅰ室溶液质量理论上减少
时,Ⅰ室溶液质量理论上减少_______ g。


 时,Ⅰ室溶液质量理论上减少
时,Ⅰ室溶液质量理论上减少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.根据电化学相关知识,回答问题:
(1)如甲图为电解精炼银的示意图,_____ (填“a”或“b”)极为含有杂质的粗银。
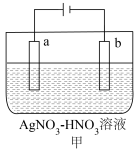
(2)利用如乙图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。阳极电极反应式为______ ,电解过程中Li+向______ (填“A”或“B”)电极迁移。

II.如图X是直流电源,c、d为石墨棒,e、f是质量相同的铜棒。接通电路后,发现d附近显红色。

(3)①b为电源的______ 极(填“正”“负”“阴”或“阳”,下同)。
②Z池中e为______ 极。
③连接Y、Z池线路,电子流动的方向是d_____ e(用“→”或“←”填空)。
(4)写出c极上反应的电极反应式:______ 。
(1)如甲图为电解精炼银的示意图,

(2)利用如乙图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。阳极电极反应式为

II.如图X是直流电源,c、d为石墨棒,e、f是质量相同的铜棒。接通电路后,发现d附近显红色。

(3)①b为电源的
②Z池中e为
③连接Y、Z池线路,电子流动的方向是d
(4)写出c极上反应的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铅蓄电池是重要的二次电池。已知:铅蓄电池总的化学方程式为: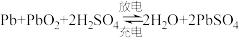 ,回答下列问题:
,回答下列问题:
(1)铅蓄电池负极板上覆盖的物质是__________ (填名称),充电时,PbSO4在__________ (填“阳极”、“阴极”或“两个电极”)上__________ (填“生成或除去”)。
(2)铅蓄电池在充电时正极接电源的__________ (正极/负极),充电时该极的电极反应式为__________ 。
(3)用铅蓄电池作为电源,电解饱和食盐水,电极均为惰性电极,电解饱和食盐水总反应的化学方程式为__________ 。当铅蓄电池负极生成2molPbSO4时,_________ (阴极/阳极)产生________ molH2。
(4)电解饱和食盐水工业生产中,采用了__________ (阴/阳)离子交换膜,这样做的原因有__________ 。
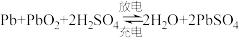 ,回答下列问题:
,回答下列问题:(1)铅蓄电池负极板上覆盖的物质是
(2)铅蓄电池在充电时正极接电源的
(3)用铅蓄电池作为电源,电解饱和食盐水,电极均为惰性电极,电解饱和食盐水总反应的化学方程式为
(4)电解饱和食盐水工业生产中,采用了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是一个化学过程的示意图。
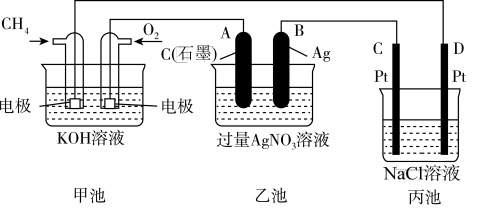
(1)C(Pt)电极的名称是__________ 。
(2)写出通入O2的电极上的电极反应式_______________________ 。
(3)写出通入CH3OH的电极上的电极反应式________________________ 。
(4)丙池的阳极电极反应为________________________ 。
(5)写出乙池中反应的化学方程式________________________ 。
(6)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2_________ mL(标准状况下);若丙池中饱和食盐水溶液的体积为500 mL,电解后,溶液的pH=________ 。(25℃,假设电解前后溶液的体积无变化)。

(1)C(Pt)电极的名称是
(2)写出通入O2的电极上的电极反应式
(3)写出通入CH3OH的电极上的电极反应式
(4)丙池的阳极电极反应为
(5)写出乙池中反应的化学方程式
(6)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某课外小组设计如图1所示装置为电源对粗铜(含有Cu,少量Fe、Zn、Ag、Au等)进行精炼。
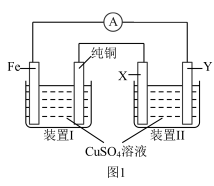
(1)装置Ⅰ中Fe电极上发生反应的电极反应式为___________ 。
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为___________ mol,装置Ⅰ的能量转化率为___________ 。(已知:装置Ⅰ中 足量)
足量)
(3)有同学提议,为避免副反应的发生,应将装置Ⅰ改为如图2所示装置,则溶液Z中溶质的化学式为___________ ,阴离子交换膜的作用为___________ (任写一条)。
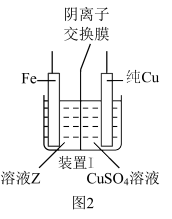
(4)装置Ⅱ中X电极材料的名称为___________ ,Y电极上的电极反应式为___________ ,一段时间后,装置Ⅱ溶液中阳离子主要为 和
和___________ 。

(1)装置Ⅰ中Fe电极上发生反应的电极反应式为
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为
 足量)
足量)(3)有同学提议,为避免副反应的发生,应将装置Ⅰ改为如图2所示装置,则溶液Z中溶质的化学式为

(4)装置Ⅱ中X电极材料的名称为
 和
和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某课外活动小组用如图所示装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应式为___________ 。
(2)若开始时开关K与b极连接,则B极的电极反应式为___________ ,总反应的离子方程式为___________ 。
(3)若开始时开关K与b连接,下列说法正确的是___________(填字母)。
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用惰性电极及如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为___________ 。
②制得的氢氧化钾溶液从出口___________ (填“A”“B”“C”或“D”)导出。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b极连接,则B极的电极反应式为
(3)若开始时开关K与b连接,下列说法正确的是___________(填字母)。
| A.溶液中Na+向A极移动 |
| B.从A极处逸出的气体能使湿润的KI-淀粉试纸变蓝 |
| C.反应一段时间后加适量盐酸可恢复到电解前电解质溶液的浓度 |
| D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子 |

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:

(1)断开K2,闭合K1,若所盛溶液为CuSO4溶液,则A极为________ 极,B极的电极反应式为_________________________________________ 。若所盛溶液为KCl溶液,则B极的电极反应式为__________________________________ 。
(2)断开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可以观察到的现象是________ ,Na+移向________ (填“A”或“B”)极。
②B电极上的电极反应式为______________________________________ ,总反应的化学方程式是_________________________________________ 。
③反应一段时间后断开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL,将溶液充分混合,溶液的pH约为________ 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的________ 。

(1)断开K2,闭合K1,若所盛溶液为CuSO4溶液,则A极为
(2)断开K1,闭合K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可以观察到的现象是
②B电极上的电极反应式为
③反应一段时间后断开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL,将溶液充分混合,溶液的pH约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图所示,在用石墨作电极的电解池中,加入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极上有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,经洗涤、干燥、称量,发现电极质量增加1.6g。请回答下列问题:

(1)写出B电极的电极反应式:_______ 。
(2)写出电解时总反应的离子方程式:_________ 。
(3)要使电解后的溶液恢复到电解前的状态,则可加入______ ,其质量为_____ 。(假设电解前后溶液的体积不变)

(1)写出B电极的电极反应式:
(2)写出电解时总反应的离子方程式:
(3)要使电解后的溶液恢复到电解前的状态,则可加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电解装置如图所示:
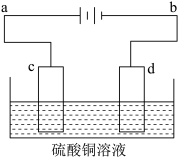
Ⅰ.当用惰性电极电解时,c为____________ 极, d极的电极反应_________ ,电解总反应的化学方程____________________
Ⅱ.(1)若用此装置进行铁上镀铜则c为__________ (填铁或铜),电解液浓度_____________ (增大,减小或不变)
(2)电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________ mol.
Ⅲ.若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极________ (填图中的字母)。

Ⅰ.当用惰性电极电解时,c为
Ⅱ.(1)若用此装置进行铁上镀铜则c为
(2)电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子
Ⅲ.若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,其中甲池的总反应为2CH3OH+3O2+4KOH=2K2CO3+6H2O,回答下问题:
请回答下列问题:
(1)甲池为_______ (填“原电池”、“电解池”或“电镀池”),负极的电极反应式为_______ 。
(2)乙池A(石墨)电极的名称为_______ (填“正极”、“负极”、“阴极”或“阳极”),乙池中总反应式为_______ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为_______ mL(标准状况下),丙池中析出_______ g铜。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是_______(填选项字母)。
(5)若丙中电极不变,将其溶液换成含酚酞的NaCl溶液,电键闭合一段时间后,丙中D极附近观察到的现象是_______ ,溶液的pH将_______ (填“增大”、“减小”或“不变”)。C电极上的电极反应式为_______ ,检验该电极反应产物的方法是_______ 。
(6)若用丙装置电解精炼铜,粗铜(内含Zn、Fe、Ni等杂质)应该放在_______ (填C、D)极,电解进行一段时间后,电解质溶液中CuSO4的浓度将_______ (填“增大”、“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是_______(填选项字母)。
| A.Ag | B.Ag2O | C.AgOH | D.AgCl |
(6)若用丙装置电解精炼铜,粗铜(内含Zn、Fe、Ni等杂质)应该放在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烧, 电解质是熔融碳酸盐,电池总反应方程式为:C3H8+5O2 = 3CO2+4H2O。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=________ (用△H1、△H2、△H3表示)
(2)写出该电池正极的电极反应式:_________ ,电池工作时CO32-移向_________ (填“正极”或“负极”);用该电池电解1000 mL lmol/L的AgNO3溶液(惰性电极),此电解池的反应方程式为_____________________________________ 。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=
(2)写出该电池正极的电极反应式:
您最近一年使用:0次



