氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g。则样品中氨基甲酸铵的物质的量分数为_______ 。[Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(CaCO3)=100]
2023高三·全国·专题练习 查看更多[1]
(已下线)专题03 物质的量的基本计算-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
更新时间:2023-02-02 11:30:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)标准状况下,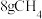 与
与_______ 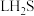 气体含有相同的氢原子数。
气体含有相同的氢原子数。
(2)19g某二价金属的氯化物 中含有0.4mol的
中含有0.4mol的 ,则R的相对原子质量为
,则R的相对原子质量为_______ 。
(3)如图是“康师傅”牌饮用矿泉水的标签的部分内容。
请认真阅读标签内容,计算:
①镁离子的物质的量浓度的最大值是_______ 。
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过_______ mol。
(4)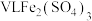 溶液中含
溶液中含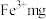 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为_______  。
。
(5)摩尔是以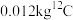 中所含的原子数目为标准,来衡量其它粒子集体中所含粒子数目的多少。如果定义
中所含的原子数目为标准,来衡量其它粒子集体中所含粒子数目的多少。如果定义 个
个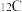 原子的物质的量为1mol,那么此时标准状况下,气体摩尔体积的数值约为
原子的物质的量为1mol,那么此时标准状况下,气体摩尔体积的数值约为_______ L/mol。
(1)标准状况下,
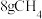 与
与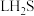 气体含有相同的氢原子数。
气体含有相同的氢原子数。(2)19g某二价金属的氯化物
 中含有0.4mol的
中含有0.4mol的 ,则R的相对原子质量为
,则R的相对原子质量为(3)如图是“康师傅”牌饮用矿泉水的标签的部分内容。
| 康师傅饮用矿物质水 净含量:350mL 配料表:纯净水硫酸镁氯化钾 保质期:12个月 主要成分: 钾离子 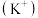 :1.0~27.3mgL :1.0~27.3mgL镁离子 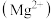 :0.1~4.8mg/L :0.1~4.8mg/L氯离子 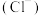 :10~27.3mg/L :10~27.3mg/L硫酸根离子  :0.4~19.2mgL :0.4~19.2mgL |
请认真阅读标签内容,计算:
①镁离子的物质的量浓度的最大值是
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过
(4)
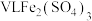 溶液中含
溶液中含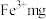 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为 。
。(5)摩尔是以
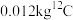 中所含的原子数目为标准,来衡量其它粒子集体中所含粒子数目的多少。如果定义
中所含的原子数目为标准,来衡量其它粒子集体中所含粒子数目的多少。如果定义 个
个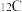 原子的物质的量为1mol,那么此时标准状况下,气体摩尔体积的数值约为
原子的物质的量为1mol,那么此时标准状况下,气体摩尔体积的数值约为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)如何运用最简方法检验NaCl溶液中有无 离子?
离子?_________ 。
(2)在同温同压下,相等质量的氧气和臭氧,它们的物质的量之比为________ ,分子个数比为________ ,原子个数比为________ 。
(3)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2===2NO2,充分反应后容器中氮原子和氧原子的个数之比为________ 。
 离子?
离子?(2)在同温同压下,相等质量的氧气和臭氧,它们的物质的量之比为
(3)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2===2NO2,充分反应后容器中氮原子和氧原子的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)湿法制备高铁酸钾的反应体系有六种微粒: 。
。
①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是______ 。
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为______ mol。
③高铁酸钾作为一种理想的水处理剂,其处理水的原理______
(2)铁明矾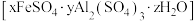 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
①称取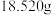 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。
②量取 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
体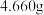 。
。
③再量取 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。
(已知 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)
①在25.00mL试样中,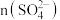
______ mol,
______ mol。
②铁明矾的化学式为______ (写出详细的解题步骤)
(1)湿法制备高铁酸钾的反应体系有六种微粒:
 。
。①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为
③高铁酸钾作为一种理想的水处理剂,其处理水的原理
(2)铁明矾
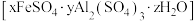 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。①称取
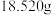 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。②量取
 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体
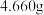 。
。③再量取
 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。(已知
 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)①在25.00mL试样中,
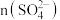

②铁明矾的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.现有下列十种物质:①H2 ②铝 ③Na2O ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)其中,属于混合物的是_________ ,属于氧化物的是__________ ,属于单质的是____ 。(本小题均用序号作答)
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH- H2O,该离子反应对应的化学方程式为
H2O,该离子反应对应的化学方程式为____________________________________________________ 。
II.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。

(1)从物质分类标准看,“铜绿”属于________ (填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:_____________ 。
(3)请写出铜绿与盐酸反应的化学方程式:_______________________ 。
(4)上述转化过程中属于化合反应的是_____________ ,属于置换反应的是____________ 。
(1)其中,属于混合物的是
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-
 H2O,该离子反应对应的化学方程式为
H2O,该离子反应对应的化学方程式为II.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。

(1)从物质分类标准看,“铜绿”属于
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:
(3)请写出铜绿与盐酸反应的化学方程式:
(4)上述转化过程中属于化合反应的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学工业中会产生大量含铬废水。需进行无害化处理检测达标后才能排放。
(1) 工业常用NaHSO3还原法处理,方法如下:向酸性废水中加入NaHSO3使Cr2O72-还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
写出NaHSO3与Cr2O72-反应的离子方程式:_______________________ 。
(2) 废水中铬元素总浓度的测定方法如下:向一定量含Cr2O72-和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O72-与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下: 。
。
①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会____ (填“偏大”、“偏小”或“不变”)。
②以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点时的现象为________ 。
③准确移取含Cr2O72-和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000 mol·L-1Na2S2O3标准溶液13.50 mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)__________ 。
(1) 工业常用NaHSO3还原法处理,方法如下:向酸性废水中加入NaHSO3使Cr2O72-还原成为Cr3+,然后加入熟石灰调节废水的pH,使Cr3+完全沉淀。
写出NaHSO3与Cr2O72-反应的离子方程式:
(2) 废水中铬元素总浓度的测定方法如下:向一定量含Cr2O72-和Cr3+的酸性废水样中加入足量(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;再加入过量的KI溶液,Cr2O72-与I-完全反应生成Cr3+和I2后,以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。测定过程中物质的转化关系如下:
 。
。①上述操作过程中,若无煮沸操作,则测定的铬元素总浓度会
②以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点时的现象为
③准确移取含Cr2O72-和Cr3+的酸性废水样100.00 mL,按上述方法测定废水样中铬元素总浓度,消耗0.01000 mol·L-1Na2S2O3标准溶液13.50 mL。计算该废水中铬元素总浓度(以mg·L-1表示)(写出计算过程)
您最近一年使用:0次

 溶液加入硫酸锌溶液中反应,在实际生产中得到的是一种碱式碳酸锌
溶液加入硫酸锌溶液中反应,在实际生产中得到的是一种碱式碳酸锌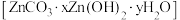 ,取该样品
,取该样品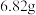 ,充分灼烧后测得残留物质量为
,充分灼烧后测得残留物质量为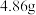 ,将所得气体通入足量澄清石灰水中,得到
,将所得气体通入足量澄清石灰水中,得到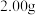 沉淀,则此碱式碳酸锌的化学式是
沉淀,则此碱式碳酸锌的化学式是

