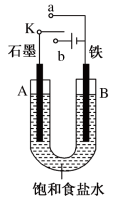
利用离子浓度差也可以设计成原电池,即“浓差电池”,其总反应是一个体系的物理状态的变化。如
类型 | 原理图及信息 | 电极反应式 |
浓差电池 |
闭合开关K后,电子由溶液浓度小的一极流出 | 负极: 正极: |
2023高三·全国·专题练习 查看更多[1]
(已下线)考向3 特殊电化学装置探究
更新时间:2023-02-13 13:18:26
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】某化学兴趣小组同学设计如图装置:
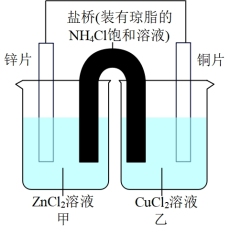
回答下列问题:
(1)正极的电极反应式为______________ 。
(2)盐桥的作用是向甲、乙两烧杯中提供Cl-和NH4+,使两烧杯中的溶液保持电荷守恒,反应过程中Cl-进入_________ (填“甲”或“乙”)烧杯。
(3)该电池反应离子方程式为__________________ 。

回答下列问题:
(1)正极的电极反应式为
(2)盐桥的作用是向甲、乙两烧杯中提供Cl-和NH4+,使两烧杯中的溶液保持电荷守恒,反应过程中Cl-进入
(3)该电池反应离子方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】化学电源与我们的生活密切相关,回答下列问题:
(1)在铜锌原电池中,以硫酸为电解质溶液,铜电极反应式为_______ 。
(2)若将电解质溶液换成硫酸铜,如图所示,则铜为_______ 极,电极上发生的是_______ (填“氧化”或“还原”)反应,铜电极反应式是_______ ;向锌电极移动的离子为_______ 。随着实验地进行,溶液质量_______ (填增加、减小或不变),若溶液质量变化2g,则转移的电子数为_______ (NA表示阿伏伽德罗的数值)。
(1)在铜锌原电池中,以硫酸为电解质溶液,铜电极反应式为
(2)若将电解质溶液换成硫酸铜,如图所示,则铜为

您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)已知FeCl3在反应中得到电子,则该反应的还原剂是__________ 。
(2)将上述反应设计成的原电池如图所示,请回答下列问题:
①电解质溶液X是_____ ;
②Cu电极上发生的电极反应式为_____ ;
③原电池工作时,盐桥中的___ 离子(填“K+”或“Cl—”)不断进入X溶液中。
(1)已知FeCl3在反应中得到电子,则该反应的还原剂是
(2)将上述反应设计成的原电池如图所示,请回答下列问题:
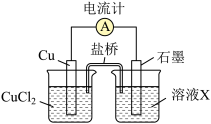
①电解质溶液X是
②Cu电极上发生的电极反应式为
③原电池工作时,盐桥中的
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,电池总反应为4Al+3O2+6H2O=4Al(OH)3。可用作灯塔所需的电池。已知:海水呈弱碱性。
(1)铝板在该电池中作______ 极,电极反应式为_______ 。
(2)铂电极作_______ 极,电极反应式为_______ 。
(1)铝板在该电池中作
(2)铂电极作
您最近一年使用:0次

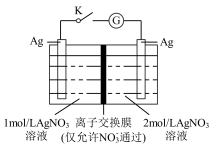
 )常用于生产锂离子电池,请回答下列问题:
)常用于生产锂离子电池,请回答下列问题: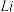 以阳离子的形式脱离
以阳离子的形式脱离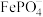 本身会转变为一种电中性化合物,该化合物的化学式为
本身会转变为一种电中性化合物,该化合物的化学式为