某无色溶液,其中可能存在的离子有:Na+、Ag+、Ba2+、Fe3+、Al3+、AlO2-、S2-、SO32-、CO32-、SO42-,现取该溶液进行实验,实验结果如下:
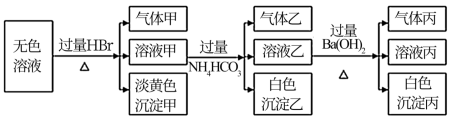
试回答下列问题:
(1)生成沉淀甲的离子方程式为:____________ 。
(2)生成气体丙和沉淀丙的离子方程式为_________ 。
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表
(4)综上所述,该溶液肯定存在的离子有:_________ 。
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是_________ 。

试回答下列问题:
(1)生成沉淀甲的离子方程式为:
(2)生成气体丙和沉淀丙的离子方程式为
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入下表
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | 检验CO2 | 澄清石灰水 | 溶液变浑浊 |
(4)综上所述,该溶液肯定存在的离子有:
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是
更新时间:2019-08-29 16:26:26
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
【推荐1】某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:

(1)“酸浸”过程中主要反应的离子方程式为:
_______________________ 、__________________________________________ 。
(2)“酸浸”时,提高浸出速率的具体措施有_________________________ 。(写出两个)
(3)“碱溶”的目的是___________________________________________________ 。
物质X的电子式为_________________ 。该工艺设计中,过量X参与反应的离子方程式是:_________________________________________________________________ 。
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为:_________________________________ 。

(1)“酸浸”过程中主要反应的离子方程式为:
(2)“酸浸”时,提高浸出速率的具体措施有
(3)“碱溶”的目的是
物质X的电子式为
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】某混合溶液M中大量含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中5种浓度相等的离子。若向M溶液中加入过量0.1mol/L的HBr溶液,有无色气体N产生,但反应前后阴离子种类不发生改变。回答下列问题:
中5种浓度相等的离子。若向M溶液中加入过量0.1mol/L的HBr溶液,有无色气体N产生,但反应前后阴离子种类不发生改变。回答下列问题:
(1)在实验室中,用1mol/L的HBr溶液配制500mL 0.1mol/L的HBr溶液时,需要的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需要_______ 。
(2)M溶液中含有的5种离子分别为____ 、_____ 、____ 、_____ 、_____ 。
(3)生成无色气体N的离子方程式为_______ ,实验室中制备N气体常用的药品为_______ 。
(4)若向M溶液中加入过量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中5种浓度相等的离子。若向M溶液中加入过量0.1mol/L的HBr溶液,有无色气体N产生,但反应前后阴离子种类不发生改变。回答下列问题:
中5种浓度相等的离子。若向M溶液中加入过量0.1mol/L的HBr溶液,有无色气体N产生,但反应前后阴离子种类不发生改变。回答下列问题:(1)在实验室中,用1mol/L的HBr溶液配制500mL 0.1mol/L的HBr溶液时,需要的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需要
(2)M溶液中含有的5种离子分别为
(3)生成无色气体N的离子方程式为
(4)若向M溶液中加入过量的
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】有一澄清透明的溶液,可能大量存在有NH4+、Fe3+、H+、Mg2+、A13+、I-、CO32-等离子。现分别取溶液进行下列实验:
(1)加入淀粉溶液,未见蓝色。
(2)加入少量AgNO3溶液有黄色沉淀和气体生成。
(3)逐滴加入1mol·L-1NaOH溶液,随着NaOH溶液的滴入,产生沉淀的量如图所示。

试确定:溶液中一定不存在的离子有________ ,其中阴离子物质的量为_________ ,加入少量AgNO3溶液的离子反应方程式为________________ 。
(1)加入淀粉溶液,未见蓝色。
(2)加入少量AgNO3溶液有黄色沉淀和气体生成。
(3)逐滴加入1mol·L-1NaOH溶液,随着NaOH溶液的滴入,产生沉淀的量如图所示。

试确定:溶液中一定不存在的离子有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】定性分析溶液中的微粒组成是化学科学研究的前提和重要方面。请你根据所学知识对以下溶液做出定性的判断。
(1)某无色溶液含有下列离子中的若干种:H+、NH4+、Fe2+、Ba2+、Al3+、CO32–、Cl–、OH–、NO3–。若该溶液显酸性,则溶液中能大量共存的离子最多有_____ 种;若溶液显碱性,则溶液中能大量共存的离子最多有_____ 种。
(2)某溶液由Na+、Cu2+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的若干种离子组成。取适量该溶液进行如下实验:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②向①所得的溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③向②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
则原溶液中可能存在的离子是_____ ;一定存在的离子是__________________________ 。
(1)某无色溶液含有下列离子中的若干种:H+、NH4+、Fe2+、Ba2+、Al3+、CO32–、Cl–、OH–、NO3–。若该溶液显酸性,则溶液中能大量共存的离子最多有
(2)某溶液由Na+、Cu2+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的若干种离子组成。取适量该溶液进行如下实验:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②向①所得的溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③向②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
则原溶液中可能存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】现有 某溶液中可能含有
某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,现将此溶液分成三等份,进行如下实验:
中的若干种,现将此溶液分成三等份,进行如下实验:
①向第一份中加入 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;
②向第二份中加足量 溶液并加热,收集到气体
溶液并加热,收集到气体 (标准状况);
(标准状况);
③向第三份中加足量 溶液,得到沉淀
溶液,得到沉淀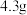 ,加入足量盐酸充分反应后,沉淀剩余
,加入足量盐酸充分反应后,沉淀剩余 。
。
根据上述实验,回答下列问题:
(1)实验③中生成沉淀的离子方程式为___________ ,沉淀溶解的离子方程式为________ 。
(2)溶液中一定不存在的离子有___________ 。
(3)实验①中加入 溶液,有白色沉淀产生,能否说明原溶液中含有
溶液,有白色沉淀产生,能否说明原溶液中含有 ?
?___________ (填“能”或“否”),理由是___________ 。
(4)推断 是否存在
是否存在___________ (填“是”或“否”),若存在,计算其物质的量浓度:___________ (若不存在,此问不作答)
 某溶液中可能含有
某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,现将此溶液分成三等份,进行如下实验:
中的若干种,现将此溶液分成三等份,进行如下实验:①向第一份中加入
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;②向第二份中加足量
 溶液并加热,收集到气体
溶液并加热,收集到气体 (标准状况);
(标准状况);③向第三份中加足量
 溶液,得到沉淀
溶液,得到沉淀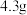 ,加入足量盐酸充分反应后,沉淀剩余
,加入足量盐酸充分反应后,沉淀剩余 。
。根据上述实验,回答下列问题:
(1)实验③中生成沉淀的离子方程式为
(2)溶液中一定不存在的离子有
(3)实验①中加入
 溶液,有白色沉淀产生,能否说明原溶液中含有
溶液,有白色沉淀产生,能否说明原溶液中含有 ?
?(4)推断
 是否存在
是否存在
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】化合物A由4种元素组成,实验如下:
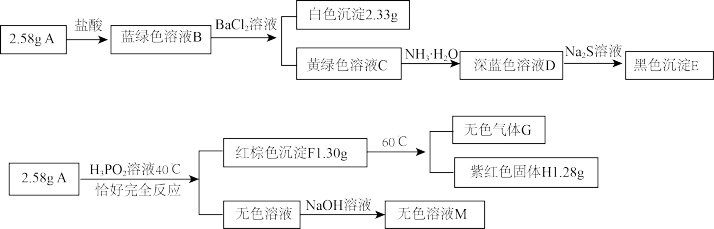
已知:除说明外,加入试剂均为足量;生成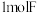 时消耗
时消耗 的
的
回答下列问题:
(1) 的分子式为
的分子式为_______ , 的化学式为
的化学式为_______ 。
(2)溶液B中溶质成分是_______ (用化学式表示),根据 的现象,给出相应微粒与阳离子结合由强到弱的排序
的现象,给出相应微粒与阳离子结合由强到弱的排序_______ 。
(3)写出 与
与 反应的化学方程式
反应的化学方程式_______ 。
(4)检验溶液 的主要阴离子(任选2种)
的主要阴离子(任选2种)_______ 。

已知:除说明外,加入试剂均为足量;生成
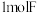 时消耗
时消耗 的
的
回答下列问题:
(1)
 的分子式为
的分子式为 的化学式为
的化学式为(2)溶液B中溶质成分是
 的现象,给出相应微粒与阳离子结合由强到弱的排序
的现象,给出相应微粒与阳离子结合由强到弱的排序(3)写出
 与
与 反应的化学方程式
反应的化学方程式(4)检验溶液
 的主要阴离子(任选2种)
的主要阴离子(任选2种)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:
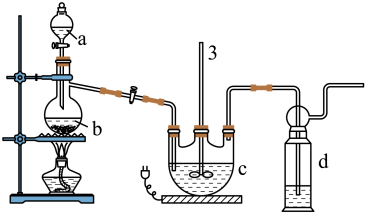
(1)仪器a的名称是_______ ,仪器b的名称是_______ 。b中利用质量分数为70%〜80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______ 。c中试剂为_______
(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______ (填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______ mol∙L-1
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:

(1)仪器a的名称是
(2)实验中要控制SO2的生成速率,可以采取的措施有
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)
| 装置 | 试剂X | 实验现象 |
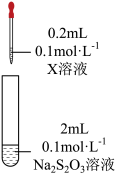 | Fe2(SO4)3溶液 | 混合后溶液先变成紫黑色,30s后几乎变为无色 |
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质,其体实验流程如下:
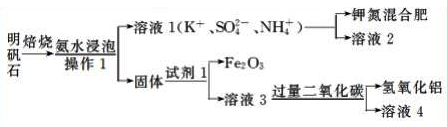
请回答下列问题:
(1)明矾石焙烧后用稀氨水浸出。需用到480mL稀氨水(每升含有39g氨), 则需取浓氨水(每升含有210g氨)_____ mL来配制(数值取整数),用规格为____ 量筒量取。操作l所用到的玻璃仪器的名称是______ 。
(2)写出上图“固体”中所有物质的化学式_____ 。
(3)由溶液3制取氢氧化铝的离子方程式为_______ 。
(4)请你写出验证溶液l中有K+的实验操作:________ 。
(5)为测定混合肥料K2S04、(NH4)2SO4中钾的含量,完成下列步骤:
①称取钾氮肥试样并溶于水,加入足量____ 溶液,产生白色沉淀。
②过滤、洗涤、干燥。其中,洗涤沉淀的操作方法为________ 。
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol, 则试样中K2S04的物质的量为:_____ mol(用含m 、n 的代数式表示)。
(7)实验室用Fe203与CO反应来制取单质Fe。
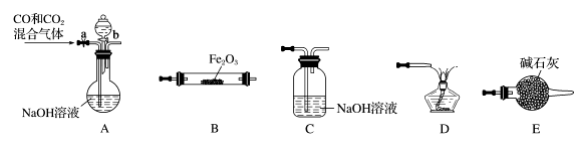
①请按气流由左到右的方向连接下列各装置,顺序为A→____ →____ →____ →_____ 。
②检查装置A气密性的方法是_____ 。
③在点燃B处的酒精灯前,应进行的操作是______ 。
④装置C的作用是_____________ 。

请回答下列问题:
(1)明矾石焙烧后用稀氨水浸出。需用到480mL稀氨水(每升含有39g氨), 则需取浓氨水(每升含有210g氨)
(2)写出上图“固体”中所有物质的化学式
(3)由溶液3制取氢氧化铝的离子方程式为
(4)请你写出验证溶液l中有K+的实验操作:
(5)为测定混合肥料K2S04、(NH4)2SO4中钾的含量,完成下列步骤:
①称取钾氮肥试样并溶于水,加入足量
②过滤、洗涤、干燥。其中,洗涤沉淀的操作方法为
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol, 则试样中K2S04的物质的量为:
(7)实验室用Fe203与CO反应来制取单质Fe。

①请按气流由左到右的方向连接下列各装置,顺序为A→
②检查装置A气密性的方法是
③在点燃B处的酒精灯前,应进行的操作是
④装置C的作用是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】有一瓶澄清的溶液,其中可能含有NH4+、Na+、Ba2+、Al3+、Fe3+、I-、NO3-、CO32-、SO42-、AlO2-,取该溶液进行以下实验:
(1) 取pH试纸检验,溶液呈强酸性,可以排除_______________ 离子的存在。
(2) 取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色,可以排除___________ 离子的存在。
(3) 写出(2)所发生的反应的离子方程式__________________ 。
(4) 另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,则又可以排除______________ 离子的存在。
(5) 取出(4)部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明_____ 离子存在,又可排除_______ 离子的存在。
(6) 将(4)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。根据上述实验事实确定:该溶液中肯定存在的离子是__________ 肯定不存在的离子是_________________ ,还不能确定是否存在的离子是_______ ,鉴别的方法是_____________ (具体的操作方法)。
(1) 取pH试纸检验,溶液呈强酸性,可以排除
(2) 取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色,可以排除
(3) 写出(2)所发生的反应的离子方程式
(4) 另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,则又可以排除
(5) 取出(4)部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明
(6) 将(4)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。根据上述实验事实确定:该溶液中肯定存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】根据要求,回答下列问题:
I.某溶液由Na+、Al3+、Fe3+、NH 、Cl-、NO
、Cl-、NO 、CO
、CO 、SO
、SO 中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
步骤i:加入过量NaOH溶液,加热,产生气体和沉淀;
步骤ii:过滤,得滤液、滤渣;
步骤iii:取滤渣,洗涤、灼烧,得固体W;
步骤iv:取少量滤液,加入足量BaCl2溶液,产生白色沉淀。
(1)步骤iii所得固体W为________ (填化学式)。
(2)原溶液中一定存在的离子是_______ ,原溶液中一定不存在的离子是_______ 。
Ⅱ.Cr、Ca、O可形成一种具有特殊导电性的晶体(化学式为CaxCrOy,x、y为整数),其立方晶胞如图所示,Ca与O最小间距大于Cr与O最小间距。
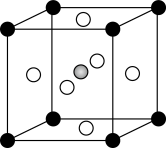
(3)Cr在晶胞中的位置为________ (填“顶点”“面心”或“体心”)。晶体中1个Ca周围与其最近的O的个数为_______ 。若Ca与O最小间距为apm,阿伏加德罗常数为NA,则该晶体的密度为________ g•cm-3(列出计算式)。
I.某溶液由Na+、Al3+、Fe3+、NH
 、Cl-、NO
、Cl-、NO 、CO
、CO 、SO
、SO 中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。步骤i:加入过量NaOH溶液,加热,产生气体和沉淀;
步骤ii:过滤,得滤液、滤渣;
步骤iii:取滤渣,洗涤、灼烧,得固体W;
步骤iv:取少量滤液,加入足量BaCl2溶液,产生白色沉淀。
(1)步骤iii所得固体W为
(2)原溶液中一定存在的离子是
Ⅱ.Cr、Ca、O可形成一种具有特殊导电性的晶体(化学式为CaxCrOy,x、y为整数),其立方晶胞如图所示,Ca与O最小间距大于Cr与O最小间距。

(3)Cr在晶胞中的位置为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质,其体实验流程如下:

请回答下列问题:
(1)明矾石焙烧后用稀氨水浸出。需用到480mL稀氨水(每升含有39g氨), 则需取浓氨水(每升含有210g氨)_____ mL来配制(数值取整数),用规格为____ 量筒量取。操作l所用到的玻璃仪器的名称是______ 。
(2)写出上图“固体”中所有物质的化学式_____ 。
(3)由溶液3制取氢氧化铝的离子方程式为_______ 。
(4)请你写出验证溶液l中有K+的实验操作:________ 。
(5)为测定混合肥料K2S04、(NH4)2SO4中钾的含量,完成下列步骤:
①称取钾氮肥试样并溶于水,加入足量____ 溶液,产生白色沉淀。
②过滤、洗涤、干燥。其中,洗涤沉淀的操作方法为________ 。
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol, 则试样中K2S04的物质的量为:_____ mol(用含m 、n 的代数式表示)。
(7)实验室用Fe203与CO反应来制取单质Fe。

①请按气流由左到右的方向连接下列各装置,顺序为A→____ →____ →____ →_____ 。
②检查装置A气密性的方法是_____ 。
③在点燃B处的酒精灯前,应进行的操作是______ 。
④装置C的作用是_____________ 。

请回答下列问题:
(1)明矾石焙烧后用稀氨水浸出。需用到480mL稀氨水(每升含有39g氨), 则需取浓氨水(每升含有210g氨)
(2)写出上图“固体”中所有物质的化学式
(3)由溶液3制取氢氧化铝的离子方程式为
(4)请你写出验证溶液l中有K+的实验操作:
(5)为测定混合肥料K2S04、(NH4)2SO4中钾的含量,完成下列步骤:
①称取钾氮肥试样并溶于水,加入足量
②过滤、洗涤、干燥。其中,洗涤沉淀的操作方法为
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol, 则试样中K2S04的物质的量为:
(7)实验室用Fe203与CO反应来制取单质Fe。

①请按气流由左到右的方向连接下列各装置,顺序为A→
②检查装置A气密性的方法是
③在点燃B处的酒精灯前,应进行的操作是
④装置C的作用是
您最近一年使用:0次




