硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:
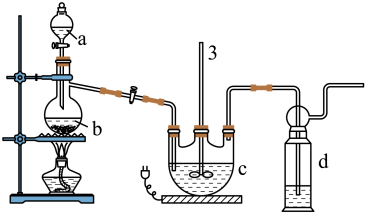
(1)仪器a的名称是_______ ,仪器b的名称是_______ 。b中利用质量分数为70%〜80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______ 。c中试剂为_______
(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______ (填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______ mol∙L-1
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:

(1)仪器a的名称是
(2)实验中要控制SO2的生成速率,可以采取的措施有
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)
| 装置 | 试剂X | 实验现象 |
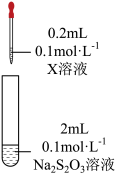 | Fe2(SO4)3溶液 | 混合后溶液先变成紫黑色,30s后几乎变为无色 |
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为
更新时间:2020-04-20 22:16:49
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】硼氢化钠(NaBH4)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33 ℃)。工业上可用硼镁矿(主要成分为Mg2B2O5·H2O,含少量杂质Fe3O4)制取NaBH4,其工艺流程如下:
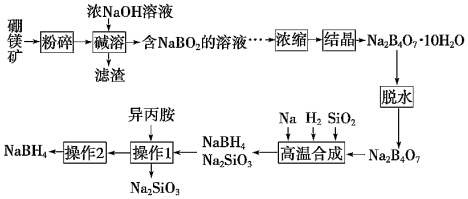
回答下列问题:
(1)NaBH4的电子式为________ 。
(2)碱溶时Mg2B2O5发生反应的化学方程式是________ 。
(3)滤渣的成分是________ 。
(4)高温合成中,加料之前需将反应器加热至100 ℃以上并通入氩气,该操作的目的是____________________ ,原料中的金属钠通常保存在________ 中,实验室取用少量金属钠用到的实验用品有________ 、玻璃片和小刀。
(5)操作2的名称为________ 。流程中可循环利用的物质是________ 。
(6)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1gNaBH4的还原能力相当于________ g H2的还原能力(B元素化合价不变,氧化产物中氢元素化合价相同,计算结果保留两位小数)。

回答下列问题:
(1)NaBH4的电子式为
(2)碱溶时Mg2B2O5发生反应的化学方程式是
(3)滤渣的成分是
(4)高温合成中,加料之前需将反应器加热至100 ℃以上并通入氩气,该操作的目的是
(5)操作2的名称为
(6)NaBH4常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1gNaBH4的还原能力相当于
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】稀土元素被誉为“现代工业的维生素”和“21世纪新材料宝库”,广泛应用于新材料、冶金化工、电子信息、节能环保等领域,由普通级氯化镧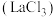 料液制备高纯氧化铜
料液制备高纯氧化铜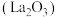 的新工艺流程如图所示。
的新工艺流程如图所示。 太高,EDTA和
太高,EDTA和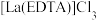 会结晶沉淀。
会结晶沉淀。
回答下列问题:
(1)普通级氯化镧料液中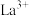 通过树脂
通过树脂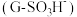 时,在树脂吸附柱上发生反应生成
时,在树脂吸附柱上发生反应生成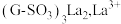 被吸附在树脂内部,反应的离子方程式为
被吸附在树脂内部,反应的离子方程式为________ 。
(2)经氨水处理过的淋洗液,再经 淋洗,发生反应
淋洗,发生反应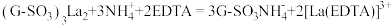 ,淋洗液的
,淋洗液的 对分离效率的影响如图所示。则淋洗时,淋洗液的
对分离效率的影响如图所示。则淋洗时,淋洗液的 应调到
应调到
__________ 。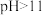 时,分离效率就迅速下降,原因是
时,分离效率就迅速下降,原因是____________ 。
(4)用草酸溶液将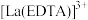 中的
中的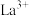 沉淀出来,最后进行高温焙烧。在空气中高温焙烧
沉淀出来,最后进行高温焙烧。在空气中高温焙烧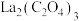 ,若空气中氧气的体积分数为
,若空气中氧气的体积分数为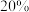 ,则消耗的空气与高温焙烧生成的
,则消耗的空气与高温焙烧生成的 的物质的量之比为
的物质的量之比为__________ 。
(5)锶镧铜氧化物超导体的晶胞结构(底面是正方形的长方体)如图所示,晶胞中锶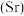 原子与镧
原子与镧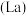 原子的个数比为
原子的个数比为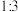 ,体心与顶点的
,体心与顶点的 原子有着相同的化学环境,
原子有着相同的化学环境, 原子1的分数坐标为
原子1的分数坐标为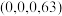 。则该超导体的化学式为
。则该超导体的化学式为__________ ,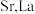 原子2的分数坐标为
原子2的分数坐标为__________ ,体心 原子与
原子与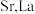 原子之间的最近距离为
原子之间的最近距离为__________  (列出含a、c的计算式)。
(列出含a、c的计算式)。
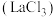 料液制备高纯氧化铜
料液制备高纯氧化铜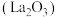 的新工艺流程如图所示。
的新工艺流程如图所示。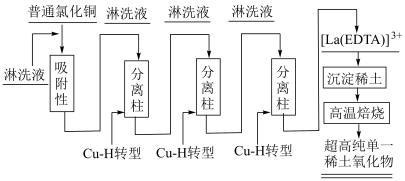
 太高,EDTA和
太高,EDTA和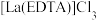 会结晶沉淀。
会结晶沉淀。回答下列问题:
(1)普通级氯化镧料液中
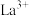 通过树脂
通过树脂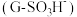 时,在树脂吸附柱上发生反应生成
时,在树脂吸附柱上发生反应生成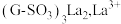 被吸附在树脂内部,反应的离子方程式为
被吸附在树脂内部,反应的离子方程式为(2)经氨水处理过的淋洗液,再经
 淋洗,发生反应
淋洗,发生反应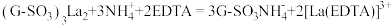 ,淋洗液的
,淋洗液的 对分离效率的影响如图所示。则淋洗时,淋洗液的
对分离效率的影响如图所示。则淋洗时,淋洗液的 应调到
应调到

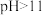 时,分离效率就迅速下降,原因是
时,分离效率就迅速下降,原因是(4)用草酸溶液将
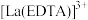 中的
中的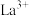 沉淀出来,最后进行高温焙烧。在空气中高温焙烧
沉淀出来,最后进行高温焙烧。在空气中高温焙烧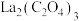 ,若空气中氧气的体积分数为
,若空气中氧气的体积分数为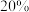 ,则消耗的空气与高温焙烧生成的
,则消耗的空气与高温焙烧生成的 的物质的量之比为
的物质的量之比为(5)锶镧铜氧化物超导体的晶胞结构(底面是正方形的长方体)如图所示,晶胞中锶
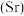 原子与镧
原子与镧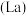 原子的个数比为
原子的个数比为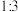 ,体心与顶点的
,体心与顶点的 原子有着相同的化学环境,
原子有着相同的化学环境, 原子1的分数坐标为
原子1的分数坐标为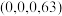 。则该超导体的化学式为
。则该超导体的化学式为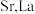 原子2的分数坐标为
原子2的分数坐标为 原子与
原子与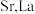 原子之间的最近距离为
原子之间的最近距离为 (列出含a、c的计算式)。
(列出含a、c的计算式)。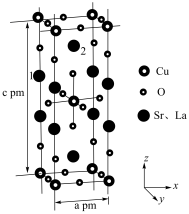
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】磷酸亚铁锂( )是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为
)是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为 ,含有少量
,含有少量 等杂质)制备
等杂质)制备 的工艺流程如图所示。
的工艺流程如图所示。
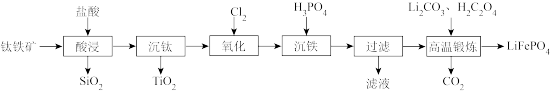
回答下列问题:
(1)反应过程中 的化合价没有发生变化,则
的化合价没有发生变化,则 中
中 元素的化合价为
元素的化合价为_______ 。
(2)实验室中进行过滤操作需要用到的玻璃仪器有烧杯、_______ 。
(3)氧化时发生反应的离子方程式为_______ ;滤液中溶质的主要为_______ (填化学式)。
(4)高温煅烧时发生反应的化学方程式为_______ 。
(5)理论上反应过程中消耗 和
和 的物质的量之比为
的物质的量之比为_______ 。
 )是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为
)是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为 ,含有少量
,含有少量 等杂质)制备
等杂质)制备 的工艺流程如图所示。
的工艺流程如图所示。
回答下列问题:
(1)反应过程中
 的化合价没有发生变化,则
的化合价没有发生变化,则 中
中 元素的化合价为
元素的化合价为(2)实验室中进行过滤操作需要用到的玻璃仪器有烧杯、
(3)氧化时发生反应的离子方程式为
(4)高温煅烧时发生反应的化学方程式为
(5)理论上反应过程中消耗
 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】锂和铍是重要的稀有金属元素,被国内外视为战略资源。一种从尾矿(主要含BeO、Li2O、SiO2及Fe、Al元素)中提取锂、铍的工艺如图:
②Li+可与FeCl 结合成LiFeCl4的形式被TBP萃取;
结合成LiFeCl4的形式被TBP萃取;
③HC1+FeCl3 HFeCl4(易溶于有机溶剂);
HFeCl4(易溶于有机溶剂);
④Ksp[Fe(OH)3]=1×10-38。
(1)“酸浸”时BeO发生反应的化学方程式为_______ 。
(2)“氧化”时,温度不宜过低,也不宝过高的原因是_______ 。
(3)“氧化”后溶液中c(Fe3+)浓度为0.01mol/L,“沉铁”时为了防止生成Fe(OH)3沉淀,pH值最好不大于______ ,“沉铁”后的pH______ (填"变大”、“变小”或“不变”)。
(4)“萃取”步骤中,以TBP为萃取剂,FeCl3为萃取剂,还需要加入NH4C1的作用是______ 。
(5)“反萃取”步骤中,加入的反萃取剂最好是________ 。
(6)“操作X”包括的步骤为_______ 、_______ 。

②Li+可与FeCl
 结合成LiFeCl4的形式被TBP萃取;
结合成LiFeCl4的形式被TBP萃取;③HC1+FeCl3
 HFeCl4(易溶于有机溶剂);
HFeCl4(易溶于有机溶剂);④Ksp[Fe(OH)3]=1×10-38。
(1)“酸浸”时BeO发生反应的化学方程式为
(2)“氧化”时,温度不宜过低,也不宝过高的原因是
(3)“氧化”后溶液中c(Fe3+)浓度为0.01mol/L,“沉铁”时为了防止生成Fe(OH)3沉淀,pH值最好不大于
(4)“萃取”步骤中,以TBP为萃取剂,FeCl3为萃取剂,还需要加入NH4C1的作用是
(5)“反萃取”步骤中,加入的反萃取剂最好是
(6)“操作X”包括的步骤为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某实验小组欲制取氧化铜并证明其能加快氯酸钾的分解,进行如下实验:
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液。直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是__________ (填实验序号),步骤①、③中研磨固体所用仪器的名称是____________ 。
(2)步骤③中洗涤沉淀的操作是__________ 。
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
回答下列问题:
(3)上述实验中的“待测数据”指________ 。
(4)若要证明实验中产生的气体是O2,可用小试管收集气体,后续操作为_____ 。
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a.__________ 。
b. CuO的化学性质有没有改变。
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液。直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是
(2)步骤③中洗涤沉淀的操作是
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
实验序号 | KClO3质量 | 其他物质的质量 | 待测数据 |
④ | 1.2g | 无其他物质 | |
⑤ | 1.2g | CuO 0.5g | |
⑥ | 1.2g | MnO2 0.5g |
(3)上述实验中的“待测数据”指
(4)若要证明实验中产生的气体是O2,可用小试管收集气体,后续操作为
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a.
b. CuO的化学性质有没有改变。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】乙炔亚铜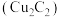 是一种难溶于水的暗红色固体,是一种对热和冲击敏感的高爆炸药。某研究性学习小组利用电石(含少量
是一种难溶于水的暗红色固体,是一种对热和冲击敏感的高爆炸药。某研究性学习小组利用电石(含少量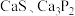 )通过如图实验装置制备少量
)通过如图实验装置制备少量 :
: 的原理为
的原理为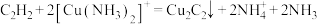 ;
;
② 在水溶液中为无色离子。
在水溶液中为无色离子。
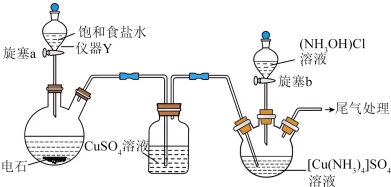
(1)仪器 的名称为
的名称为___________ ;装置组装后,首先进行的操作是___________ 。
(2) 溶液的作用是
溶液的作用是___________ 。
(3)实验进行过程中先打开旋塞___________ ,待观察到___________ 的现象时,再打开旋塞___________ 。逸出的尾气中含有 ,三口烧瓶中
,三口烧瓶中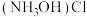 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)有同学提出 可能会影响
可能会影响 的生成速率。为证实该设想设计下表实验
的生成速率。为证实该设想设计下表实验
①通过实验Ⅰ和Ⅱ说明 越小,
越小, 的生成速率越慢,则
的生成速率越慢,则 和
和 的关系是
的关系是___________ 。
②实验测得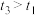 ,其可能原因是
,其可能原因是___________ 。
③实验Ⅳ中 选用
选用___________ (填化学式)进行实验,可能可以说明 越大,
越大, 的生成速率越快。
的生成速率越快。
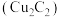 是一种难溶于水的暗红色固体,是一种对热和冲击敏感的高爆炸药。某研究性学习小组利用电石(含少量
是一种难溶于水的暗红色固体,是一种对热和冲击敏感的高爆炸药。某研究性学习小组利用电石(含少量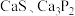 )通过如图实验装置制备少量
)通过如图实验装置制备少量 :
:
 的原理为
的原理为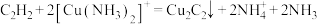 ;
;②
 在水溶液中为无色离子。
在水溶液中为无色离子。(1)仪器
 的名称为
的名称为(2)
 溶液的作用是
溶液的作用是(3)实验进行过程中先打开旋塞
 ,三口烧瓶中
,三口烧瓶中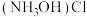 发生反应的离子方程式为
发生反应的离子方程式为(4)有同学提出
 可能会影响
可能会影响 的生成速率。为证实该设想设计下表实验
的生成速率。为证实该设想设计下表实验| 实验序号 | 与电石反应的试剂 | 收集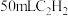 所需时间 所需时间 |
| Ⅰ | 蒸馏水 |  |
| Ⅱ |  氢氧化钠溶液 氢氧化钠溶液 |  |
| Ⅲ | 硫酸溶液( 稀释) 稀释) |  |
| Ⅳ | X | 待测 |
 越小,
越小, 的生成速率越慢,则
的生成速率越慢,则 和
和 的关系是
的关系是②实验测得
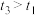 ,其可能原因是
,其可能原因是③实验Ⅳ中
 选用
选用 越大,
越大, 的生成速率越快。
的生成速率越快。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】乙酸乙酯是一种重要的化工原料,广泛用于药物染料等工业。某兴趣小组同学欲制备乙酸乙酯并对所得产物进行探究,实验装置如图所示:
Ⅰ.乙酸乙酯的制备,实验装置如图所示:

(1)为了防止加热时液体暴沸,需要在试管A中加入___________ 。
(2)导管末端不伸入饱和碳酸钠溶液中的原因是___________ 。
(3)饱和 溶液作用是___________(填选项)
溶液作用是___________(填选项)
Ⅱ.产物的探究
(4)实验过程中,试管A中混合溶液变黑,将反应产生的蒸汽直接通入酸性 溶液中,溶液褪色。针对酸性
溶液中,溶液褪色。针对酸性 溶液褪色现象,甲同学认为反应产生的蒸汽中含有
溶液褪色现象,甲同学认为反应产生的蒸汽中含有 气体,使酸性
气体,使酸性 溶液褪色。乙同学认为褪色还可能是因为
溶液褪色。乙同学认为褪色还可能是因为___________ 。
(5)取下试管B振荡,红色褪去。为了探究褪色原因,进行如下实验。
①用化学方程式解释实验Ⅰ中产生气泡的原因是___________ 。
②测得实验Ⅰ褪色后的下层溶液呈碱性,对比实验Ⅰ和实验Ⅱ,小组得出该实验中乙酸与碳酸钠反应___________ (填“是”或“不是”)溶液褪色的主要原因。
③针对实验Ⅱ中现象,小组同学提出猜想:酚酞更易溶于乙酸乙酯。实验Ⅲ中观察到___________ ,证实猜想正确。
Ⅰ.乙酸乙酯的制备,实验装置如图所示:

(1)为了防止加热时液体暴沸,需要在试管A中加入
(2)导管末端不伸入饱和碳酸钠溶液中的原因是
(3)饱和
 溶液作用是___________(填选项)
溶液作用是___________(填选项)| A.反应乙酸和乙醇 |
| B.反应乙酸并溶解部分乙醇 |
C.乙酸乙酯在饱和 溶液中的溶解度比在水中的小,有利于分层析出 溶液中的溶解度比在水中的小,有利于分层析出 |
| D.加快酯的生成速率,提高其产率 |
Ⅱ.产物的探究
(4)实验过程中,试管A中混合溶液变黑,将反应产生的蒸汽直接通入酸性
 溶液中,溶液褪色。针对酸性
溶液中,溶液褪色。针对酸性 溶液褪色现象,甲同学认为反应产生的蒸汽中含有
溶液褪色现象,甲同学认为反应产生的蒸汽中含有 气体,使酸性
气体,使酸性 溶液褪色。乙同学认为褪色还可能是因为
溶液褪色。乙同学认为褪色还可能是因为(5)取下试管B振荡,红色褪去。为了探究褪色原因,进行如下实验。
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 |  |  |  |
| 操作 | 充分振荡、静置 | 充分振荡、静置 | 充分振荡、静置、分液。取下层溶液,加入饱和 溶液 溶液 |
| 现象 | 上层液体变薄,冒气泡,下层溶液红色褪去 | 上层液体不变薄,无气泡,下层溶液红色褪去 | ___________ |
②测得实验Ⅰ褪色后的下层溶液呈碱性,对比实验Ⅰ和实验Ⅱ,小组得出该实验中乙酸与碳酸钠反应
③针对实验Ⅱ中现象,小组同学提出猜想:酚酞更易溶于乙酸乙酯。实验Ⅲ中观察到
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某学习小组探究溴乙烷的消去反应并验证产物。

实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)实验原理:__________________________________ 。
(2)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因:_________________________ 。
(3)丙同学认为只要对实验装置进行适当改进,即可避免对乙烯气体检验的干扰,改进方法:______________________________________________________ 。
改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显。该小组再次查阅资料,对实验进行进一步的改进。
资料一:溴乙烷于55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%。
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快。
资料三:溴乙烷的沸点:38.2℃。
(4)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是_______________________________ 。
(5)结合资料二、三,你认为还应该在实验装置中增加的两种仪器是
①________________________ 。②___________________________ 。

实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)实验原理:
(2)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因:
(3)丙同学认为只要对实验装置进行适当改进,即可避免对乙烯气体检验的干扰,改进方法:
改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显。该小组再次查阅资料,对实验进行进一步的改进。
资料一:溴乙烷于55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%。
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快。
资料三:溴乙烷的沸点:38.2℃。
(4)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是
(5)结合资料二、三,你认为还应该在实验装置中增加的两种仪器是
①
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:
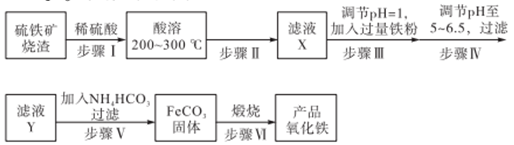
试回答下列问题:
(1)实验室实现“步骤II”中分离操作所用的玻璃仪器有____ 、玻璃棒和烧杯等;该步骤是为了除去_______ (填相关物质的化学式)。
(2)检验步骤III已经进行完全的操作是_______________________ 。
(3)步骤V的反应温度一般需控制在35℃以下,其目的是______________ ;该步骤中反应生成FeCO3的离子反应方程式为___________ 。
(4)步骤VI中发生反应的化学反应方程式为____________________ 。
(5)步骤V中,FeCO3达到沉淀溶解平衡时,若c(Fe2+)=1×10-6mol/L,欲使所得的FeCO3中不含有Fe(OH)2,应控制溶液的pH≤_____ (已知:Ksp[Fe(OH)2]=4.9×10-17,lg7=0.8)。
(6)欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶” “水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为______ 。

试回答下列问题:
(1)实验室实现“步骤II”中分离操作所用的玻璃仪器有
(2)检验步骤III已经进行完全的操作是
(3)步骤V的反应温度一般需控制在35℃以下,其目的是
(4)步骤VI中发生反应的化学反应方程式为
(5)步骤V中,FeCO3达到沉淀溶解平衡时,若c(Fe2+)=1×10-6mol/L,欲使所得的FeCO3中不含有Fe(OH)2,应控制溶液的pH≤
(6)欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶” “水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】某无色透明酸性溶液中可能含有K+、Fe2+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-、NO3-中的若干种离子。某同学取50 mL的溶液进行如下实验:
回答下列问题:
(1)原溶液中肯定存在的离子是____________ ,肯定不存在的离子是______________ 。
(2)原溶液中可能存在的离子是______________ 。
(3)原溶液中Cl-的浓度为______________ 。
(4)原溶液中c(K+)范围:_______________ (若不存在,说明理由)

回答下列问题:
(1)原溶液中肯定存在的离子是
(2)原溶液中可能存在的离子是
(3)原溶液中Cl-的浓度为
(4)原溶液中c(K+)范围:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】某澄清溶液中,可能含有下表中的若干种离子。
(已知H2SiO3是不溶于水的胶状沉淀,加热时易分解为两种氧化物;硅酸钙、硅酸钡是沉淀,硅酸银不存在)
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
(1)通过以上实验说明,一定存在的离子是___________ ;一定不存在离子是____________ ;可能存在的离子是____________________ 。
(2)写出实验Ⅰ中加入足量稀盐酸生成标准状况下0.56 L气体对应的离子方程式:___________________________________________________________________ 。写出实验Ⅱ中对应的化学方程式:________________________________ 。
(3)溶液中的阳离子的最小浓度是_________ mol·L-1。
| 阳离子 | K+ | Ag+ | Ca2+ | Ba2+ |
| 阴离子 | NO3- | CO32- | SiO32- | SO42- |
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色胶状沉淀并放出标准状况下0.56 L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、 灼烧至恒重,称量所得固体质量 | 固体质量为2.4 g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
(2)写出实验Ⅰ中加入足量稀盐酸生成标准状况下0.56 L气体对应的离子方程式:
(3)溶液中的阳离子的最小浓度是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】根据要求,回答下列问题:
I.某溶液由Na+、Al3+、Fe3+、NH 、Cl-、NO
、Cl-、NO 、CO
、CO 、SO
、SO 中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
步骤i:加入过量NaOH溶液,加热,产生气体和沉淀;
步骤ii:过滤,得滤液、滤渣;
步骤iii:取滤渣,洗涤、灼烧,得固体W;
步骤iv:取少量滤液,加入足量BaCl2溶液,产生白色沉淀。
(1)步骤iii所得固体W为________ (填化学式)。
(2)原溶液中一定存在的离子是_______ ,原溶液中一定不存在的离子是_______ 。
Ⅱ.Cr、Ca、O可形成一种具有特殊导电性的晶体(化学式为CaxCrOy,x、y为整数),其立方晶胞如图所示,Ca与O最小间距大于Cr与O最小间距。
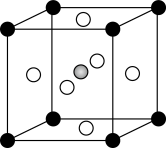
(3)Cr在晶胞中的位置为________ (填“顶点”“面心”或“体心”)。晶体中1个Ca周围与其最近的O的个数为_______ 。若Ca与O最小间距为apm,阿伏加德罗常数为NA,则该晶体的密度为________ g•cm-3(列出计算式)。
I.某溶液由Na+、Al3+、Fe3+、NH
 、Cl-、NO
、Cl-、NO 、CO
、CO 、SO
、SO 中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。
中的若干种离子所组成,且各离子的物质的量浓度相同。为确定其组成,现取适量溶液进行如下实验。步骤i:加入过量NaOH溶液,加热,产生气体和沉淀;
步骤ii:过滤,得滤液、滤渣;
步骤iii:取滤渣,洗涤、灼烧,得固体W;
步骤iv:取少量滤液,加入足量BaCl2溶液,产生白色沉淀。
(1)步骤iii所得固体W为
(2)原溶液中一定存在的离子是
Ⅱ.Cr、Ca、O可形成一种具有特殊导电性的晶体(化学式为CaxCrOy,x、y为整数),其立方晶胞如图所示,Ca与O最小间距大于Cr与O最小间距。

(3)Cr在晶胞中的位置为
您最近一年使用:0次



