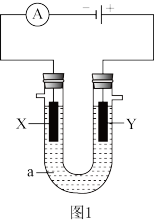
电解原理在化学领域应用广泛如图1表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请完成以下问题:
 +
+
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是______________ ;_______ .
②电解一段时间后,该反应总离子方程式_______ ;
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是_______ ,电解一段时间后,CuSO4溶液浓度_______ (填“增大”、减小”或“不变”)。
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:____ ;

(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:
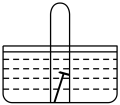
若试管内液面上升,则正极电极反应式为:______________________ 。
 +
+(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液:
①在X极附近观察到的现象是
②电解一段时间后,该反应总离子方程式
(2)若用该装置电解精炼铜,电解液a选用CuSO4溶液,则:X电极的材料是
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是:

(4)如图, 水槽中试管内有一枚铁钉,放置数天观察:

若试管内液面上升,则正极电极反应式为:
更新时间:2023-03-21 21:35:34
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】电化学腐蚀分类
由于条件不同,钢铁的腐蚀可以分为析氢腐蚀和吸氧腐蚀两种类型。
(1)析氢腐蚀:在酸性环境中,由于腐蚀过程中不断有H2放出,所以叫做析氢腐蚀。
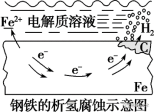
有关反应如下:
负极:___________ 。
正极:___________ 。
总反应:___________ 。
(2)吸氧腐蚀:如果钢铁表面吸附的水膜酸性很弱或呈中性,但溶有一定量的氧气,此时就发生吸氧腐蚀。
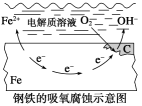
有关反应如下:
负极:___________ 。
正极:___________ 。
总反应:___________ 。
在空气中Fe(OH)2被进一步氧化成Fe(OH)3,Fe(OH)3失去部分水后生成Fe2O3·xH2O,它是铁锈的主要成分。
由于条件不同,钢铁的腐蚀可以分为析氢腐蚀和吸氧腐蚀两种类型。
(1)析氢腐蚀:在酸性环境中,由于腐蚀过程中不断有H2放出,所以叫做析氢腐蚀。

有关反应如下:
负极:
正极:
总反应:
(2)吸氧腐蚀:如果钢铁表面吸附的水膜酸性很弱或呈中性,但溶有一定量的氧气,此时就发生吸氧腐蚀。

有关反应如下:
负极:
正极:
总反应:
在空气中Fe(OH)2被进一步氧化成Fe(OH)3,Fe(OH)3失去部分水后生成Fe2O3·xH2O,它是铁锈的主要成分。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电化学原理在现实生活中有着十分广泛的应用。请回答下列问题:
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述_______ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_______ 。
(2)电镀在工业上有着广泛的应用,可以镀锌、镀铜、镀金等。利用如图所示装置可以将铜牌变为银牌,即在铜牌表面电镀一层银,该电解池的阴极反应可表示为_______ 。

(3)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含 的水溶液制备金属钴,其装置如图甲、乙。
的水溶液制备金属钴,其装置如图甲、乙。

①图乙中Co电极应连接乙醇燃料电池的_______ 极(填“a”或“b”。
②图甲中a极上发生的电极反应是_______ 。
③生成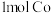 ,Ⅰ室溶液质量理论上减少
,Ⅰ室溶液质量理论上减少_______ g。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)电镀在工业上有着广泛的应用,可以镀锌、镀铜、镀金等。利用如图所示装置可以将铜牌变为银牌,即在铜牌表面电镀一层银,该电解池的阴极反应可表示为

(3)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含
 的水溶液制备金属钴,其装置如图甲、乙。
的水溶液制备金属钴,其装置如图甲、乙。
①图乙中Co电极应连接乙醇燃料电池的
②图甲中a极上发生的电极反应是
③生成
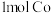 ,Ⅰ室溶液质量理论上减少
,Ⅰ室溶液质量理论上减少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示三套实验装置,分别回答下列问题。
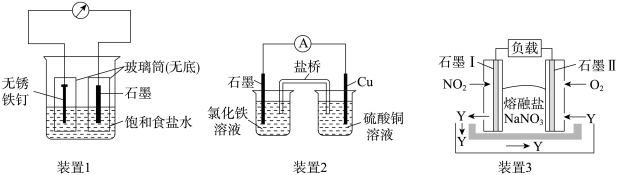
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被___________ (填“氧化”或“还原”);向插入石墨的玻璃筒内滴入酚酞溶液,可观察到石墨附近的溶液变红,该电极反应式为___________ 。
(2)装置2中的石墨作___________ (填“正”或“负”)极,该装置发生的总反应的离子方程式为___________ 。
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为___________ (填化学式);石墨II极的电极反应式为:___________ ;当石墨I极中有1molNO2参加反应时,石墨II极消耗的O2的体积___________ (标准状况下)。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被
(2)装置2中的石墨作
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】84消毒液等含氯消毒剂等可有效灭活新型冠状病毒。了解这些消毒剂的制备原理、性质十分重要。
试回答下列问题:
(1)取少量84消毒液于试管中,滴几滴酚酞试液,溶液先变红后褪色,其主要原因是_______ (用离子方程式表示)。
(2)采用如图所示的简易装置可以在家中制备84消毒液。a为电源______ 极,制备84消毒液的总反应的化学方程式为_______ 。
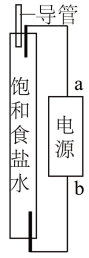
(3)盛装84消毒液宜选择塑料容器,不宜用铁器,其主要原因是________ (答2条即可)。
试回答下列问题:
(1)取少量84消毒液于试管中,滴几滴酚酞试液,溶液先变红后褪色,其主要原因是
(2)采用如图所示的简易装置可以在家中制备84消毒液。a为电源

(3)盛装84消毒液宜选择塑料容器,不宜用铁器,其主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电解原理在化学工业中有广泛应用。
(1)如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则Y电极上的电极反应式为____________ ;
②如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是_________ ,Y电极反应式为__________________ (说明:杂质发生的电极反应不必写出)。
(2)NOx、SO2的大量排放是造成大气污染的主要原因,研究其处理方法,将其变废为宝越来越受到人们的重视,按要求回答下列问题。
①富集废气中的SO2,并使其与O2反应可制备硫酸,装置如图所示,X、Y均为多孔电极材料。

Ⅰ气体A是_______ ,X极的电极反应式为___________________________ 。
Ⅱ消耗5.6L(标准状况下)气体B时,通过质子交换膜的H+的个数为__________ 。
②SO2也可用于制备Na2S2O3,但产品常含有杂质。某 SO2制得的此产品,为测其纯度,准确称取Wg该产品,用适量蒸馏水溶解,配成100ml溶液,取20mL,以淀粉作指示剂,用0.2000 mol•L-1碘的标准溶液滴定。反应原理为: 2S2O32-+I2=S4O62-+2I-。滴定至终点时,溶液颜色的变化:_______________________________ 。消耗碘的标准溶液体积为20.00mL。求产品的纯度为(设Na2S2O3相对分子质量为M)____________________ 。
(1)如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则Y电极上的电极反应式为
②如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是
(2)NOx、SO2的大量排放是造成大气污染的主要原因,研究其处理方法,将其变废为宝越来越受到人们的重视,按要求回答下列问题。
①富集废气中的SO2,并使其与O2反应可制备硫酸,装置如图所示,X、Y均为多孔电极材料。

Ⅰ气体A是
Ⅱ消耗5.6L(标准状况下)气体B时,通过质子交换膜的H+的个数为
②SO2也可用于制备Na2S2O3,但产品常含有杂质。某 SO2制得的此产品,为测其纯度,准确称取Wg该产品,用适量蒸馏水溶解,配成100ml溶液,取20mL,以淀粉作指示剂,用0.2000 mol•L-1碘的标准溶液滴定。反应原理为: 2S2O32-+I2=S4O62-+2I-。滴定至终点时,溶液颜色的变化:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
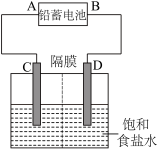
已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO42--2e- =PbSO4
正极PbO2+4H++SO42-+2e- =PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式_________________________ 。
(2)若在电解池C极一侧滴酚酞溶液,电解一段时间后未呈红色,说明铅蓄电池的A极为____ 极。
(3)用铅蓄电池电解1 L饱和食盐水(食盐水足量、密度为1.15 g/cm-3)时,
①若收集到11.2 L(标准状况下)氯气,则至少转移电子________ mol。
②铅蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为__________ L。
③消耗硫酸a mol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出)__________________________________ (用含a的代数式表示)。

已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO42--2e- =PbSO4
正极PbO2+4H++SO42-+2e- =PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式
(2)若在电解池C极一侧滴酚酞溶液,电解一段时间后未呈红色,说明铅蓄电池的A极为
(3)用铅蓄电池电解1 L饱和食盐水(食盐水足量、密度为1.15 g/cm-3)时,
①若收集到11.2 L(标准状况下)氯气,则至少转移电子
②铅蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为
③消耗硫酸a mol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。
(1)粗铜精炼时,通常用精铜作____ 极(填“阴”或“阳”)。
(2)硒在元素周期表中的位置如图所示:

Se原子结构示意图可表示为________ 。
②从原子结构角度解释硫与硒元素性质相似与不同的原因:同一主族________ 。
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
① 请写出CuSe与浓H2SO4反应的化学方程式________ 。
② 焙烧过程产生的烟气中含有少量SeO2,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为_______ 。
③ 写出步骤ⅱ中的化学方程式_______ 。
(4)下列说法合理的是________ 。
a. SeO2既有氧化性又有还原性,其还原性比SO2强
b. 浓硒酸可能具有强氧化性、脱水性
c. 热稳定性:H2Se < HCl < H2S
d. 酸性:H2SeO4 < HBrO4 < HClO4
(1)粗铜精炼时,通常用精铜作
(2)硒在元素周期表中的位置如图所示:

Se原子结构示意图可表示为
②从原子结构角度解释硫与硒元素性质相似与不同的原因:同一主族
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
① 请写出CuSe与浓H2SO4反应的化学方程式
② 焙烧过程产生的烟气中含有少量SeO2,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为
③ 写出步骤ⅱ中的化学方程式
(4)下列说法合理的是
a. SeO2既有氧化性又有还原性,其还原性比SO2强
b. 浓硒酸可能具有强氧化性、脱水性
c. 热稳定性:H2Se < HCl < H2S
d. 酸性:H2SeO4 < HBrO4 < HClO4
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电解原理在化学工业中有广泛应用。下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:___________ (填写“阳极”或“阴极”)。
(2)若X、Y都是惰性电极,a是饱和食盐水,Y极上的电极反应式为___________ 。
(3)若X、Y都是惰性电极,a是CuCl2溶液,X极的电极反应式为___________ 。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是___________ 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的的方案是___________。 填字母编号
填字母编号

(2)若X、Y都是惰性电极,a是饱和食盐水,Y极上的电极反应式为
(3)若X、Y都是惰性电极,a是CuCl2溶液,X极的电极反应式为
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的的方案是___________。
 填字母编号
填字母编号
| 方案 | X | Y |  溶液 溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 |  |
| C | 铁 | 银 | 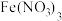 |
| D | 铁 | 银 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图为一个电化学过程的示意图。

请回答下列问题:
(1)通入CH3OH一极的电极反应式为__________________________ 。
(2)乙池是铜的精炼池,则A电极的材料是___________ ,B极的电极反应式为___________________ 。
(3)丙池含有0.01molKCl的溶液100mL,假如电路中转移了0.02mole-,则阳极产生的气体在标准状况下的体积是_______________ 。
(4)丙池中滴有酚酞,实验开始后观察到的现象是__________________________ ,写出丙池的总反应方程式_________________________ 。

请回答下列问题:
(1)通入CH3OH一极的电极反应式为
(2)乙池是铜的精炼池,则A电极的材料是
(3)丙池含有0.01molKCl的溶液100mL,假如电路中转移了0.02mole-,则阳极产生的气体在标准状况下的体积是
(4)丙池中滴有酚酞,实验开始后观察到的现象是
您最近一年使用:0次



