钢铁很容易生锈腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。因此,该小组同学又进行了钢铁腐蚀探究,希望能找到防止钢铁腐蚀的好办法。如图,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。红墨水柱两边液面变为:左低、右高。
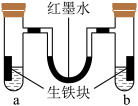
(1)请猜测a试管中铁发生的是________ (填“析氢”或“吸氧”)腐蚀。
(2)b管中生铁中碳上发生的电极反应式________________________ 。

(1)请猜测a试管中铁发生的是
(2)b管中生铁中碳上发生的电极反应式
更新时间:2023-03-05 13:02:20
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________ (填字母)。
a.碳棒 b.锌板 c.铜板
材料B需定期拆换,其是原因:________________ 。

(2)图2中,钢闸门C作__________ 极。若用氯化钠溶液液模拟海水进行实验,D为石墨块,则D上的电极反应为________________________ ,检测该电极反应产物的方法是______________________ 。
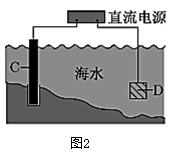
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的____________ 极(填“正”或“负”)。F电极上的电极反应为__________________________ 。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学方程式解释其原因:________________________ 。

(4)为提高甲醇燃料的利用率,科学家发明了甲醇燃料电池,电池的一个电极通入空气,另一个电极通入甲醇蒸气,电解质是掺入了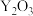 的
的 晶体,在高温下它能传导
晶体,在高温下它能传导 。电池在高温下工作时正极反应式为
。电池在高温下工作时正极反应式为__________________________ 。
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择
a.碳棒 b.锌板 c.铜板
材料B需定期拆换,其是原因:

(2)图2中,钢闸门C作

(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学方程式解释其原因:

(4)为提高甲醇燃料的利用率,科学家发明了甲醇燃料电池,电池的一个电极通入空气,另一个电极通入甲醇蒸气,电解质是掺入了
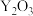 的
的 晶体,在高温下它能传导
晶体,在高温下它能传导 。电池在高温下工作时正极反应式为
。电池在高温下工作时正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】从金属材料到无机非金属材料,再到高分子材料,不同的组成和性能决定了材料独特的功能和用途。
(1)合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架,该合金中含量最高的金属为_______ (填元素符号)。
(2)铁锈的主要成分是_______ (填化学式),它是钢铁在潮湿的空气中发生_______ 腐蚀的结果。
(3)生产、生活中常见的无机非金属材料主要有_______ 。
(4)结合实例比较金属材料与无机非金属材料各有什么优缺点___________ 。
(1)合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架,该合金中含量最高的金属为
(2)铁锈的主要成分是
(3)生产、生活中常见的无机非金属材料主要有
(4)结合实例比较金属材料与无机非金属材料各有什么优缺点
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________ 。
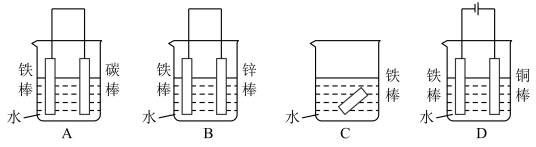
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①铁件应与电源的________ 极相连(写正或负),B电极的电极反应式是______ 。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为10.24 g,则电镀时电路中通过的电子为________ mol。
③电镀结束后CuSO4溶液的浓度______ (填变大,变小,不变)
④镀层破损后,铁不易被腐蚀的是___________ (填序号)。
A 镀铜铁 B 镀锌铁 C 镀锡铁
(1)下列哪个装置可防止铁棒被腐蚀
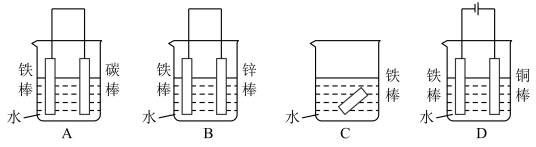
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①铁件应与电源的
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为10.24 g,则电镀时电路中通过的电子为
③电镀结束后CuSO4溶液的浓度
④镀层破损后,铁不易被腐蚀的是
A 镀铜铁 B 镀锌铁 C 镀锡铁
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钢铁在自然界中的腐蚀比较普遍。
(1)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的_____ 腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与直流电源的_____ (填“正”或“负”)极相连。
(2)利用如图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于_____ 处。若X为锌,开关K置于M处,该电化学防护法称为_____ 。
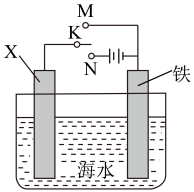
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图所示,请回答:
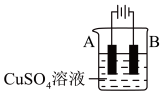
①应将铁件置于_____ 极(填A或B),另一电极材料应为_____ 。
②若电镀前铁、铜两片金属的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者的质量差为5.12g,则电镀时电路中通过的电子为_____ mol。
(1)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的
(2)利用如图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于

(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图所示,请回答:

①应将铁件置于
②若电镀前铁、铜两片金属的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者的质量差为5.12g,则电镀时电路中通过的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】《化学与生活》
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①蛋白质是人体必需的营养物质,它在人体内最终分解为( ) 。
A.葡萄糖 B.氨基酸 C.脂肪酸
②现有下列五种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是_______ ;可直接进入血液,补充能量的是______ ;应用最广泛的抗生素之一的是______ ;即可作为调味剂,又可作为防腐剂、着色剂的是______ ;食用过多会引起血压升高、肾脏受损的________ 。
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是( ) 。
A.酒精 B.蔗糖 C.甲醛
②一般情况下,合金比组成它的成分金属硬度__________ (填大、小)。
③_______ 腐蚀是造成钢铁腐蚀的主要原因,自行车的钢圈通常采用________ (填涂油漆或镀Cr)防腐蚀。
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①蛋白质是人体必需的营养物质,它在人体内最终分解为
A.葡萄糖 B.氨基酸 C.脂肪酸
②现有下列五种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是
A.酒精 B.蔗糖 C.甲醛
②一般情况下,合金比组成它的成分金属硬度
③
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属腐蚀是金属材料使用过程中的一种普遍现象。
(1)金属腐蚀的本质是_________ 的过程。用铝饭盒盛放醋酸,一段时间后饭盒被腐蚀,这种腐蚀属于__________ ,若用铝饭盒盛放食盐水,一段时间后,饭盒被腐蚀,这种腐蚀属于___________ 。
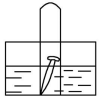
(2)钢铁的电化学腐蚀有两种不同的类型,在如图所示的装置中,试管内有一枚铁钉,放置数天观察:①若试管内液面上升,写出此时的电极反应式,负极:___________ ,正极:____________ 。②若试管内液面下降,则此时发生____________ (填电化学腐蚀类型),溶液呈___ 性,正极上的电极反应式为________________ 。
(3)钢铁发生吸氧腐蚀时,生成Fe(OH)2后的另一个反应方程式为__________________ 。
(1)金属腐蚀的本质是

(2)钢铁的电化学腐蚀有两种不同的类型,在如图所示的装置中,试管内有一枚铁钉,放置数天观察:①若试管内液面上升,写出此时的电极反应式,负极:
(3)钢铁发生吸氧腐蚀时,生成Fe(OH)2后的另一个反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。 段主要发生
段主要发生___________ 腐蚀, 段负极反应式为
段负极反应式为___________ 。
 段主要发生
段主要发生 段负极反应式为
段负极反应式为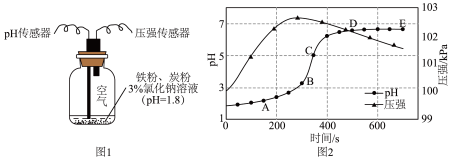
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铜在潮湿的空气中也能发生电化学腐蚀。
(1)铜___ (填“能”或“不能”)发生析氢腐蚀,原因是________________________________ 。
(2)若铜在中性或碱性环境中发生电化学腐蚀,则负极反应为________ ,正极反应为________ ,总反应为________ 。得到的产物还可与空气中的CO2继续反应,得到铜绿[Cu2(OH)2CO3],化学方程式是____________ 。
(3)若铜在酸性环境中发生电化学腐蚀,则正极反应为________ ,总反应为___________ 。
(4)工业上制取硫酸铜就是利用(3)的原理。试计算1 t铜理论上可以制得多少吨无水硫酸铜_____ ?
(1)铜
(2)若铜在中性或碱性环境中发生电化学腐蚀,则负极反应为
(3)若铜在酸性环境中发生电化学腐蚀,则正极反应为
(4)工业上制取硫酸铜就是利用(3)的原理。试计算1 t铜理论上可以制得多少吨无水硫酸铜
您最近一年使用:0次
【推荐1】回答下列问题:
(1)图中甲装置为 碱性燃料电池,其电极均为
碱性燃料电池,其电极均为 电极,装置乙中,C、D电极为
电极,装置乙中,C、D电极为 电极,其表面均覆盖着
电极,其表面均覆盖着 ,其电解液为稀
,其电解液为稀 溶液。
溶液。
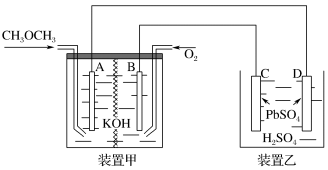
①甲装置中能量的转化形式主要为_______ 。
②写出乙装置中D极的电极反应式_______ 。
③当有46g二甲醚参加反应时,电路中通过的电子的数目为_______ 。
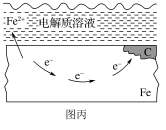
(2)钢铁锈蚀图如图丙所示:
①钢铁锈蚀的负极反应式为_______ 。
②钢铁发生吸氧腐蚀的正极反应式为_______ 。
(3)我国的科技人员为了消除 的污染,利用原电池原理,变废为宝,设计由
的污染,利用原电池原理,变废为宝,设计由 和
和 来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为
来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为_______ (填“正极”或“负极”),B极的电极反应式是_______ 。

(1)图中甲装置为
 碱性燃料电池,其电极均为
碱性燃料电池,其电极均为 电极,装置乙中,C、D电极为
电极,装置乙中,C、D电极为 电极,其表面均覆盖着
电极,其表面均覆盖着 ,其电解液为稀
,其电解液为稀 溶液。
溶液。
①甲装置中能量的转化形式主要为
②写出乙装置中D极的电极反应式
③当有46g二甲醚参加反应时,电路中通过的电子的数目为
(2)钢铁锈蚀图如图丙所示:

①钢铁锈蚀的负极反应式为
②钢铁发生吸氧腐蚀的正极反应式为
(3)我国的科技人员为了消除
 的污染,利用原电池原理,变废为宝,设计由
的污染,利用原电池原理,变废为宝,设计由 和
和 来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为
来制备硫酸,设计装置如图丁所示,电极A、B为多孔的惰性材料,则A极为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)下列反应是氧化还原反应且是吸热反应的是___________ 。
A.稀醋酸与烧碱溶液的反应
B.灼热的炭与CO2的反应
C.铁片与稀盐酸反应
D.Ba(OH)2•8H2O与NH4Cl反应
E.干冰汽化
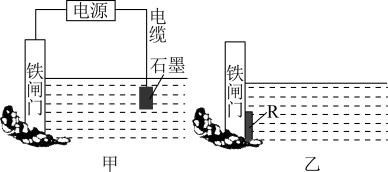
(2)实际生产生活中,钢铁等金属因电化学腐蚀损失巨大,而电化学在金属制备和加工中也发挥着重要的作用。生活中钢铁腐蚀以吸氧腐蚀为主,该腐蚀过程中正极的电极反应式为___________ 。金属的两种常见电化学防护方法如下图所示,图甲中铁闸门连接电源的___________ (填“正极”或“负极”),图乙所示金属的防护方法称为___________ 。
(1)下列反应是氧化还原反应且是吸热反应的是
A.稀醋酸与烧碱溶液的反应
B.灼热的炭与CO2的反应
C.铁片与稀盐酸反应
D.Ba(OH)2•8H2O与NH4Cl反应
E.干冰汽化
(2)实际生产生活中,钢铁等金属因电化学腐蚀损失巨大,而电化学在金属制备和加工中也发挥着重要的作用。生活中钢铁腐蚀以吸氧腐蚀为主,该腐蚀过程中正极的电极反应式为
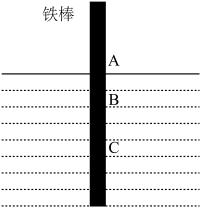
| A.铁棒AB段发生的反应为O2+2H2O+4e-=4OH- |
| B.腐蚀过程中在铁棒上会产生微电流,且方向是从BC段到AB段 |
| C.向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响 |
| D.产生这种现象的本质是铁棒所处的化学环境不同 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究金属腐蚀和防腐的原理很有现实意义。
(1)如图甲为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有__________(填字母)。
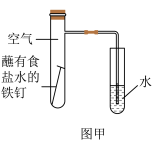
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化逐渐减慢,你认为影响因素为__________ 。

(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子生成蓝色沉淀,常用于亚铁离子的检验):
根据以上实验探究,试判断③______ (填“a”或“b”)为负极,该点腐蚀更严重。
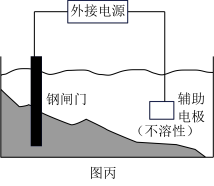
(4)图丙中钢闸门应与外接电源的__________ 相连(填“正极”或“负极”)钢闸门不会被腐蚀,属于__________ 保护法。
(1)如图甲为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有__________(填字母)。

| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化逐渐减慢,你认为影响因素为

(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子生成蓝色沉淀,常用于亚铁离子的检验):
实验操作 | 实验现象 | 实验结论 |
向 溶液中滴加2~3滴酚酞指示剂 溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为① |
然后再滴加2~3滴铁氰化钾溶液 | b点周围出现监色沉淀 | b点电极反应为② |
(4)图丙中钢闸门应与外接电源的

您最近一年使用:0次



