锡( )是人类较早发现并使用的金属,其原子结构示意图为:
)是人类较早发现并使用的金属,其原子结构示意图为: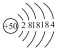 。锡属于主族元素,请描述其在元素周期表中的位置
。锡属于主族元素,请描述其在元素周期表中的位置________ 。有同学认为,锡的金属性比硅强,你认为合理吗?请简述理由。________
 )是人类较早发现并使用的金属,其原子结构示意图为:
)是人类较早发现并使用的金属,其原子结构示意图为: 。锡属于主族元素,请描述其在元素周期表中的位置
。锡属于主族元素,请描述其在元素周期表中的位置
2023高一·全国·专题练习 查看更多[1]
(已下线)第5章 金属及其化合物 5.1金属的性质
更新时间:2023-03-13 19:43:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)③、④、⑤、⑥简单离子半径由小到大的顺序为_____________________ 。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_____________________ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______ 。
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

(a)X溶液与Y溶液反应的离子方程式为_________ ,
(b)N→⑥的单质的化学方程式为________________ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)③、④、⑤、⑥简单离子半径由小到大的顺序为
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

(a)X溶液与Y溶液反应的离子方程式为
(b)N→⑥的单质的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图是短周期元素①~⑤在元素周期表中的位置。

(1)②在周期表中的位置是第___________ 周期第___________ 族,其与 反应的化学方程式是
反应的化学方程式是___________ 。
(2)③的一种核素的中子数是10,表示该核素的符号是___________ 。
(3)非金属性:④___________ ⑤(填“>”或“<”),从原子结构角度解释其原因:___________ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程___________ 。
(5)下列关于①的说法正确的是___________ 。
a、原子结构示意图为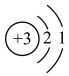
b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强

(1)②在周期表中的位置是第
 反应的化学方程式是
反应的化学方程式是(2)③的一种核素的中子数是10,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a、原子结构示意图为

b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表和元素周期律的应用
(1)根据同周期、同主族元素性质的递变规律判断元素性质的_______________ 。
(2)应用于_______________ 元素的相互推断。
(3)预测新元素
为新元素的发现及预测它们的_______________ 提供线索。
(4)寻找新物质
①在金属与非金属分界线附近寻找_______________ 。
②研究_______________ 附近元素,制造新农药。
③在_______________ 中寻找催化剂和耐高温、耐腐蚀的合金材料。
(1)根据同周期、同主族元素性质的递变规律判断元素性质的
(2)应用于
(3)预测新元素
为新元素的发现及预测它们的
(4)寻找新物质
①在金属与非金属分界线附近寻找
②研究
③在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】焦亚硫酸钠(Na2S2O5)是常用的脱氧剂,其制备方法是向Na2CO3溶液中通入SO2,生成NaHSO3和CO2,一定条件下NaHSO3转化为Na2S2O5。
完成下列填空:
(1)碳原子的原子结构示意图是____________ 。氧原子核外能量不同的电子有_____ 种。CO2的电子式是_________________ 。
(2)从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。______________________
(3)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其化学方程式为_______________ 。
证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________ 。
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+H2O→Na2SO4+H2SO4,该反应中,氧化产物是_____ ;若反应中转移了0.04 mol的电子,有____ g Na2S2O5参加反应。
完成下列填空:
(1)碳原子的原子结构示意图是
(2)从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。
(3)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其化学方程式为
证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+H2O→Na2SO4+H2SO4,该反应中,氧化产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以下元素均为第4周期元素,请回答相关问题。
(1)钾、锰分别位于___________ 族、___________ 族。
(2)基态铁原子的电子排布式为___________ 。
(3)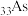 、
、 、
、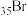 三种非金属元素的电负性由大到小的顺序为
三种非金属元素的电负性由大到小的顺序为___________ ;Br可与第三周期Cl元素形成化合物BrCl,其中显正价的元素为___________ ,原因是___________ 。
(1)钾、锰分别位于
(2)基态铁原子的电子排布式为
(3)
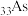 、
、 、
、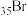 三种非金属元素的电负性由大到小的顺序为
三种非金属元素的电负性由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分:(不得用a~h字母回答)元素周期表有7个横行,每一个横行称为“周期”,周期序数=电子层数;元素周期表共有18列,每一列称为 “族”,下表中的7列为主族元素,分别用罗马数字Ⅰ、Ⅱ、……表明族序数,族序数=最外层电子数。
根据a~h各元素的性质,选择相应的化学符号、化学式或化学方程式 填空:
(1)单质氧化性最强的是__________ ,酸性最强的含氧酸是_____________ 。
(2)写出e的碱性气态氢化物的电子式_____ ,将它和化合物df 2通入饱和食盐水发生反应的化学方程式是_____ 。
(3)最高价氧化物对应的水化物中,碱性最强的是___________ 。
(4)在b、c、g、h中,常见离子半径最大的是__________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
一 | a | ||||||
二 | d | e | f | h | |||
三 | b | c | g |
(1)单质氧化性最强的是
(2)写出e的碱性气态氢化物的电子式
(3)最高价氧化物对应的水化物中,碱性最强的是
(4)在b、c、g、h中,常见离子半径最大的是
您最近一年使用:0次



