下图是短周期元素①~⑤在元素周期表中的位置。

(1)②在周期表中的位置是第___________ 周期第___________ 族,其与 反应的化学方程式是
反应的化学方程式是___________ 。
(2)③的一种核素的中子数是10,表示该核素的符号是___________ 。
(3)非金属性:④___________ ⑤(填“>”或“<”),从原子结构角度解释其原因:___________ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程___________ 。
(5)下列关于①的说法正确的是___________ 。
a、原子结构示意图为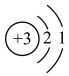
b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强

(1)②在周期表中的位置是第
 反应的化学方程式是
反应的化学方程式是(2)③的一种核素的中子数是10,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a、原子结构示意图为

b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强
更新时间:2023/01/06 08:49:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)写出元素符号:
①________ ,②________ ,⑨________ 。
(2)写出下列反应的化学方程式:
⑤的单质跟④的氢氧化物溶液反应:________________________________________ 。
⑥的单质在③的单质中燃烧:__________________________________________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ |
①
(2)写出下列反应的化学方程式:
⑤的单质跟④的氢氧化物溶液反应:
⑥的单质在③的单质中燃烧:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有几种元素的性质或原子结构如下表:
(1)元素X的一种同位素用来作原子量标准,这种同位素的符号是__________ 。
(2)画出T的原子结构示意图__________ 。
(3)写出由T、Y和Z三种元素组成的一种化合物在水溶液中的电离方程式__________ 。
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成Ne原子电子层结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其单质之一是空气中主要成分,最常见的助燃剂 |
| Z | 形成双原子单质分子,黄绿色气体 |
(1)元素X的一种同位素用来作原子量标准,这种同位素的符号是
(2)画出T的原子结构示意图
(3)写出由T、Y和Z三种元素组成的一种化合物在水溶液中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐3】四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数
依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_____ 、_______ ; 杂化轨道分别是________ 、_________ ;a分子的立体结构是____________ 。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______ 晶体、_______ 晶体:
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)__________ ;
(4)Y与Z比较,电负性较大的____________ , 其+2价离子的核外电子排布式是_________ 。
依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)
(4)Y与Z比较,电负性较大的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了a~i九种元素在周期表中的位置:
请回答下列问题:
(1)a的一种核素可测定文物年代,这种核素的符号为_____ 。c元素氢化物的电子式是_____ ,j的原子结构示意图_____ 。
(2)b、d、g三种元素的简单离子半径由大到小的顺序是_____ (填离子符号)。
(3)元素e的单质与i的最高价氧化物对应的水化物溶液反应的离子方程式为_____ 。
(4)设计实验并预测实验现象,证明h和g的非金属性的强弱_____ :
(5)工业上冶炼金属e的化学反应方程式_____ 。
周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | h | ||
| 4 | i | j | ||||||
(1)a的一种核素可测定文物年代,这种核素的符号为
(2)b、d、g三种元素的简单离子半径由大到小的顺序是
(3)元素e的单质与i的最高价氧化物对应的水化物溶液反应的离子方程式为
(4)设计实验并预测实验现象,证明h和g的非金属性的强弱
(5)工业上冶炼金属e的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表显示了元素周期表中短周期的一部分,①~⑥代表6种短周期元素。已知③与氢元素能组成生活中最常见的化合物X。请填写下列空白。
(1)④是___________ (写出元素符号)。
(2)⑥的单质与X反应的化学方程式为___________ 。
(3)①、②、③分别与氢元素组成含10个电子的分子的化学式分别为___________ 、___________ 、___________ 。
| ① | ② | ③ | ||||
| ④ | ⑤ | ⑥ |
(2)⑥的单质与X反应的化学方程式为
(3)①、②、③分别与氢元素组成含10个电子的分子的化学式分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分。
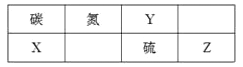
回答下列问题:
(1)Z元素在周期表中的位置为________ 。
(2)表中元素原子半径最大的是(写元素符号)________ 。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是________ 。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol Y单质比1 mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1 mol化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为________________ ,
Q与水反应的化学方程式为_______________________________________ 。

回答下列问题:
(1)Z元素在周期表中的位置为
(2)表中元素原子半径最大的是(写元素符号)
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol Y单质比1 mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1 mol化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为
Q与水反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响。完成下列填空:
(1)在氧、硫、硒、碲元素原子形成的简单阴离子中,其离子半径由大到小的顺序为______ (用离子符号表示)。与硫元素同周期且在本周期中非金属性最强的元素在周期表中的位置_______ 。
(2)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是____
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(3)石油化工的废气中有H2S,写出从废气中回收单质硫的两种方法
(除空气外,不能使用其他原料)。以化学方程式表示:___________________________
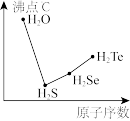
(4)从图可知氧族元素氢化物的沸点变化规律是________________________________________ 。
(5)2SO2(g)+O2(g)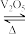 2SO3(g)是制备提取的需要反应,在恒温下,向容积固定的容器中加入一定量的SO2和O2,能说明该可逆反应已达到平衡状态的是
2SO3(g)是制备提取的需要反应,在恒温下,向容积固定的容器中加入一定量的SO2和O2,能说明该可逆反应已达到平衡状态的是______ (填序号)
a.V(O2)正=2v(SO2)逆 b.c(SO2)=c(SO3)
c.混合气体的密度保持不变 d.容器中压强不随时间变化而变化
(1)在氧、硫、硒、碲元素原子形成的简单阴离子中,其离子半径由大到小的顺序为
(2)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(3)石油化工的废气中有H2S,写出从废气中回收单质硫的两种方法
(除空气外,不能使用其他原料)。以化学方程式表示:
(4)从图可知氧族元素氢化物的沸点变化规律是

(5)2SO2(g)+O2(g)
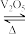 2SO3(g)是制备提取的需要反应,在恒温下,向容积固定的容器中加入一定量的SO2和O2,能说明该可逆反应已达到平衡状态的是
2SO3(g)是制备提取的需要反应,在恒温下,向容积固定的容器中加入一定量的SO2和O2,能说明该可逆反应已达到平衡状态的是a.V(O2)正=2v(SO2)逆 b.c(SO2)=c(SO3)
c.混合气体的密度保持不变 d.容器中压强不随时间变化而变化
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】指出下列反应的氧化剂和还原剂
(1)2H2+O2=2H2O:氧化剂_______ ;还原剂_______ 。
(2)4P+5O2=2P2O5:氧化剂_______ ;还原剂_______ 。
(3)Fe+H2SO4=FeSO4+H2 :氧化剂
:氧化剂_______ ;还原剂_______ 。
(4)WO3+3H2=W+3H2O:氧化剂_______ ;还原剂_______ 。
(5)已知 与
与 属于两性氢氧化物,写出
属于两性氢氧化物,写出 分别溶于
分别溶于 溶液、盐酸的化学方程式:
溶液、盐酸的化学方程式:_______ 、_______ 。
(1)2H2+O2=2H2O:氧化剂
(2)4P+5O2=2P2O5:氧化剂
(3)Fe+H2SO4=FeSO4+H2
 :氧化剂
:氧化剂(4)WO3+3H2=W+3H2O:氧化剂
(5)已知
 与
与 属于两性氢氧化物,写出
属于两性氢氧化物,写出 分别溶于
分别溶于 溶液、盐酸的化学方程式:
溶液、盐酸的化学方程式:
您最近一年使用:0次



