海水的综合利用
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是___________ 。
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是___________ 。
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是___________ 。
A.贝壳在海水提取镁的生产流程中,主要经历了 的过程
的过程
B.工业生产中利用电解熔融 制备镁
制备镁
C.在从海水中提取镁的工业流程中, 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁
(4)下图是海水提溴的工艺流程,下列说法错误的是___________ 。
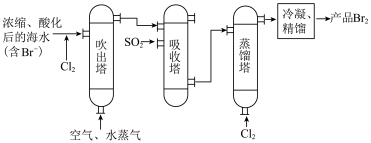
A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为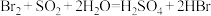
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式___________ 。
②检验阳极产物时可选用___________ ,向阴极附近溶液滴加紫色石蕊试液呈___________ 色。
③实验测得产生的 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为___________  。
。
(6)实验室模拟工业从海藻中提碘的流程如图:
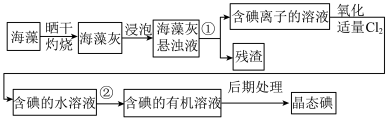
①选择合适实验操作名称填入流程图中:①___________ ,②___________ 。
A.溶解 B.过滤 C.萃取 D.分液
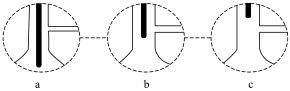
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
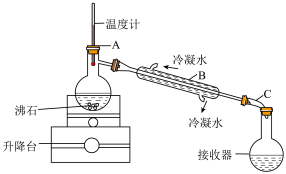
②装置中间部分是“冷凝管”,该装置中有一处明显的错误是___________ 。
③装置A中,温度计所处的正确位置是___________ 。(选填编号)
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是
A.贝壳在海水提取镁的生产流程中,主要经历了
 的过程
的过程B.工业生产中利用电解熔融
 制备镁
制备镁C.在从海水中提取镁的工业流程中,
 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用
 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁(4)下图是海水提溴的工艺流程,下列说法错误的是

A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为
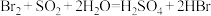
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式
②检验阳极产物时可选用
③实验测得产生的
 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为 。
。(6)实验室模拟工业从海藻中提碘的流程如图:

①选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

②装置中间部分是“冷凝管”,该装置中有一处明显的错误是
③装置A中,温度计所处的正确位置是

更新时间:2023-03-17 08:09:15
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。

Ⅰ.(1)上述过程中没有涉及到的四大基本反应类型是______ ;
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
(2)步骤1中分离操作的名称是___________ ;
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:a.盐酸;b.BaCl2溶液;c.NaOH溶液;d.Na2CO3溶液。加入试剂的顺序是_____________ ;
II.实验室利用精盐配制480mL 2.0mol·L-1NaCl溶液。
(4)除烧杯和玻璃棒外,还需要的玻璃仪器有___________________ 、_______________ ;
(5)用托盘天平称取固体NaCl________ g;
(6)配制时,按以下几个步骤进行:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥定容 ⑦摇匀 ⑧装瓶。操作中还缺少一个重要步骤是______________________ ;
(7)下列错误操作可使所配制氯化钠溶液浓度偏低的是_________ 。
a.容量瓶洗净后残留了部分的水
b.转移时溶液溅到容量瓶外面
c.定容时俯视容量瓶的刻度线
d.摇匀后见液面下降,再加水至刻度线

Ⅰ.(1)上述过程中没有涉及到的四大基本反应类型是
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
(2)步骤1中分离操作的名称是
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:a.盐酸;b.BaCl2溶液;c.NaOH溶液;d.Na2CO3溶液。加入试剂的顺序是
II.实验室利用精盐配制480mL 2.0mol·L-1NaCl溶液。
(4)除烧杯和玻璃棒外,还需要的玻璃仪器有
(5)用托盘天平称取固体NaCl
(6)配制时,按以下几个步骤进行:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥定容 ⑦摇匀 ⑧装瓶。操作中还缺少一个重要步骤是
(7)下列错误操作可使所配制氯化钠溶液浓度偏低的是
a.容量瓶洗净后残留了部分的水
b.转移时溶液溅到容量瓶外面
c.定容时俯视容量瓶的刻度线
d.摇匀后见液面下降,再加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】碘和铁均是人体必需的微量元素。
(1)海带中含有丰富的以碘离子形式存在的碘元素。在实验室中,从海藻中提取碘的流程如下:
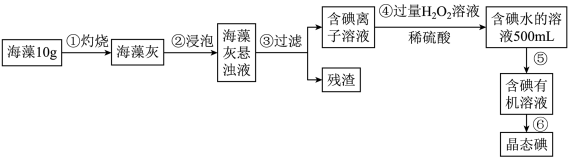
①上述流程中涉及下列操作,其中错误的是________________ (填标号)。
A.将海藻灼烧成灰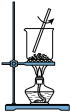
B.过滤含I-溶液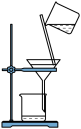
C.下口放出含碘的苯溶液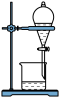
D.分离碘并回收苯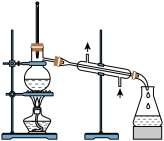
②写出步骤④发生反应的离子方程式:_______________________________________
③要证明步骤④所得溶液中含有碘单质,可加入___________________ (填试剂名称),观察到________________________ (填现象)说明溶液中存在碘。
(2)探究铁与稀硝酸的反应。用5.6gFe粉和含有0.3 mol HNO3的稀硝酸进行实验,若两种物质恰好完全反应,且HNO3只被还原成NO。回答下列问题:
①Fe粉与稀硝酸反应生成硝酸铁的化学方程式为___________________________________
②反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)=_________________ 。
③标准状况下,生成NO气体的体积为_________________ L(保留两位小数)。
(1)海带中含有丰富的以碘离子形式存在的碘元素。在实验室中,从海藻中提取碘的流程如下:

①上述流程中涉及下列操作,其中错误的是
A.将海藻灼烧成灰

B.过滤含I-溶液

C.下口放出含碘的苯溶液

D.分离碘并回收苯

②写出步骤④发生反应的离子方程式:
③要证明步骤④所得溶液中含有碘单质,可加入
(2)探究铁与稀硝酸的反应。用5.6gFe粉和含有0.3 mol HNO3的稀硝酸进行实验,若两种物质恰好完全反应,且HNO3只被还原成NO。回答下列问题:
①Fe粉与稀硝酸反应生成硝酸铁的化学方程式为
②反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)=
③标准状况下,生成NO气体的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】从海水淡化后的母液中提取溴和镁的一种过程如下:
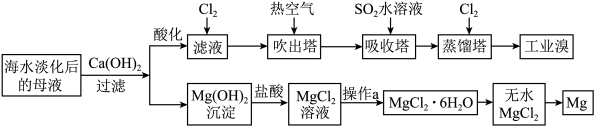
(1)操作a的主要步骤包括___________ ,过滤,洗涤,低温干燥。
(2)提取镁过程中由“无水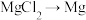 ”所选取的冶炼方法是
”所选取的冶炼方法是___________ (填字母序号)。
A.电解法 B.还原法 C.热分解法
(3)“吹出塔”中通入热空气能吹出 的原因是
的原因是___________ 。“吸收塔”中发生反应的离子方程式为___________ 。
(4)提取溴的过程中,经过2次 转化的目的是
转化的目的是___________ 。理论上每得到
 至少共需要
至少共需要___________ 
 。
。

(1)操作a的主要步骤包括
(2)提取镁过程中由“无水
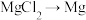 ”所选取的冶炼方法是
”所选取的冶炼方法是A.电解法 B.还原法 C.热分解法
(3)“吹出塔”中通入热空气能吹出
 的原因是
的原因是(4)提取溴的过程中,经过2次
 转化的目的是
转化的目的是
 至少共需要
至少共需要
 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】海水中化学资源的综合开发利用,已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,如图为提取它们的主要步骤:
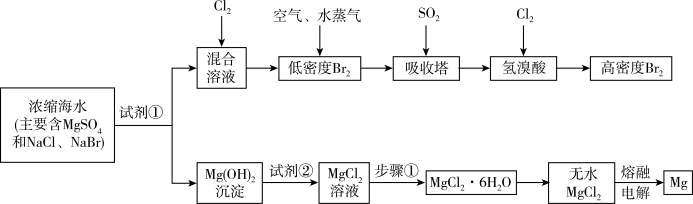
请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是_________ 。
(2)吸收塔中反应的离子方程式是_______ ,工业生产1mol Br2,理论上需要Cl2的物质的量为______ 。
(3)取10L海水经过提纯浓缩,向吸收塔吸收后的溶液中加入0.100 mol/L AgNO3溶液8.0 mL恰好完全反应,则海水中含溴的含量为______ mg/L(不考虑提纯过程中溴的损失)。
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用__________ (写化学式)。
(2)步骤①包括加热、蒸发、冷却、结晶、____________ 。
(3)通电时无水MgCl2在熔融状态下反应的化学方程式是_______________ 。

请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是
(2)吸收塔中反应的离子方程式是
(3)取10L海水经过提纯浓缩,向吸收塔吸收后的溶液中加入0.100 mol/L AgNO3溶液8.0 mL恰好完全反应,则海水中含溴的含量为
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用
(2)步骤①包括加热、蒸发、冷却、结晶、
(3)通电时无水MgCl2在熔融状态下反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】溴及其化合物广泛用于医药、塑料阻燃剂等。溴主要以 形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下:
形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下:
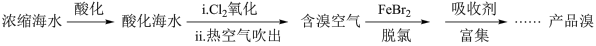
(1)酸化:将海水酸化的主要目的是避免___________ (填离子反应方程式)。
(2)脱氯:除去含溴空气中残留的
①具有脱氯作用的离子是___________ 。
②溶液失去脱氯作用后,补加 或加入
或加入___________ ,脱氯作用恢复。
③富集、制取 :
: 吸收了
吸收了 后,
后, 歧化为
歧化为 和
和 。则
。则 是
是___________ (填字母)。
a、 溶液 b、
溶液 b、 溶液 c、
溶液 c、 气体
气体
(3)再用 酸化歧化后的溶液得到
酸化歧化后的溶液得到 ,其离子反应方程式为
,其离子反应方程式为___________ 。
(4)探究 溶液与
溶液与 溶液反应时
溶液反应时 浓度对生成
浓度对生成 的影响,实验如下:
的影响,实验如下:
① 中溶液呈棕红色说明产生了
中溶液呈棕红色说明产生了___________ 。
②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由;若认为乙同学的分析合理,进一步设计实验方案说明。理由或方案:___________ 。
③酸化歧化后的溶液宜选用的酸是___________ (填“稀硫酸”或“浓硫酸”)。
 形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下:
形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程如下: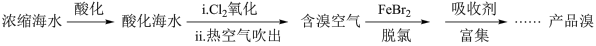
(1)酸化:将海水酸化的主要目的是避免
(2)脱氯:除去含溴空气中残留的

①具有脱氯作用的离子是
②溶液失去脱氯作用后,补加
 或加入
或加入③富集、制取
 :
: 吸收了
吸收了 后,
后, 歧化为
歧化为 和
和 。则
。则 是
是a、
 溶液 b、
溶液 b、 溶液 c、
溶液 c、 气体
气体(3)再用
 酸化歧化后的溶液得到
酸化歧化后的溶液得到 ,其离子反应方程式为
,其离子反应方程式为(4)探究
 溶液与
溶液与 溶液反应时
溶液反应时 浓度对生成
浓度对生成 的影响,实验如下:
的影响,实验如下:| 序号 | A | B | C |
| 试剂组成 | 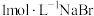 溶液 溶液 | 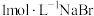 溶液 溶液 | 将B中反应后溶液 |
20% | 98% | 用水稀释 | |
| 实验现象 | 无明显现象 | 溶液呈棕红色放热 | 溶液颜色变得很浅 |
①
 中溶液呈棕红色说明产生了
中溶液呈棕红色说明产生了②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由;若认为乙同学的分析合理,进一步设计实验方案说明。理由或方案:
③酸化歧化后的溶液宜选用的酸是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海水淡化可获得淡水,并可按下述工业流程提取溴和镁。
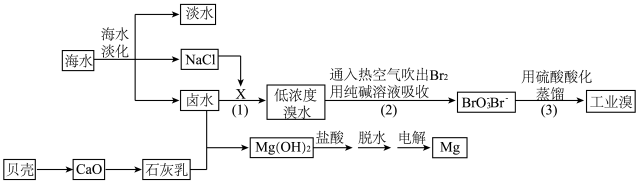
(1)海水淡化的方法为____ (写出其中一种即可)。
(2)步骤(1)中的X是一种单质,X的化学式为____ 。
(3)步骤(2)通入热空气吹出Br2,利用了溴的____ (填序号);溴与碳酸钠反应中氧化剂与还原剂物质的量之比为____ 。
a.氧化性 b.还原性 c.挥发性
(4)步骤(3)发生反应的离子方程式为____ ;充分反应后,要提取还要进行的操作为____ 、蒸馏。
(5)工业上从卤水中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是___ ;从母液中得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入____ (填化学式)溶液中,充分搅拌后经过滤、洗涤可得Mg(OH)2。
(6)写出冶炼金属镁的化学方程式___ 。

(1)海水淡化的方法为
(2)步骤(1)中的X是一种单质,X的化学式为
(3)步骤(2)通入热空气吹出Br2,利用了溴的
a.氧化性 b.还原性 c.挥发性
(4)步骤(3)发生反应的离子方程式为
(5)工业上从卤水中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是
(6)写出冶炼金属镁的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
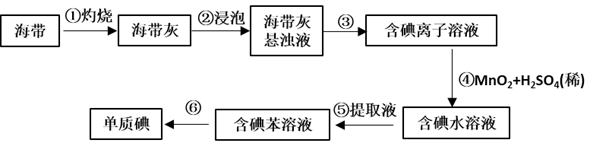
a.灼烧海带时,除需要三脚架外,还需要用到实验仪器是_____ (填字母)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
b.步骤③的实验选择上述图_____ (填“甲”“乙”或“丙”)装置。步骤⑤的实验操作名称是_____ ,选择上述图_____ (填“甲”“乙”或“丙”)装置。步骤⑥的目的是从含碘苯溶液中分离出单质碘,同时回收苯,该步骤的实验操作名称是_____ ,选择上述图_____ (填“甲”“乙”或“丙”)装置。
(2)某盐的混合溶液中含有Na+、Mg2+、Cl-、SO42-离子,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO42-)=_____

(1)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

a.灼烧海带时,除需要三脚架外,还需要用到实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
b.步骤③的实验选择上述图
(2)某盐的混合溶液中含有Na+、Mg2+、Cl-、SO42-离子,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO42-)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.请回答实验室制取蒸馏水的有关问题。
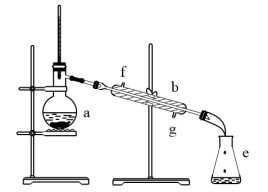
(1)写出下列仪器的名称:a.___________ b. ___________
(2)若利用该装置分离四氯化碳和酒精的混合物,还缺少的仪器是___________ ,将仪器补充完整后进行实验。冷却水由___________ (填f或g,下同)口通入,___________ 口流出。
(3)实验开始几分钟后,发现忘记添加沸石,此时应该进行的操作是___________ 。
Ⅱ.海洋植物如海带、海藻中含有大量的碘元素,请回答提取碘的有关问题。

(4)图中操作⑤,还可选择的试剂是___________
(5)操作⑤需要使用的主要玻璃仪器为___________ 。
(6)操作⑤的萃取环节结束后,分液漏斗中上层液体呈___________ 色;打开分液漏斗活塞,将下层液体从下口放出时,却未见液体流下,原因可能是___________ 。

(1)写出下列仪器的名称:a.
(2)若利用该装置分离四氯化碳和酒精的混合物,还缺少的仪器是
(3)实验开始几分钟后,发现忘记添加沸石,此时应该进行的操作是
Ⅱ.海洋植物如海带、海藻中含有大量的碘元素,请回答提取碘的有关问题。

(4)图中操作⑤,还可选择的试剂是___________
| A.酒精 | B.四氯化碳 | C.醋酸 | D.汽油 |
(6)操作⑤的萃取环节结束后,分液漏斗中上层液体呈
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】Ⅰ.海带中含有丰富的碘,某学习小组设计并进行以下实验:
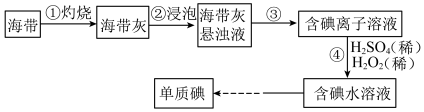
(1)步骤③的实验操作为___________ (填实验名称),此过程使用玻璃棒,玻璃棒的作用是___________ 。
(2)步骤④的离子反应方程式为: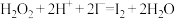 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是___________ ,还原剂是___________ 。步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现蓝色,说明有碘单质产生。
Ⅱ.碘称为“智力元素”。过去食盐中作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失, 被氧气氧化成碘单质(
被氧气氧化成碘单质( ),同时得到强碱性物质。
),同时得到强碱性物质。
(3)写出潮湿环境下 与氧气反应的化学方程式:
与氧气反应的化学方程式:___________ 。
Ⅲ.现在的食盐里改添加性质稳定的 ,以满足人们需要。几种粒子之间有如图所示关系:
,以满足人们需要。几种粒子之间有如图所示关系:
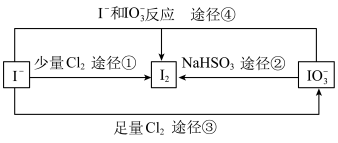
(4)四个途径中属于氧化还原反应的是___________ (填序号)。
(5)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(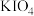 ),反应方程式为:
),反应方程式为: ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(6)比较 、
、 和
和 的氧化性强弱:
的氧化性强弱:___________ 。

(1)步骤③的实验操作为
(2)步骤④的离子反应方程式为:
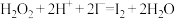 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是Ⅱ.碘称为“智力元素”。过去食盐中作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,
 被氧气氧化成碘单质(
被氧气氧化成碘单质( ),同时得到强碱性物质。
),同时得到强碱性物质。(3)写出潮湿环境下
 与氧气反应的化学方程式:
与氧气反应的化学方程式:Ⅲ.现在的食盐里改添加性质稳定的
 ,以满足人们需要。几种粒子之间有如图所示关系:
,以满足人们需要。几种粒子之间有如图所示关系:
(4)四个途径中属于氧化还原反应的是
(5)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(
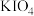 ),反应方程式为:
),反应方程式为: ,写出该反应的离子方程式:
,写出该反应的离子方程式:(6)比较
 、
、 和
和 的氧化性强弱:
的氧化性强弱:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】海水中含有丰富的矿物资源,很多以离子状态存在。现今人们重视海洋资源的利用,从海洋中获取了多种物质。如图是以海水为原料获取几种物质的流程图:
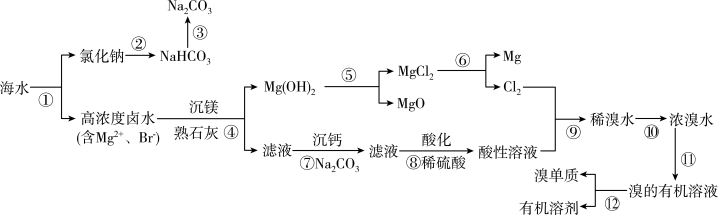
已知 在碱性溶液中不能稳定存在。
在碱性溶液中不能稳定存在。
回答下列问题:
(1)步骤⑫的操作名称为___________ 。
(2)步骤②的实现需要向氯化钠溶液中通入 、
、 ,应先通入
,应先通入__________ 。
(3)步骤⑥的化学方程式为_______________________________________________________ 。步骤⑨的离子方程式为_________________________________________ 。
(4)步骤⑧的目的是________________________________________ 。
(5)步骤⑪为萃取分液,需要用到的萃取试剂可以为_________ (填字母)需要用到的玻璃仪器名称为_______ 。
a. 裂化汽油 b. 苯 c. 酒精 d. 四氯化碳

已知
 在碱性溶液中不能稳定存在。
在碱性溶液中不能稳定存在。回答下列问题:
(1)步骤⑫的操作名称为
(2)步骤②的实现需要向氯化钠溶液中通入
 、
、 ,应先通入
,应先通入(3)步骤⑥的化学方程式为
(4)步骤⑧的目的是
(5)步骤⑪为萃取分液,需要用到的萃取试剂可以为
a. 裂化汽油 b. 苯 c. 酒精 d. 四氯化碳
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海洋蕴藏着丰富的资源,以海水为原料可以制取Na、NaOH 、Mg、Cl2、Br2等。下图是某化工厂对海水资源综合利用的示意图。
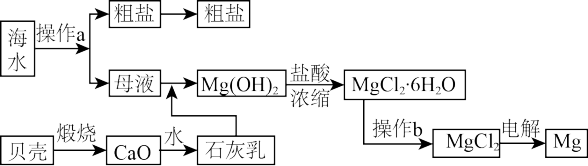
回答下列问题:
(1)流程图中操作a的名称为_______________ 。
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是____________ (填序号)。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。电解所得的镁蒸气需在特定的环境中冷却,不能用CO2 作冷却剂的原因是___________________ (用化学方程式表示)。
(4)上述流程没有涉及到的四大基本反应类型是________________
A 化合反应 B 分解反应 C 置换反应 D 复分解反应
(5)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入氯气,又制取了重要的化工原料溴单质,生成溴单质反应的离子方程式是______________________ 。

回答下列问题:
(1)流程图中操作a的名称为
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、
 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③Ba(OH)2,这3种试剂添加的合理顺序是(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。电解所得的镁蒸气需在特定的环境中冷却,不能用CO2 作冷却剂的原因是
(4)上述流程没有涉及到的四大基本反应类型是
A 化合反应 B 分解反应 C 置换反应 D 复分解反应
(5)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入氯气,又制取了重要的化工原料溴单质,生成溴单质反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海水中含有丰富的矿物资源,很多以离子状态存在。今人重视海洋资源的利用,从海洋中获取了多种物质。如图是以海水为原料获取几种物质的流程图:
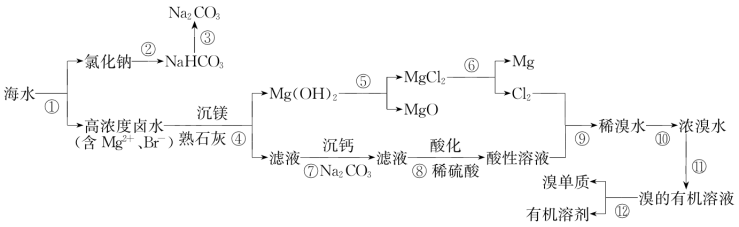
已知Br2在碱性溶液中不能稳定存在。回答下列问题:
(1)步骤③的操作名称为___________
(2)步骤②的实现需要向氯化钠溶液中通入CO2、NH3,应先通入___________
(3)步骤⑥的化学方程式为___________ 步骤⑨的离子方程式为___________
(4)步骤⑧的目的是___________
(5)步骤⑪为萃取分液,需要用到的萃取试剂可以为___________ (填字母),需要用到的玻璃仪器名称为___________
a.裂化汽油 b.苯 c.酒精 d.四氯化碳

已知Br2在碱性溶液中不能稳定存在。回答下列问题:
(1)步骤③的操作名称为
(2)步骤②的实现需要向氯化钠溶液中通入CO2、NH3,应先通入
(3)步骤⑥的化学方程式为
(4)步骤⑧的目的是
(5)步骤⑪为萃取分液,需要用到的萃取试剂可以为
a.裂化汽油 b.苯 c.酒精 d.四氯化碳
您最近一年使用:0次



