下列比较错误的是
| A.原子半径:N>O>F | B.酸性强弱:H2SO4>H2CO3>H2SiO3 |
| C.氢化物稳定性:PH3>H2S>HCl | D.碱性强弱:KOH>NaOH>Mg(OH)2 |
更新时间:2023-03-21 08:58:57
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】运用元素周期律分析下面的推断,其中错误的是
| A.铍的氧化物对应的水化物可能具有两性 |
| B.砹是一种有色固体,HAt很不稳定,AgAt是有色难溶于水的固体 |
| C.高溴酸(HBrO4)的酸性比硒酸(H2SeO4)的酸性弱 |
| D.硫酸锶(SrSO4)是难溶于水和盐酸的白色固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】几种短周期元素的原子半径及主要化合价如下表:
下列说法错误的是
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10m) | 1. 86 | 0. 99 | 1. 43 | I.60 | 0. 75 | 0. 74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | — |
| 最低负价 | — | -1 | — | — | -3 | -2 | |
| A.Q2-比R3-更容易失去电子 |
| B.X、Z、R的最高价氧化物的水化物之间可两两相互反应 |
| C.元素X和Q形成的化合物中可能既含离子键,也含共价键 |
| D.元素形成的气态氢化物稳定性:Q>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A.X的最常见气态氢化物的水溶液显酸性 |
| B.Z、W常见气态氢化物的稳定性W比Z强 |
| C.Z的单质与氢气反应比Y的单质与氢气反应剧烈 |
| D.X的原子半径小于Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】主族元素X、Y、Z、W的原子序数依次增加,Y、Z、W位于不同周期,且序数均小于20,X的单质是手机电池重要的材料;常温下,Y的两种气态氧化物之间可发生可逆反应;X、Y、W最外层电子数之和与Z的最外层电子数相等。下列说法正确的是
| A.X、W的单质均为活泼金属,通常保存在煤油中 |
| B.常温下,Z的单质与Y的气态氢化物相遇,可能产生白烟 |
C.Y、Z可形成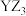 化合物, 化合物,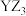 不能用于进口水果的熏蒸来消杀有害病虫 不能用于进口水果的熏蒸来消杀有害病虫 |
| D.由X、Z、W三种元素组成的化合物的水溶液显强酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如下图所示。Y与Z能形成Z2Y、Z2Y2型离子化合物,R原子最外层电子数是电子层数的2倍,T单质但难溶于水微溶于酒精。下列说法正确的是
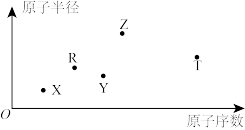
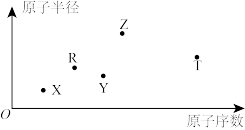
| A.最高价氧化物对应水化物的酸性:R>T |
| B.氢化物的沸点一定是Y>R |
| C.原子半径和离子半径均满足Y<Z |
| D.由X、Y、Z、T四种元素组成的化合物中既含有离子键又含有共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】X、Y、Z、W是原子序数依次增大的短周期主族元素,它们均位于不同的奇数族。X与Y位于不同周期,且X、Y、W族序数之和等于Z的质子数,X与W的最高化合价之和为8,Z元素是金属元素且位于元素周期表中“分界线”旁。下列说法错误的是
A.简单离子半径: |
| B.X、Y、W三种元素可形成水溶液显酸性的化合物 |
C.常见单质沸点: |
D.最高价氧化物对应的水化物的酸性: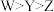 |
您最近一年使用:0次

 洗涤残留在试管壁上的N单质。下列说法不正确的是
洗涤残留在试管壁上的N单质。下列说法不正确的是


