依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。___________
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。
更新时间:2023-03-28 21:59:05
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】元素周期表的用途广泛。
(1)用“>”或“<”填空:
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液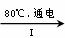 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
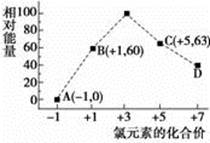
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
(1)用“>”或“<”填空:
| 离子半径 | 非金属性 | 熔点 | 沸点 |
| K+_____S2- | N____O | 金刚石_____晶体硅 | HF____HCl |
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液
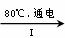 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。

①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】人类利用化学反应不仅可以创造新物质,还可以获取能量或实现不同形式能量之间的转化。已知下列热化学方程式:
①氢气燃烧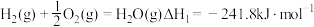
②太阳光分解水制氢气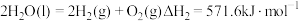
(1)从能量转化角度分析,反应①为_______ 反应。(选填“吸热”或“放热”)
(2)反应②中主要能量转化形式为_______ 能转化为_______ 能。
(3)若在反应②中使用催化剂,
_______ 。(选填“增大”“减小”或“不变”)
(4) 时,单位质量或单位体积的燃料完全燃烧所放出的热量叫做该燃料的热值。根据下表一些燃料的热值及所学知识简要说明氢气作为能源的优点
时,单位质量或单位体积的燃料完全燃烧所放出的热量叫做该燃料的热值。根据下表一些燃料的热值及所学知识简要说明氢气作为能源的优点_______ 。
(5)可以通过图示的方法表示化学反应是放热反应还是吸热反应。下列化学反应中的能量变化与图中所示不符合的是_______。

(6)天然气是一种高效、清洁的气体燃料,主要成分是甲烷。 时,
时,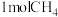 气体完全燃烧生成液态水和
气体完全燃烧生成液态水和 气体,放出
气体,放出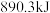 的热量,反应的热化学方程式为
的热量,反应的热化学方程式为_______ 。
(7)根据键能数据计算 的反应热
的反应热 为
为_______  。(已知:共价键的强弱可用键能来衡量。键能是指气态分子中
。(已知:共价键的强弱可用键能来衡量。键能是指气态分子中 化学键解离成气态原子所吸收的能量。)
化学键解离成气态原子所吸收的能量。)
①氢气燃烧
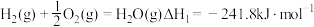
②太阳光分解水制氢气
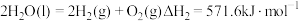
(1)从能量转化角度分析,反应①为
(2)反应②中主要能量转化形式为
(3)若在反应②中使用催化剂,

(4)
 时,单位质量或单位体积的燃料完全燃烧所放出的热量叫做该燃料的热值。根据下表一些燃料的热值及所学知识简要说明氢气作为能源的优点
时,单位质量或单位体积的燃料完全燃烧所放出的热量叫做该燃料的热值。根据下表一些燃料的热值及所学知识简要说明氢气作为能源的优点| 燃料 | 热值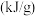 |
| 氢气 | 142.9 |
| 一氧化碳 | 10.11 |
| 甲烷 | 55.64 |

| A.铝热反应 | B.生石灰与水反应 | C.铁粉与硫粉加热反应 | D.氯酸钾分解制氧气 |
 时,
时,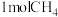 气体完全燃烧生成液态水和
气体完全燃烧生成液态水和 气体,放出
气体,放出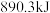 的热量,反应的热化学方程式为
的热量,反应的热化学方程式为(7)根据键能数据计算
 的反应热
的反应热 为
为 。(已知:共价键的强弱可用键能来衡量。键能是指气态分子中
。(已知:共价键的强弱可用键能来衡量。键能是指气态分子中 化学键解离成气态原子所吸收的能量。)
化学键解离成气态原子所吸收的能量。)| 化学键 | C-H | C-F | H-F | F-F |
键能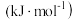 | 414 | 489 | 565 | 155 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】依据事实,写出下列反应的热化学反应方程式。
(1)在25℃、101kPa下,1g甲醇完全燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________________________________ 。
(2)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为___________________________________ 。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量,则表示该反应的热化学方程式为_________________________________________________ 。
(4)已知拆开1molH—H键,1molN—H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为______________________________ 。
(1)在25℃、101kPa下,1g甲醇完全燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量,则表示该反应的热化学方程式为
(4)已知拆开1molH—H键,1molN—H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究重点。
Ⅰ.已知:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1
2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1
H2(g)+Cl2(g)=2HCl(g) ΔH=-184 kJ·mol-1

(1)H2与O2反应生成气态水的热化学方程式是_______ 。
(2)断开1 mol H-O所需能量为_______ kJ。
Ⅱ.已知:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1①
CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1②
又知CH4的燃烧热为890.3 kJ·mol-1。
(3)利用上述已知条件写出甲烷完全燃烧的热化学方程式:_______ 。
(4)以甲烷为原料制取氢气是工业上常用的制氢方法,CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_______ 。
(5)高温下H2O可分解生成分子或原子。高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是_______ ,等物质的量的A、H2化学能较低的物质是_______ 。

Ⅰ.已知:4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1
2Cl2(g)+2H2O(g) ΔH=-115.6 kJ·mol-1H2(g)+Cl2(g)=2HCl(g) ΔH=-184 kJ·mol-1

(1)H2与O2反应生成气态水的热化学方程式是
(2)断开1 mol H-O所需能量为
Ⅱ.已知:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1①
CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1②
又知CH4的燃烧热为890.3 kJ·mol-1。
(3)利用上述已知条件写出甲烷完全燃烧的热化学方程式:
(4)以甲烷为原料制取氢气是工业上常用的制氢方法,CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
(5)高温下H2O可分解生成分子或原子。高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究化学反应中的能量变化有重要意义,请根据学过的知识回答下列问题。
(1)已知CH3OH(1)的燃烧热△H = - 238.6 kJ·mol-1,CH3OH(1)+ O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a
O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a___________ (填“> ”“<”或“=”) 238. 6。
(2)已知:H2(g)+ O2(g)
O2(g)  H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为
H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为___________ 。
(3)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:___________ 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H = - 1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为___________ kJ。
(5)已知25℃、101 kPa时,1 g甲烷不完全燃烧生成CO和液态水时放出37.96 kJ热量,则该条件下反应2CH4(g) +3O2(g)=2CO(g)+4H2O(l)的△H =___________ kJ·mol-1。
(1)已知CH3OH(1)的燃烧热△H = - 238.6 kJ·mol-1,CH3OH(1)+
 O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a
O2(g)=CO2(g) +2H2O(g) △H = -akJ·mol-1,则a(2)已知:H2(g)+
 O2(g)
O2(g)  H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为
H2O(g) △H = -241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为(3)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H = - 1176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
(5)已知25℃、101 kPa时,1 g甲烷不完全燃烧生成CO和液态水时放出37.96 kJ热量,则该条件下反应2CH4(g) +3O2(g)=2CO(g)+4H2O(l)的△H =
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25 ℃、101 kPa时,16 g CH4完全燃烧生成液态水时放出的热量是890.31 kJ,则表示CH4燃烧热的热化学方程式是_______________________ 。
(2)已知:C(s) + O2(g) CO2(g) ΔH1 =-437.3 kJ•mol-1
CO2(g) ΔH1 =-437.3 kJ•mol-1
2H2(g) + O2(g) 2H2O(g) ΔH2 =-571.6 kJ•mol-1
2H2O(g) ΔH2 =-571.6 kJ•mol-1
2CO(g) +O2(g) 2CO2(g) ΔH3 =-566.0 kJ•mol-1
2CO2(g) ΔH3 =-566.0 kJ•mol-1
则煤气化主要反应的热化学方程式是:C(s)+ H2O(g) CO(g) + H2(g) ΔH =
CO(g) + H2(g) ΔH =________ kJ•mol-1。如果该反应ΔS =+133.7 J·mol-1·K-1 ,该反应在常温下 _______ 自发进行(填 “能”或“不能”)。
(3) 已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则反应N2(g)+3H2(g) 2NH3 (g) ΔH =
2NH3 (g) ΔH =_________
(1)在25 ℃、101 kPa时,16 g CH4完全燃烧生成液态水时放出的热量是890.31 kJ,则表示CH4燃烧热的热化学方程式是
(2)已知:C(s) + O2(g)
 CO2(g) ΔH1 =-437.3 kJ•mol-1
CO2(g) ΔH1 =-437.3 kJ•mol-12H2(g) + O2(g)
 2H2O(g) ΔH2 =-571.6 kJ•mol-1
2H2O(g) ΔH2 =-571.6 kJ•mol-12CO(g) +O2(g)
 2CO2(g) ΔH3 =-566.0 kJ•mol-1
2CO2(g) ΔH3 =-566.0 kJ•mol-1 则煤气化主要反应的热化学方程式是:C(s)+ H2O(g)
 CO(g) + H2(g) ΔH =
CO(g) + H2(g) ΔH =(3) 已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则反应N2(g)+3H2(g)
 2NH3 (g) ΔH =
2NH3 (g) ΔH =
您最近一年使用:0次



