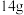利用微生物电池可以将工业废水中的有机物(以葡萄糖为例)、硝酸盐、亚硝酸盐转化为大气循环系统中的物质,其反应机理如图所示。下列说法正确的是


| A.外电路中:电流从非生物电极→灯泡→微生物电极 |
| B.电池温度越高,越有利于N2的产生 |
C.非生物电极的电极反应式: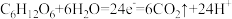 |
| D.若生成1molN2,则反应中一定转移8mol电子 |
更新时间:2023-04-16 16:03:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】 在强碱性溶液中主要以
在强碱性溶液中主要以 形式存在。
形式存在。 燃料电池工作原理如图所示。正极反应式为
燃料电池工作原理如图所示。正极反应式为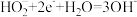 。提示:电池效率等于电路上通过的电子数与负极失去电子数之比。下列说法错误的是
。提示:电池效率等于电路上通过的电子数与负极失去电子数之比。下列说法错误的是
 在强碱性溶液中主要以
在强碱性溶液中主要以 形式存在。
形式存在。 燃料电池工作原理如图所示。正极反应式为
燃料电池工作原理如图所示。正极反应式为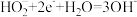 。提示:电池效率等于电路上通过的电子数与负极失去电子数之比。下列说法错误的是
。提示:电池效率等于电路上通过的电子数与负极失去电子数之比。下列说法错误的是
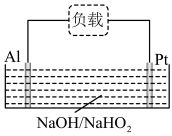
| A.Al极发生氧化反应 |
| B.电流由Pt极经负载流向Al极 |
C.放电时, 向Al极迁移 向Al极迁移 |
D.若正极生成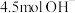 ,电路经过2.4mol电子,电池效率为60% ,电路经过2.4mol电子,电池效率为60% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某原电池以铂、银为电极,用含Ag+的固体作电解质,Ag+可在固体电解质中自由移动。电池总反应式为2Ag+Cl2 =2AgCl。利用该电池可以测定空气中Cl2的含量。下列说法中错误的是
| A.空气中c(Cl2)越大,消耗Ag的速率越快 |
| B.铂电极上发生的电极反应式为Cl2+2e-=2Cl- |
| C.电池工作时电解质中Ag+总数保持不变 |
| D.电子移动方向:银→外电路导线→铂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于各图的说法,不正确的是
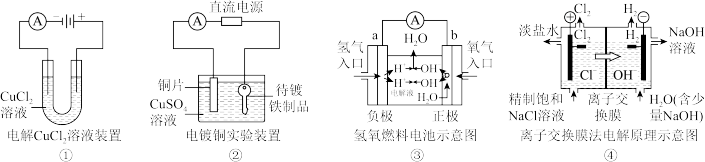

| A.①中阴极处能产生使湿润淀粉—KI试纸变蓝的气体 |
| B.②中待镀铁制品应与电源负极相连 |
| C.③中电子由a极流向b极 |
| D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】流动电池是一种新型电池,其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。某种流动电池装置如图所示,电池总反应为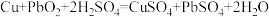 。下列说法不正确的是
。下列说法不正确的是
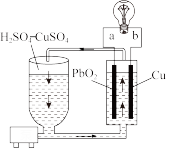
 。下列说法不正确的是
。下列说法不正确的是
| A.a为正极,b为负极 |
B.该电池工作时 电极附近溶液的pH增大 电极附近溶液的pH增大 |
C.b极的电极反应为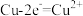 |
| D.电流由b极流出,经导线流向a极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】微生物脱盐电池是高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含CH3COO-的溶液为例)。下列说法错误 的是
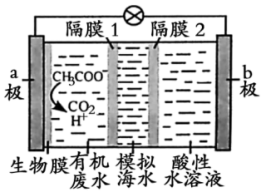

| A.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜 |
| B.电池工作一段时间后,正、负极产生气体的物质的量之比为2:1 |
| C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g |
| D.负极反应为CH3COO-+2H2O-8e-=2CO2↑+7H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一种热再生氨基液流电池的工作原理如图所示,下列有关说法错误 的是
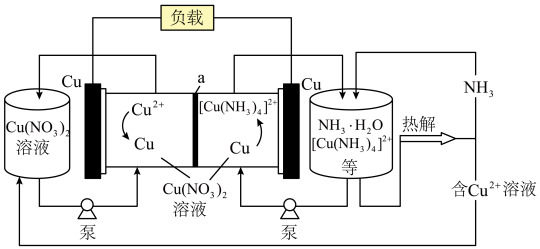
| A.a为阴离子交换膜 |
B.放电时负极反应为 |
C.为保证电池的循环使用需不断更换新的负极金属 板 板 |
D.热解的离子方程式为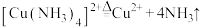 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】取琼脂、饱和食盐水的混合溶液倒入培养皿中,滴入几滴酚酞和 溶液,混合均匀,放入裹有锌片的铁钉(如下图所示),一段时间后,下列说法不正确的是
溶液,混合均匀,放入裹有锌片的铁钉(如下图所示),一段时间后,下列说法不正确的是
 溶液,混合均匀,放入裹有锌片的铁钉(如下图所示),一段时间后,下列说法不正确的是
溶液,混合均匀,放入裹有锌片的铁钉(如下图所示),一段时间后,下列说法不正确的是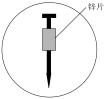
| A.锌片附近琼脂颜色变红 |
B.铁钉上的电极反应式: |
| C.离子在半凝固态的琼脂内可定向移动 |
| D.将锌片改为铜片,琼脂中会出现蓝、红、蓝三个色块 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】2021年我国科研人员以二硫化钼(MoS2)作为电极催化剂,研发出一种Zn-NO电池系统,该电池同时具备合成氨和对外供电的功能,其工作原理如图所示。已知双极膜可将水解离为H+和OH—,并实现其定向通过,则下列说法错误的是
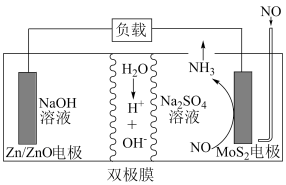

| A.Zn/ZnO电极电势要比MoS2电极电势低 |
| B.双极膜的存在能保证两侧电解质溶液的浓度不变 |
| C.Zn/ZnO电极表面发生的反应为Zn-2e—+2OH—=ZnO+H2O |
| D.当电路通过1mol e—时,整个电池系统质量会增大2.6 g |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】Li-SO2Cl2电池可用于心脏起搏器。该电池的电极材料分别为Li和C,电解液是LiAlCl4-SO2Cl2,总反应为:2Li+SO2Cl2=2LiCl+SO2↑,其工作示意图如图所示。下列叙述中正确的是
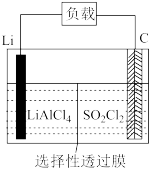

| A.电池工作时负极材料是Li,发生还原反应 |
| B.电池工作肘,电子流向:锂电极→负载→碳棒→电解液→锂电极 |
| C.外电路流过0.2mol电子,生成2.24L气体 |
| D.电池必须在无水、无氧的条件下进行工作 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔融) 4Na+O2↑+2H2O;后来盖•吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH
4Na+O2↑+2H2O;后来盖•吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
 4Na+O2↑+2H2O;后来盖•吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH
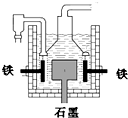
4Na+O2↑+2H2O;后来盖•吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是( )
| A.电解熔融氢氧化钠制钠,阴极发生电极反应为:2OH--2e-═H2↑+O2↑ |
| B.盖•吕萨克法制钠原理是利用铁的还原性比钠强 |
| C.若戴维法与盖•吕萨克法制得等量的钠,则两反应中转移的电子总数也相同 |
| D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
您最近一年使用:0次

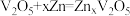 。下列关于电池工作原理的说法中,错误的是
。下列关于电池工作原理的说法中,错误的是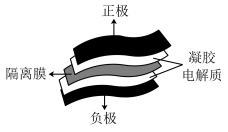
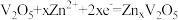
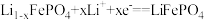 ;下列说法不正确的是
;下列说法不正确的是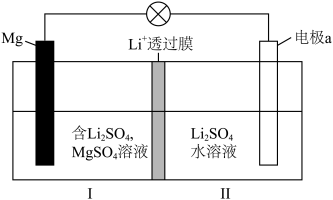
 极为阴极
极为阴极 从I室向II室迁移
从I室向II室迁移 溶液的浓度增大
溶液的浓度增大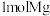 ,电极a质量理论上增加
,电极a质量理论上增加