中国药学家屠呦呦发现了青蒿素,开创了疟疾治疗新方法,她因此荣获2015年诺贝尔生理学或医学奖。已知:
①青蒿素由C、H、O元素组成,是无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为156℃~157℃。
②乙醚的沸点为34.5℃。③从青蒿中提取青蒿素的方法之一是以萃取原理为基础,主要有乙醚浸取法和汽油浸取法。
Ⅰ.实验室用乙醚提取青蒿素流程如图1所示。_______ 。
(2)操作Ⅱ的名称为_______ 。
(3)操作Ⅲ的主要过程可能是_______ (填字母)。
A.加入乙醚进行萃取、分液
B.加入95%的乙醇,浓缩、结晶、过滤
C.加水溶解,蒸发浓缩、冷却结晶,过滤
Ⅱ.用如图2所示实验装置测定青蒿素实验式方法如下:将14.1g青蒿素样品放在装置C硬质玻璃管中,缓缓通入空气数分钟后再充分燃烧,精确测定装置E和F实验前后质量,根据所测数据计算。_______ ;装置F中盛放的物质是_______ 。
(5)该实验装置可能会产生误差,改进方法是_______ 。
(6)用合理改进后的装置进行实验,测得的数据如表所示,通过质谱仪测得青蒿素的相对分子质量是282,结合以上数据,得出青蒿素的分子式为_______ 。
①青蒿素由C、H、O元素组成,是无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为156℃~157℃。
②乙醚的沸点为34.5℃。③从青蒿中提取青蒿素的方法之一是以萃取原理为基础,主要有乙醚浸取法和汽油浸取法。
Ⅰ.实验室用乙醚提取青蒿素流程如图1所示。
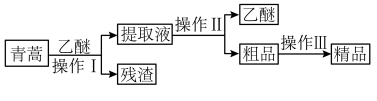
(2)操作Ⅱ的名称为
(3)操作Ⅲ的主要过程可能是
A.加入乙醚进行萃取、分液
B.加入95%的乙醇,浓缩、结晶、过滤
C.加水溶解,蒸发浓缩、冷却结晶,过滤
Ⅱ.用如图2所示实验装置测定青蒿素实验式方法如下:将14.1g青蒿素样品放在装置C硬质玻璃管中,缓缓通入空气数分钟后再充分燃烧,精确测定装置E和F实验前后质量,根据所测数据计算。
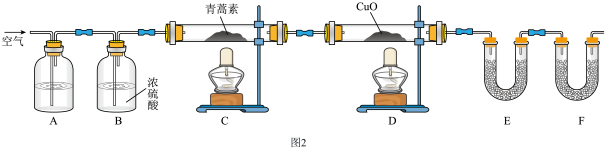
(5)该实验装置可能会产生误差,改进方法是
(6)用合理改进后的装置进行实验,测得的数据如表所示,通过质谱仪测得青蒿素的相对分子质量是282,结合以上数据,得出青蒿素的分子式为
| 装置 | 实验前/g | 实验后/g |
| E | 11.3 | 21.2 |
| F | 40.1 | 73.1 |
更新时间:2023-04-19 21:39:25
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】0.1 mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6 mol,则该烃的分子式为______ 。若该烃能使溴水褪色,且该烃中所有的碳原子都在一个平面上,则该烃的结构简式为________ ,写出该烃在催化剂作用下发生加聚反应的化学方程式_____________________ 。
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐2】(1)燃烧法是测定有机物组成的传统方法。有机物X由C、H、O三种元素组成,经测定其相对分子质量为90。取1.8 g X在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08 g和2.64 g。则有机物X的分子式为__________________ 。
(2)核磁共振谱(NMR)是现代化学测定有机物结构最常用的方法之一。已知(1)中有机物X含有一个—COOH,在1HNMR谱上观察氢原子给出四种特征峰,强度为3∶1∶1∶1。则X的结构简式为___________________________________ 。
(3)X可以在一定条件下生成高分子化合物A,写出A的结构简式____________________ ,由X制得A的反应类型为_____________________________ 。
(2)核磁共振谱(NMR)是现代化学测定有机物结构最常用的方法之一。已知(1)中有机物X含有一个—COOH,在1HNMR谱上观察氢原子给出四种特征峰,强度为3∶1∶1∶1。则X的结构简式为
(3)X可以在一定条件下生成高分子化合物A,写出A的结构简式
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐3】某有机化合物是汽车防冻液的成分之一,经元素分析测定,该有机化合物中各元素的质量分数是:碳38.7%,氢9.7%,氧51.6%。
(1)该有机化合物的实验式为___________ 。
(2)用相对密度法测得该有机化合物的密度是同温同压下氢气密度的31倍,则该物质的相对分子质量为___________ 。
(3)根据该有机化合物的实验式和相对分子质量,推断其分子式___________ 。
(4)该有机化合物的红外光谱中有羟基 和烃基
和烃基 的吸收峰,试写出其可能的结构简式
的吸收峰,试写出其可能的结构简式___________ 。
(1)该有机化合物的实验式为
(2)用相对密度法测得该有机化合物的密度是同温同压下氢气密度的31倍,则该物质的相对分子质量为
(3)根据该有机化合物的实验式和相对分子质量,推断其分子式
(4)该有机化合物的红外光谱中有羟基
 和烃基
和烃基 的吸收峰,试写出其可能的结构简式
的吸收峰,试写出其可能的结构简式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】2008年,三鹿等多家乳制品企业为使蛋白质含量检测合格而加入三聚氰胺,使多名儿童患肾结石,实验室可用下列实验装置测定三聚氰胺的分子式。
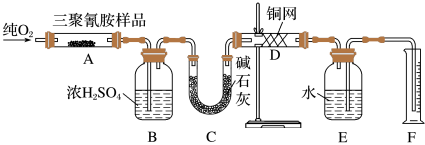
已知三聚氰胺的相对分子质量为126。取1.26 g三聚氰胺样品,放在纯氧中充分燃烧,生成二氧化碳、水、氮气,实验测得装置B增重0.54g,C增重1.32g,排入F中水的体积为672 mL(可按标准状况计算)。
(1)E装置的作用是_____ 。
(2)需要加热的装置是____ (填字母代号)。
(3)装置D的作用是_____ 。
(4)F处读数时应该注意的是____ 、_____ 。
(5)三聚氰胺的分子式为____ 。

已知三聚氰胺的相对分子质量为126。取1.26 g三聚氰胺样品,放在纯氧中充分燃烧,生成二氧化碳、水、氮气,实验测得装置B增重0.54g,C增重1.32g,排入F中水的体积为672 mL(可按标准状况计算)。
(1)E装置的作用是
(2)需要加热的装置是
(3)装置D的作用是
(4)F处读数时应该注意的是
(5)三聚氰胺的分子式为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐2】烃A在标准状况下的密度为1.25g•L﹣1,以A和水煤气(CO、H2)为原料在一定条件 下可获得有机物B、C、D、E,其相互转化关系如图。已知B是CO与H2以物质的量之比为 1:1 反应的产物,E为有浓郁香味、不易溶于水的油状液体。
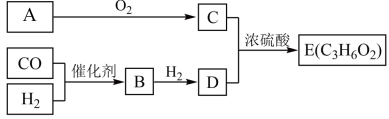
请回答:
(1)有机物C种含有的官能团名称是_____ 。
(2)C+D→E的反应类型是_____ 。
(3)有机物B在一定条件下转化为D的化学方程式是_____ 。
(4)下列说法不正确的是_____ 。
A.有机物D与金属钠反应比水与金属钠反应要剧烈
B.有机物C、D、E可用饱和碳酸钠溶液鉴别
C.实验室制备E时,浓硫酸主要起氧化作用
D.有机物 B、C均能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化

请回答:
(1)有机物C种含有的官能团名称是
(2)C+D→E的反应类型是
(3)有机物B在一定条件下转化为D的化学方程式是
(4)下列说法不正确的是
A.有机物D与金属钠反应比水与金属钠反应要剧烈
B.有机物C、D、E可用饱和碳酸钠溶液鉴别
C.实验室制备E时,浓硫酸主要起氧化作用
D.有机物 B、C均能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】有机物M是一种无色透明的液体,具有香味。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:用李比希法确定M的实验式:这种方法是在电炉加热下用纯氧氧化管内样品,根据产物的质量确定有机物M的组成。_______ (填序号,装置不能重复使用)。
(2)C装置的作用是_______
(3)E装置中反应的化学方程式为_______
(4)F装置(燃烧管)中CuO的作用是_______
若实验中所取纯样品M只含C、H、O三种元素中的两种或三种,准确称取3.70gM,经充分反应后,A管质量增加6.60g,B管质量增加2.70g。
(5)该样品M的实验式为______
步骤二:质谱法确定分子式:
(6)如图是该有机物M的质谱图,则其相对分子质量为_____ ,分子式为_____ 。
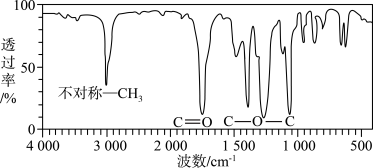
(7)M的核磁共振氢谱有2个峰且面积之比为1:1,利用红外光谱仪测得M的红外光谱如图所示。_______ ,M的结构简式为_______ 。
步骤一:用李比希法确定M的实验式:这种方法是在电炉加热下用纯氧氧化管内样品,根据产物的质量确定有机物M的组成。

(2)C装置的作用是
(3)E装置中反应的化学方程式为
(4)F装置(燃烧管)中CuO的作用是
若实验中所取纯样品M只含C、H、O三种元素中的两种或三种,准确称取3.70gM,经充分反应后,A管质量增加6.60g,B管质量增加2.70g。
(5)该样品M的实验式为
步骤二:质谱法确定分子式:
(6)如图是该有机物M的质谱图,则其相对分子质量为

(7)M的核磁共振氢谱有2个峰且面积之比为1:1,利用红外光谱仪测得M的红外光谱如图所示。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D是中学常见的混合物分离或提纯的基本装置。
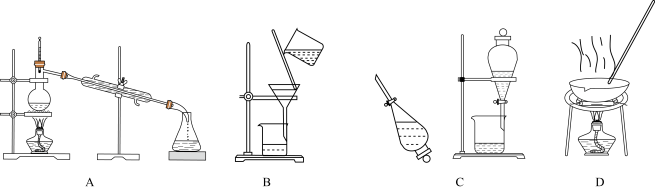
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去Fe(OH)3胶体中悬浮的Fe(OH)3沉淀___ ;
(2)从碘水中提取碘___ ;
(3)用自来水制取蒸馏水___ ;
(4)除去粗盐中的泥沙___ ;
(5)与海水晒盐原理相符的是___ 。

请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去Fe(OH)3胶体中悬浮的Fe(OH)3沉淀
(2)从碘水中提取碘
(3)用自来水制取蒸馏水
(4)除去粗盐中的泥沙
(5)与海水晒盐原理相符的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以离子的形式存在。实验中从海藻提取碘的流程图如下:
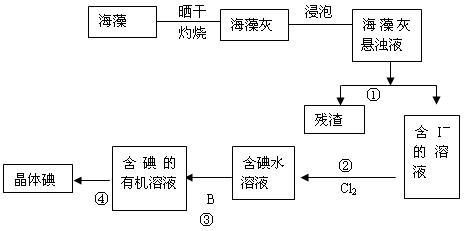
(1)指出提取碘的过程中有关的实验操作名称①_______________ 写出过程②中有关反应的离子方程式:___________________________
(2)提取碘的过程③中可选择的有机试剂为_________
(3)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
______________________________________________________________
(4)在过程④的操作中发现晶体碘大量附着在烧瓶内壁上,是由于碘具有_______ 性质。

(1)指出提取碘的过程中有关的实验操作名称①
(2)提取碘的过程③中可选择的有机试剂为
| A.酒精、四氯化碳 | B.四氯化碳、苯 |
| C.汽油、醋酸 | D.汽油、甘油 |
(4)在过程④的操作中发现晶体碘大量附着在烧瓶内壁上,是由于碘具有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务。
(1)被称作海洋元素的是________ (写元素符号)。
(2)工业上常以食盐为原料制备氯气,再用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式________ 。
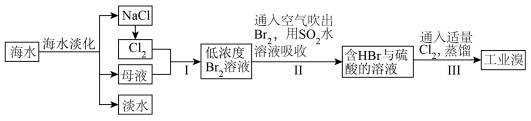
(3)从海水中提取食盐和溴的过程如下:
Ⅰ.①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br¯,其目的为富集溴元素,请写出步骤Ⅱ的化学方程式,________ 。
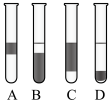
②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为右图中________ 。
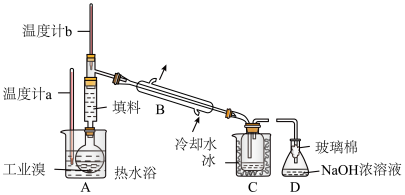
Ⅱ.某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如右装置简图:
请你参与分析讨论:
①实验装置气密性良好,要在C中获得纯净的液溴即达到提纯溴的目的,操作中控制的关键条件是:________ 。
②为除去该产物中仍残留的少量Cl2,可向其中加入________ 溶液,充分反应后,再进行的分离操作是________ 。
(1)被称作海洋元素的是
(2)工业上常以食盐为原料制备氯气,再用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式
(3)从海水中提取食盐和溴的过程如下:

Ⅰ.①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br¯,其目的为富集溴元素,请写出步骤Ⅱ的化学方程式,
②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为右图中

Ⅱ.某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如右装置简图:

请你参与分析讨论:
①实验装置气密性良好,要在C中获得纯净的液溴即达到提纯溴的目的,操作中控制的关键条件是:
②为除去该产物中仍残留的少量Cl2,可向其中加入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
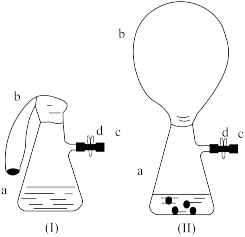
【推荐1】如图(I)中瓶a内放入20mL 6mol∙L−1盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧瓶口和侧口都不漏气。将图(I)的装置在托盘天平上称量,质量为w1g。根据实验现象填空:
(1)把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大,如图(Ⅱ)。反应结束后,再次称量,质量为w2g。则w1和w2的大小关系是____ (不考虑气球浮力的影响)。
(2)实验室需要95mL 6mol∙L−1NaOH溶液,配制时需要NaOH固体___ 克。
①要用到的玻璃仪器有___ ,在操作中,玻璃棒的作用是___ 。
②在操作中出现下列情况会导致所配制的溶液浓度偏低的是___ (填序号)。
①氢氧化钠敞口放置②称量左物右码③转移时有液体溅出④定容时仰视⑤没有烘干容量瓶⑥没有用蒸馏水洗涤烧杯。
(3)取25mL 6mol∙L−1NaOH溶液,先用滴管取少量NaOH溶液,再将滴管插入图(Ⅱ)的胶管c口为便于操作,可以适当倾斜瓶a,注意防止漏气。打开d,将溶液挤入瓶中,立即夹紧d。可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失。用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失。(提示:滴加溶液时会出现局部溶液过浓),写出使沉淀又消失的化学方程式___ 。
(4)将剩余的NaOH溶液全部很快倒入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解,继续轻摇瓶a气球逐渐缩小,直至恢复反应前的下垂状。请写出使“气球缩小,直至恢复下垂状”所发生的反应的化学方程式___ 。
(5)计算标况下气球内最多能产生的气体的体积为____ 毫升。
(1)把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大,如图(Ⅱ)。反应结束后,再次称量,质量为w2g。则w1和w2的大小关系是

(2)实验室需要95mL 6mol∙L−1NaOH溶液,配制时需要NaOH固体
①要用到的玻璃仪器有
②在操作中出现下列情况会导致所配制的溶液浓度偏低的是
①氢氧化钠敞口放置②称量左物右码③转移时有液体溅出④定容时仰视⑤没有烘干容量瓶⑥没有用蒸馏水洗涤烧杯。
(3)取25mL 6mol∙L−1NaOH溶液,先用滴管取少量NaOH溶液,再将滴管插入图(Ⅱ)的胶管c口为便于操作,可以适当倾斜瓶a,注意防止漏气。打开d,将溶液挤入瓶中,立即夹紧d。可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失。用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失。(提示:滴加溶液时会出现局部溶液过浓),写出使沉淀又消失的化学方程式
(4)将剩余的NaOH溶液全部很快倒入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解,继续轻摇瓶a气球逐渐缩小,直至恢复反应前的下垂状。请写出使“气球缩小,直至恢复下垂状”所发生的反应的化学方程式
(5)计算标况下气球内最多能产生的气体的体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某纯碱样品中含有少量NaCl杂质,现用如图所示装置来测定纯碱样品中Na2CO3的质量分数(铁架台、铁夹等在图中均已略去;碱石灰是生石灰与氢氧化钠的混合物,可以吸收水和二氧化碳)。

实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为80.20g;
③准确称得25.00g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入一定量空气;
⑥然后称得干燥管D的总质量为86.80g ;
⑦重复步骤⑤和⑥的操作,直到干燥管D的质量不变,为89.00 g。
试回答:
(1)装置A中试剂X应选用足量的___________
A.饱和NaCl溶液 B.浓H2SO4 C.NaHCO3溶液 D.NaOH溶液
(2)请用文字叙述装置E的作用:___________ 。
(3)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为___________ 。

实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为80.20g;
③准确称得25.00g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入一定量空气;
⑥然后称得干燥管D的总质量为86.80g ;
⑦重复步骤⑤和⑥的操作,直到干燥管D的质量不变,为89.00 g。
试回答:
(1)装置A中试剂X应选用足量的
A.饱和NaCl溶液 B.浓H2SO4 C.NaHCO3溶液 D.NaOH溶液
(2)请用文字叙述装置E的作用:
(3)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】从铜氨废液{含 、
、 、
、 、
、 、
、 、
、 等}中回收铜的工艺流程如图:
等}中回收铜的工艺流程如图:
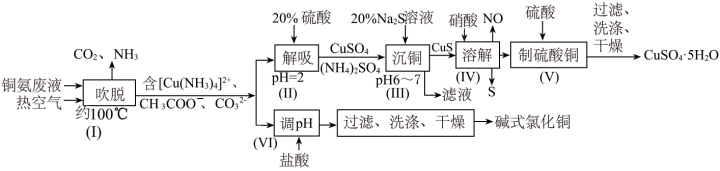
回答下列问题:
(1)步骤(Ⅰ)中被氧化的元素是___________ ,由步骤(Ⅱ)可确定 与
与 的结合能力比与
的结合能力比与 的
的___________ (填“强”或“弱”)。
(2)步骤(Ⅲ)“沉铜”时,利用 溶液而不选用NaOH溶液“沉铜”的优点是
溶液而不选用NaOH溶液“沉铜”的优点是___________ 。
(3)写出步骤(Ⅳ)“溶解”时的化学方程式:___________ ,氧化剂与还原剂的物质的量之比为___________ 。
(4)该流程中可以循环利用的物质是___________ (填化学式)。
(5)碱式氯化铜在400℃时能完全分解为CuO、 和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为
和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为___________ 。
 、
、 、
、 、
、 、
、 、
、 等}中回收铜的工艺流程如图:
等}中回收铜的工艺流程如图:
回答下列问题:
(1)步骤(Ⅰ)中被氧化的元素是
 与
与 的结合能力比与
的结合能力比与 的
的(2)步骤(Ⅲ)“沉铜”时,利用
 溶液而不选用NaOH溶液“沉铜”的优点是
溶液而不选用NaOH溶液“沉铜”的优点是(3)写出步骤(Ⅳ)“溶解”时的化学方程式:
(4)该流程中可以循环利用的物质是
(5)碱式氯化铜在400℃时能完全分解为CuO、
 和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为
和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为
您最近一年使用:0次



