肼(N2H4)暴露在空气中容易爆炸,但利用其作燃料电池是一种理想的电池,具有容量大、能量转化效率高、产物无污染等特点,其工作原理如图所示,下列叙述错误的是
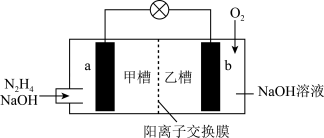

| A.电池工作时,正极附近的pH升高 |
| B.当消耗1molO2时,有2molNa+由甲槽向乙槽迁移 |
| C.负极反应为4OH-+N2H4-4e-=N2+4H2O |
| D.若去掉离子交换膜电池不能正常工作 |
更新时间:2023-04-25 10:16:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】H2S燃料电池应用前景非常广阔,该电池示意图如下。下列说法正确的是
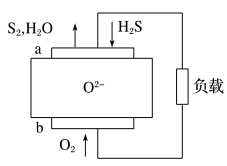

| A.电极a是正极 |
| B.O2-由电极a移向电极b |
| C.电极 a 的反应式为:2H2S+2O2--4e-=S2+2H2O |
| D.当通入1.12LO2,转移电子数0.2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。对该电池的描述合理的是:
①溶液中硫酸的物质的量浓度保持不变;②Cu极上有气泡产生,发生还原反应;③Cu为负极,Zn为正极;④原电池在工作时电子由负极通过溶液流向正极;⑤该装置将化学能转变为电能( )
①溶液中硫酸的物质的量浓度保持不变;②Cu极上有气泡产生,发生还原反应;③Cu为负极,Zn为正极;④原电池在工作时电子由负极通过溶液流向正极;⑤该装置将化学能转变为电能( )
| A.②⑤ | B.①③⑤ | C.②④⑤ | D.④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一种可充电锂-空气电池如图所示。当电池放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是


| A.放电时,多孔碳材料电极为负极 |
| B.放电时,外电路电流由多孔碳材料电极流向锂电极 |
| C.充电时,电解质溶液中Li+向多孔碳材料区迁移 |
D.充电时,电池总反应为Li2O2-x=2Li+(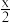 -1)O2 -1)O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某科研小组设计双阴极微生物燃料电池进行同步硝化和反硝化脱氮研究,装置如图所示,下列叙述错误的是

A.“厌氧阳极”的电极反应方程式为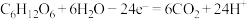 |
| B.电池工作时,“缺氧阴极”电极附近的溶液pH增大 |
| C.该电池工作中“好氧阴极”和“缺氧阴极”之间存在着对电子的竞争作用 |
D.若“好氧阴极” 完全生成 完全生成 ,向该电极输送4 mol电子时消耗的 ,向该电极输送4 mol电子时消耗的 标准状况下的体积为44.8 L 标准状况下的体积为44.8 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
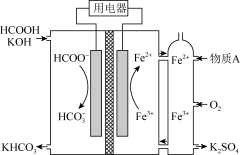
【推荐1】我国科研团队对一种大容量二次电池的研究取得重大突破,该电池因活性物质由外部连续供给而能完成连续放电,其放电时工作原理示意图如图所示。下列说法正确的是
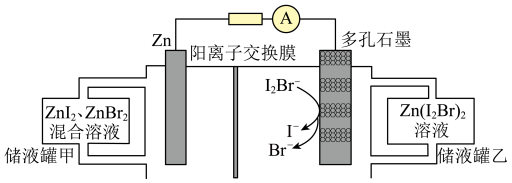

| A.放电时,多孔石墨电极上发生氧化反应 |
| B.放电时,负极区溶液中Zn2+流入储液罐甲 |
| C.充电时,阳极发生的电极反应式为2I-+Br--2e-=I2Br- |
| D.充电时,导线中通过2 mol e-,理论上阴极质量减少65 g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。下列说法正确的是


| A.b为负极,a为正极 |
| B.该电池工作时,内电路中电子由电极a流向电极b |
| C.b极的电极反应为PbO2 + 4H++4e-= Pb2++2H2O |
| D.调节电解质溶液的方法是补充H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】微生物脱盐池的 极上加入了呼吸细菌,工作时可将工业废水中的有机污染物转化为
极上加入了呼吸细菌,工作时可将工业废水中的有机污染物转化为 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是
 极上加入了呼吸细菌,工作时可将工业废水中的有机污染物转化为
极上加入了呼吸细菌,工作时可将工业废水中的有机污染物转化为 ,其工作原理如图所示。下列说法正确的是
,其工作原理如图所示。下列说法正确的是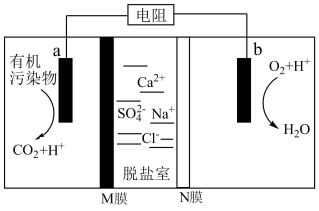
A.工作时, 极发生还原反应,电子从 极发生还原反应,电子从 极流向 极流向 极 极 |
B.若有机物为 ,则 ,则 极的电极反应式为 极的电极反应式为 |
C.在标准状况下, 极上消耗 极上消耗 气体,则通过 气体,则通过 膜的离子的物质的量为 膜的离子的物质的量为 |
D. 膜为阳离子交换膜,脱盐室最终可得到淡盐水 膜为阳离子交换膜,脱盐室最终可得到淡盐水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国科学家研发了一种低成本的铝硫二次电池,以铝箔和多孔碳包裹的 为电极材料,离子液体为电解液。放电时,电池反应为
为电极材料,离子液体为电解液。放电时,电池反应为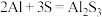 ,电极表面发生的变化如图所示。下列说法错误的是
,电极表面发生的变化如图所示。下列说法错误的是

 为电极材料,离子液体为电解液。放电时,电池反应为
为电极材料,离子液体为电解液。放电时,电池反应为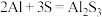 ,电极表面发生的变化如图所示。下列说法错误的是
,电极表面发生的变化如图所示。下列说法错误的是
| A.充电时,阴离子移向铝箔电极 |
B.充电时,阴极反应式为 |
| C.放电时,溶液中离子的总数不变 |
| D.放电时,正极质量增加0.54 g时,电路中通过0.06 mole- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】固体电解质在制造全固态电池、探测器方面应用广泛。一种利用原电池原理测定O2含量的气体传感器示意图如图,RbAg4I5是只能传导Ag+的固体电解质。O2可透过聚四氟乙烯膜,并与AlI3反应生成Al2O3和I2。通过电池电位计的变化可测得O2的含量。下列说法不正确的是
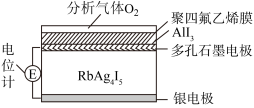

| A.多孔石墨电极上的反应可表示为I2+2Rb++2e-=2RbI |
| B.O2含量的变化会引起电位计示数的变化 |
| C.理论上,每0.1molO2参与反应,银电极质量就减小43.2g |
| D.传感器工作时RbAg4I5晶体中Ag+的量保持不变 |
您最近一年使用:0次


 +H2O
+H2O
 向a极迁移
向a极迁移

