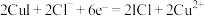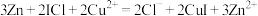我国科学家设计的“海泥电池”,既可用于深海水下仪器的电源补给,又有利于海洋环境污染治理,其中微生物代谢产物显酸性,电池工作原理如图所示。下列说法错误的是
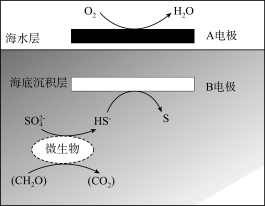
| A.A电极为正极 |
| B.质子从海底沉积层通过交接面向海水层移动 |
| C.负极的电极反应式为CH2O-4e-+H2O=CO2+4H+ |
| D.高温下微生物蛋白质变性失活,故升温不一定能提高电池的效率 |
22-23高一下·四川南充·期中 查看更多[5]
四川省南充市嘉陵第一中学2022-2023学年高一下学期4月期中考试化学试题辽宁省六校协作体2022-2023学年高一下学期期末考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题(已下线)重难点03 原电池原理的应用与化学电源-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)(已下线)重难点03 原电池的工作原理与相关判断-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
更新时间:2023-05-05 08:04:26
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】镍镉电池是一种新型的封闭式小体积的可充电电池,其放电时的工作原理如图所示。下列说法错误的是
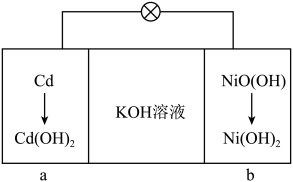

| A.a极为负极 |
B.b极的电极反应式为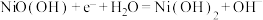 |
| C.负极区pH减小,正极区pH增大 |
D.用该电池作电源电解硫酸铜溶液时,电路中通过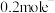 时,阳极产生 时,阳极产生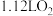 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
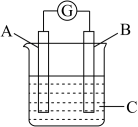
【推荐2】某科学探究小组为探究电化学原理, 设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述错误的是
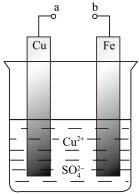

| A.a和b不连接时,铁片上有红色的铜析出 |
| B.a和b用导线连接时, 铜片为负极 |
| C.无论a和b是否连接,反应的本质相同,铁片均会被氧化,溶液中均有Fe2+生成 |
| D.a和b用导线连接时,溶液中的Cu2+应向铜电极移动且能更快地在铜电极上析出铜 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
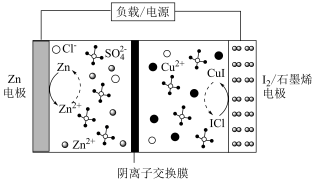
【推荐1】凭借铝的高丰度、低成本、高价态等优点,铝离子电池有望成为下一代储能器件。我国科学家研发的一种新型水系铝离子电池的工作原理如图所示,下列说法错误的是
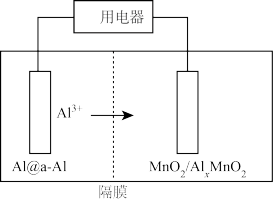

A.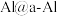 电极上发生氧化反应 电极上发生氧化反应 |
B.正极的反应式为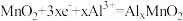 |
| C.隔膜应选用阳离子交换膜 |
D.若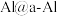 电极质量减小ag,则理论上正极将增重2ag 电极质量减小ag,则理论上正极将增重2ag |
您最近一年使用:0次
【推荐2】研究人员采用双极膜将酸-碱电解液隔离,实现MnO2/Mn2+和Zn/ 的两个溶解/沉积电极氧化还原反应,研制出新型高比能液流电池,其放电过程原理示意图如下:
的两个溶解/沉积电极氧化还原反应,研制出新型高比能液流电池,其放电过程原理示意图如下:
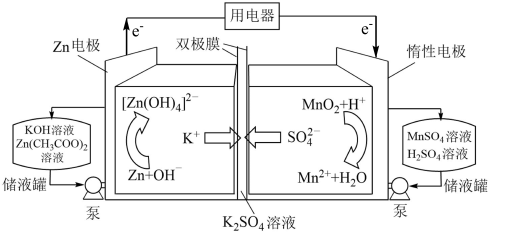
下列说法不正确的是
 的两个溶解/沉积电极氧化还原反应,研制出新型高比能液流电池,其放电过程原理示意图如下:
的两个溶解/沉积电极氧化还原反应,研制出新型高比能液流电池,其放电过程原理示意图如下:
下列说法不正确的是
A.放电过程中,总反应方程式为Zn+MnO2+4OH-+4H+=== +Mn2++2H2O +Mn2++2H2O |
| B.放电过程中,当1molZn参与反应时,理论上有4molK+发生迁移 |
C.充电过程中,阴极的电极反应为 +2e-===Zn+4OH- +2e-===Zn+4OH- |
| D.充电过程中,右侧池中溶液pH逐渐减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】锌空气电池驱动的汽车已用于公共交通,其电极总反应为2Zn + O2→2ZnO。下列说法中,不正确的是
| A.电极反应可通过空气流速控制 |
| B.可使用催化剂加速正极反应 |
| C.为了保存锌空气电池,应在电池负极贴上封条 |
| D.Zn是负极,电极反应为Zn + 2OH-→ZnO+H2O + 2e- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】碱性电池具有容量大、放电电流大的特点,得到广泛应用。锌﹣锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+MnO2(s)+H2O(l)═ZnO(s)+Mn(OH) 2 (s),下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池工作时,电子由负极经过电解质溶液流向正极 |
| C.电池正极的电极反应式为:MnO2(s) +2H2O(l)+2e-═Mn(OH)2 (s)+2OH-(aq) |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
您最近一年使用:0次

 /石墨烯电极消耗
/石墨烯电极消耗