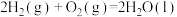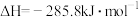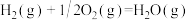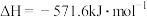下列热化学方程式书写正确的是( 的绝对值均正确)
的绝对值均正确)
 的绝对值均正确)
的绝对值均正确)A.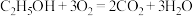  (反应热) (反应热) |
B. 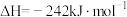 (燃烧热) (燃烧热) |
C. 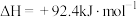 (反应热) (反应热) |
D. 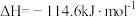 (中和热) (中和热) |
更新时间:2023-05-08 10:31:53
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】沼气是一种能源,它的主要成分是CH4。1.6gCH4完全燃烧生成CO2和液态水时,放出89kJ热量,则下列热化学方程式中正确的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=+890kJ·mol-1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=+890kJ·mol-1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890kJ·mol-1 |
| D.1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(l)ΔH=-890kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905 kJ/mol,则下列说法正确的是
4NO(g)+6H2O(g) ΔH=-905 kJ/mol,则下列说法正确的是
 4NO(g)+6H2O(g) ΔH=-905 kJ/mol,则下列说法正确的是
4NO(g)+6H2O(g) ΔH=-905 kJ/mol,则下列说法正确的是| A.因为该反应为放热反应,所以不用加热就可以快速发生 |
| B.当该反应达到平衡状态后,给容器升温,平衡将逆向移动,导致ΔH增大 |
| C.向密闭容器中投入2mol氨气和足量氧气,充分反应后放出的热量小于452.5kJ |
D.4NO(g)+6H2O(l)  4NH3(g)+5O2(g) ΔH=+905 kJ/mol 4NH3(g)+5O2(g) ΔH=+905 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在下列各说法中,正确的是
| A.ΔH>0表示放热反应,ΔH<0表示吸热反应 |
| B.热化学方程式中的化学计量数只表示物质的量,不可以是分数 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D.1 mol H2与0.5 mol O2反应生成液态水这时的反应热就是H2的燃烧热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是
A.已知: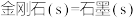 ΔH<0,则该条件下石墨比金刚石稳定 ΔH<0,则该条件下石墨比金刚石稳定 |
B.已知:反应 在室温下能自发进行,则该反应的ΔH>0,ΔS>0 在室温下能自发进行,则该反应的ΔH>0,ΔS>0 |
| C.已知中和热为57.3kJ·mol-1,则稀氨水与盐酸反应生成1mol水时放出的热量大于57.3kJ |
D.已知 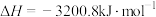 ,则 ,则 燃烧热为3200.8kJ·mol-1 燃烧热为3200.8kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列热化学方程式中,△H能正确表示物质的燃烧热的是
| A.2CO(g) +O2(g) =2CO2(g) △H=—566.0 kJ/mol |
| B.C(s) +1/2O2(g) =CO(g) △H=—110.5 kJ/mol |
| C.CH4(g) +2O2(g)= CO2(g)+2H2O(l) △H=—890.31 kJ/mol |
| D.2C8H18(l) +25O2(g)=16CO2(g)+18H2O(l) △H=—11036 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.甲烷的摩尔燃烧焓为 甲烷完全燃烧放出 甲烷完全燃烧放出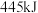 热量时,生成 热量时,生成 个数为 个数为 |
B.氢氧燃料电池中,负极有 气体参与反应时,转移的电子数为 气体参与反应时,转移的电子数为 |
C.氯碱工业中,制备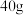 烧碱时阴极生成气体的分子数为 烧碱时阴极生成气体的分子数为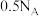 |
D. 和 和 于密闭容器中充分反应后, 于密闭容器中充分反应后, 分子的总数为 分子的总数为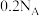 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】25℃、101 kPa时,1.00gCH4完全燃烧生成稳定的化合物放出55.6 kJ热量,下列热化学方程式正确正确的是
| A.CH4 (g) + 2O2 (g) = CO2 (g) +2H2O (g) △H= - 889.6 kJ·mol- 1 |
B. CH4 (g)+ CH4 (g)+  O2 (g) = O2 (g) = CO2 (g)+ CO2 (g)+  H2O(g) △H= -55.6 kJ·mol- 1 H2O(g) △H= -55.6 kJ·mol- 1 |
| C.CH4 (g) + 2O2 (g) =CO2 (g) + 2H2O (1) △H= -889.6 kJ·mol- 1 |
| D.CH4 (g) +2O2 (g) = CO2 (g) + 2H2O (1) △H= +889.6 kJ·mol- 1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列热化学方程式正确的是
| A.已知:S(s)+O2(g)=SO2(g) ΔH1=-Q1 kJ·mol-1,S(g)+O2(g)=SO2(g) ΔH2=-Q2 kJ·mol-1,则Q1<Q2 |
B.500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),达到平衡时放热19.3kJ,其热化学方程式为N2(g)+3H2(g)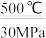 2NH3(g)ΔH=-38.6 kJ·mol-1 2NH3(g)ΔH=-38.6 kJ·mol-1 |
| C.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧热的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| D.25℃、101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法正确的是
A.反应 的 的 可通过下式估算: 可通过下式估算: 反应中断裂旧共价键的键能之和-反应中形成新共价键的键能之和 反应中断裂旧共价键的键能之和-反应中形成新共价键的键能之和 |
B.甲烷的燃烧热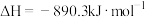 ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为: |
C.由反应 可知,含 可知,含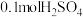 的稀溶液与含 的稀溶液与含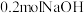 的稀溶液恰好完全反应时,放出 的稀溶液恰好完全反应时,放出 的热量 的热量 |
D.已知 , , ,则 ,则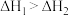 |
您最近一年使用:0次