现有H、N、O、Na、S、Cl、Fe、Cu八种常见元素,回答下列问题:
(1)S在周期表中的位置____________ ;
(2)Na+ 离子的结构示意图为__________________ ;
(3)能说明非金属性Cl比S强的事实是_____________ (用化学方程式表示);
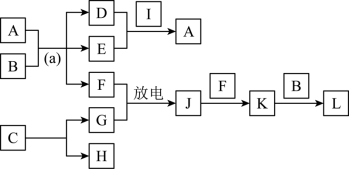
(4)物质A~L是由上述八种元素中的一种、二种或三种组成,A的摩尔质量166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E都为氢氧化物,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如图所示的关系(部分反应条件及产物已略去):
①C的化学式为____________________ ;
②D的电子式为____________________ ;
③L的稀溶液与H反应的离子方程式为___________________________________________ ;
④反应(a)的化学方程式为_________________________________________ 。
(1)S在周期表中的位置
(2)Na+ 离子的结构示意图为
(3)能说明非金属性Cl比S强的事实是
(4)物质A~L是由上述八种元素中的一种、二种或三种组成,A的摩尔质量166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E都为氢氧化物,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如图所示的关系(部分反应条件及产物已略去):

①C的化学式为
②D的电子式为
③L的稀溶液与H反应的离子方程式为
④反应(a)的化学方程式为
更新时间:2023-05-10 21:22:22
|
【知识点】 根据物质性质进行元素种类推断解读
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E、F均为短周期元素,且原子序数依次增大,A是原子半径最小的元素,B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4∶1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成离子个数比为2∶1的离子化合物丙。
(1)E在周期表中的位置为___ 。
(2)下列说法正确的有____ 。
①化合物乙分子中只含有极性共价键
②C、D、E、F原子半径由大到小的顺序为C>D>E>F
③B、E形成的氢化物中,B的氢化物更稳定
④化合物甲和化合物丙都含有离子键和共价键
(3)将F燃烧的产物通入BaCl2和HNO3的混合溶液中,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应_____ 。
(4)写出一个由以上元素构成的10电子微粒与18电子微粒反应的离子方程式____ 。
(5)A与B可形成一种二元化合物X,其中A元素质量分数为2.33%.据研究X显弱酸性。回答:
①X的电离方程式为_____ 。
②X电离的阴离子结构与二氧化碳相似,则其电子式为__ 。
(1)E在周期表中的位置为
(2)下列说法正确的有
①化合物乙分子中只含有极性共价键
②C、D、E、F原子半径由大到小的顺序为C>D>E>F
③B、E形成的氢化物中,B的氢化物更稳定
④化合物甲和化合物丙都含有离子键和共价键
(3)将F燃烧的产物通入BaCl2和HNO3的混合溶液中,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应
(4)写出一个由以上元素构成的10电子微粒与18电子微粒反应的离子方程式
(5)A与B可形成一种二元化合物X,其中A元素质量分数为2.33%.据研究X显弱酸性。回答:
①X的电离方程式为
②X电离的阴离子结构与二氧化碳相似,则其电子式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】A、B、C、D均为中学化学常见的纯净物,且存在如图所示转化关系,其中A是单质。

(1)若A是淡黄色固体,B是气态氢化物,C、D是氧化物,C是造成酸雨的主要物质之一。写出B与C发生反应的化学方程式_________________________ 。
(2)若A、B、D均为两性物质,且A、B生成C的反应均需要强碱溶液。则B生成C的离子反应方程式为________________ ,在A生成C的反应中每消耗1mol还原剂,可生成气体_______________ L(标准状况)。
(3)若组成A、B、C、D的元素为4种短周期元素a、b、c、d,其原子序数逐渐增大,且只有c为金属元素,a、d位于同一主族,b元素原子的最外层电子数是其电子层数的3倍,C、D均为正盐,C是普通玻璃的主要成分之一。则元素d在元素周期表中的位置是________ ,元素a的最高价氧化物对应水化物的水溶液中离子浓度由大到小的顺序为___________ 。

(1)若A是淡黄色固体,B是气态氢化物,C、D是氧化物,C是造成酸雨的主要物质之一。写出B与C发生反应的化学方程式
(2)若A、B、D均为两性物质,且A、B生成C的反应均需要强碱溶液。则B生成C的离子反应方程式为
(3)若组成A、B、C、D的元素为4种短周期元素a、b、c、d,其原子序数逐渐增大,且只有c为金属元素,a、d位于同一主族,b元素原子的最外层电子数是其电子层数的3倍,C、D均为正盐,C是普通玻璃的主要成分之一。则元素d在元素周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C、D、E是短周期元素,其原子序数依次增大,周期表中A与B、C与E相邻;A与E的最外层电子数之比2:3,B的最外层电子数比C的最外层电子数少1个;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红。
(1)E的元素名称是_____ ;该元素在周期表中的位置为______
(2)A、B、C的氢化物稳定性由弱到强的顺序为(用分子式表示)____ ;B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z中所含化学键的类型为 ___
(3)写出D2C2的电子式___ 。用电子式表示只含D、E两种元素的化合物的形成过程_____
(4)写出D2C2与H2O反应的离子方程式_________ 。
(5)将化合物BH3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式_______ 。
(1)E的元素名称是
(2)A、B、C的氢化物稳定性由弱到强的顺序为(用分子式表示)
(3)写出D2C2的电子式
(4)写出D2C2与H2O反应的离子方程式
(5)将化合物BH3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式
您最近一年使用:0次



