 是一种剧毒气体,回收处理的方法之一是先用NaOH溶液吸收
是一种剧毒气体,回收处理的方法之一是先用NaOH溶液吸收 ,然后对吸收液进行再处理,处理原理如图所示。下列说法错误的是
,然后对吸收液进行再处理,处理原理如图所示。下列说法错误的是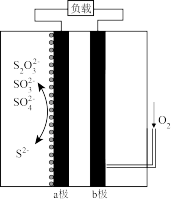
A.b极上的电极反应式为 |
B.工作中b极区 增大 增大 |
C.当电路中有4mol电子通过时,生成的 为0.5mol 为0.5mol |
D.处理 的总反应之一为 的总反应之一为 |
2022·广东·模拟预测 查看更多[2]
更新时间:2023-06-11 09:12:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某污水处理厂利用微生物电池将镀铬废水中的 催化还原,其工作原理如下图所示。下列说法错误的是
催化还原,其工作原理如下图所示。下列说法错误的是
 催化还原,其工作原理如下图所示。下列说法错误的是
催化还原,其工作原理如下图所示。下列说法错误的是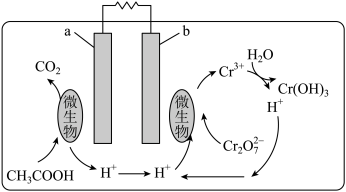
| A.电池工作过程中电子由a极经外电路流向b极 |
B. 极反应式: 极反应式: |
C.电池工作过程中 极区附近溶液的 极区附近溶液的 减小 减小 |
D.每生成33.6L ,则处理1mol ,则处理1mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】习近平总书记提出我国要在2030年实现“碳达峰”,2060年前实现“碳中和”。某科研小组用电化学方法将 转化为CO实现再利用,转化的基本原理如图所示。下列说法不正确的是
转化为CO实现再利用,转化的基本原理如图所示。下列说法不正确的是
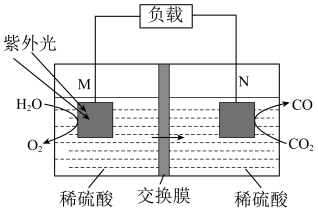
 转化为CO实现再利用,转化的基本原理如图所示。下列说法不正确的是
转化为CO实现再利用,转化的基本原理如图所示。下列说法不正确的是
| A.该装置能将化学能转化为电能 |
B.M上的电极反应方程式为 |
| C.工作一段时间后,N电极室中的溶液pH减小 |
| D.N为正极,电流从N极流出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】含氰化物的废液乱倒或与酸混合,均易生成有剧毒且易挥发的氰化氢。工业上常采用碱性氯化法来处理高浓度氰化物污水,发生的主要反应为:CN-+OH-+Cl2→CO2+N2+Cl-+H2O(未配平)。下列说法错误的是(其中 NA表示阿伏伽德罗常数的值)( )
| A.Cl2是氧化剂,CO2和N2是氧化产物 |
| B.上述离子方程式配平后,氧化剂、还原剂的化学计量数之比为 2:5 |
| C.该反应中,若有1mol CN-发生反应,则有5NA电子发生转移 |
| D.若将该反应设计成原电池,则CN-在负极区发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种向外输出电能的同时,又能使水土中重金属离子Cd2+变成沉淀而被除去的电化学装置,其工作原理如图所示,下列说法正确的是
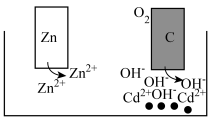

| A.锌棒为该装置的正极 |
| B.电子从锌棒经水土移向碳棒 |
| C.碳棒附近Cd2+转化为Cd而被除去 |
| D.标准状况下,每消耗22.4 LO2,理论上最多能除去2 mol Cd2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】钇稳定氧化锆浓差电池可用于测定待测环境中的含氧量,在冶金、能源等领域也应用广泛,其原理是利用空气与待测环境中氧气的浓度差对电压的影响,其工作状态如图所示。该电池工作时,下列说法错误的是

| A.空气侧的电极电势高于测量侧的电极电势 |
B. 、 、 移向空气侧 移向空气侧 |
C.电极B发生的反应为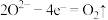 |
| D.若测量侧处于富氧环境中时,电池的正负极可能会发生转换 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】利用微生物电池除去废水中CH3COO-,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水。下列说法错误的是


| A.负极反应为:CH3COO-+2H2O-8e-=2CO2+7H+ |
| B.隔膜1为阴离子交换膜,隔膜2为阳离子交换膜 |
| C.电池工作一段时间后,正、负极产生气体的物质的量之比为1∶1 |
| D.当电路中转移1mol电子时,模拟海水理论上除盐58.5g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】新装修的房屋会释放出有毒的甲醛气体。银-Ferrozine法检测甲醛(HCHO)的原理如下(在原电池中完成氧化银与甲醛的反应)。下列说法正确的是
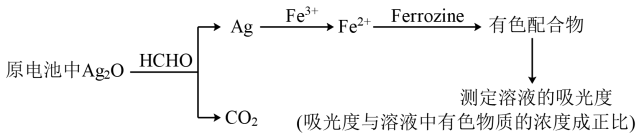

| A.其他条件相同,甲醛浓度越小,所得有色配合物溶液的吸光度越大 |
B.电池正极的电极反应式为Ag2O+2H++2e- 2Ag+H2O 2Ag+H2O |
| C.30g HCHO被氧化时,理论上电路中通过2mol电子 |
| D.理论上,消耗HCHO和消耗Fe3+的物质的量之比为4∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】最近我国科学家研制出一种可充电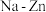 双离子电池体系,其工作原理如图所示。下列说法
双离子电池体系,其工作原理如图所示。下列说法错误 的是
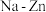 双离子电池体系,其工作原理如图所示。下列说法
双离子电池体系,其工作原理如图所示。下列说法
A.充电时,阴极区溶液的 增大 增大 |
B.放电时,每转移 电子,负极区电解质溶液质量增加 电子,负极区电解质溶液质量增加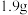 |
C.放电时,正极反应式为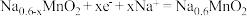 |
D.充电时,若 极质量减少 极质量减少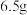 ,则有 ,则有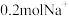 通过阳离子交换膜 通过阳离子交换膜 |
您最近一年使用:0次

 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
 的原电池-电解池组合装置如图所示,已知电极均为惰性电极,下列说法错误的是
的原电池-电解池组合装置如图所示,已知电极均为惰性电极,下列说法错误的是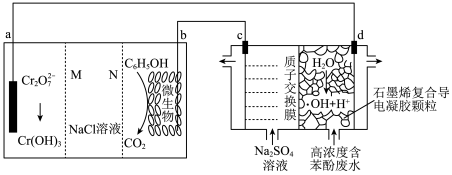
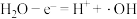
 ,理论上可处理0.1mol苯酚
,理论上可处理0.1mol苯酚

