某校化学探究小组学生进行如下实验,以验证乙酸的酸性比碳酸强,并利用乙醇和乙酸制备乙酸乙酯。
实验I:验证乙酸的酸性比碳酸强
某同学设计如下图所示的实验装置,验证乙酸的酸性强于碳酸。
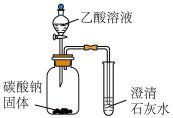
(1)题中涉及反应的离子方程式为_____________ 。
(2)根据实验现象__________ ,确定乙酸的酸性强于碳酸。
(3)另一同学对实验装置提出质疑,其理由是____________ ,应如何改进:__________ 。
实验Ⅱ:制备乙酸乙酯
该小组同学按图所示装置进行实验,以制取乙酸乙酯。
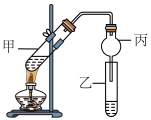
(4)试管甲中依次放入以下液体:①2mL乙醇;②3mL___________ ;③2mL乙酸。为防止试管甲中的液体在实验时暴沸,在加热前还应加入___________ 。
(5)试管乙中盛放的试剂是___________ ,其作用为______________________ 。
(6)装置丙的作用是_________________________________________________ 。
(7)若经分离得到纯乙酸乙酯8.8g,则理论上参加反应的乙醇的质量是___________ g。
实验I:验证乙酸的酸性比碳酸强
某同学设计如下图所示的实验装置,验证乙酸的酸性强于碳酸。

(1)题中涉及反应的离子方程式为
(2)根据实验现象
(3)另一同学对实验装置提出质疑,其理由是
实验Ⅱ:制备乙酸乙酯
该小组同学按图所示装置进行实验,以制取乙酸乙酯。

(4)试管甲中依次放入以下液体:①2mL乙醇;②3mL
(5)试管乙中盛放的试剂是
(6)装置丙的作用是
(7)若经分离得到纯乙酸乙酯8.8g,则理论上参加反应的乙醇的质量是
更新时间:2023-05-15 14:42:09
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】自然界的许多动植物中含有有机酸,例如,蚂蚁体内含有蚁酸(甲酸),菠菜中含有草酸(乙二酸),柑橘中能提取柠檬酸。
(1)甲酸(HCOOH)与乙酸互称为___________ 。
(2)工业上用乙烯合成乙二酸(HOOC—COOH)流程如下:
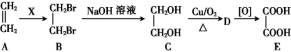
①反应类型:A B为
B为___________ ,B C为
C为___________ 。
②X为___________ (化学式),D为___________ (结构简式)。
(3)与乙酸相似,柠檬酸(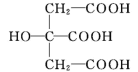 )的酸性比碳酸的强,能与碳酸钠溶液反应放出CO2气体,其反应方程式为
)的酸性比碳酸的强,能与碳酸钠溶液反应放出CO2气体,其反应方程式为___________ 。
(1)甲酸(HCOOH)与乙酸互称为
(2)工业上用乙烯合成乙二酸(HOOC—COOH)流程如下:

①反应类型:A
 B为
B为 C为
C为②X为
(3)与乙酸相似,柠檬酸(
 )的酸性比碳酸的强,能与碳酸钠溶液反应放出CO2气体,其反应方程式为
)的酸性比碳酸的强,能与碳酸钠溶液反应放出CO2气体,其反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某实验小组用如图装置进行乙醇催化氧化的实验。
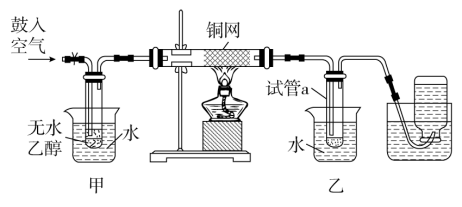
(1)实验过程中铜网出现红色和黑色交替的现象,请按先后顺序写出相应的化学反应方程式_______ 。
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是_______ 反应。
(3)甲和乙两个装置均用水浴加热,作用_______ 相同(填写“是”或“否”),甲的作用是_______ 。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_______ 。要除去该物质,可先在混合液中加入_______ (填字母),然后,再通过_______ (填实验操作名称)即可除去。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳

(1)实验过程中铜网出现红色和黑色交替的现象,请按先后顺序写出相应的化学反应方程式
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是
(3)甲和乙两个装置均用水浴加热,作用
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某化学兴趣小组,设计了如图1所示的实验装置(部分夹持装置未画出),来做乙醇催化氧化的实验,并验证其产物。请填写下列空白:

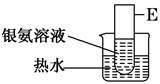
(1)在A处不断鼓入空气的情况下,熄灭B处的酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是_____________ 反应;(填“放热”或“吸热”)
(2)装置D使用冰水进行冷却的目的是___________________ ;
(3)反应开始一段时间,C中观察到的现象是____________________ ;
(4)为检测产物,取出试管a中部分液体,加入银氨溶液,水浴加热,可观察到E试管有银镜产生,说明乙醇的催化氧化产物中存在_____________ ;(填官能团名称)
(5)写出E处反应的化学方程式:_______________________________ 。
(6)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________________ 。要除去该物质,可先在混合液中加入碳酸氢钠溶液,再通过________________ (填实验操作名称)即可分离主要产物。


图1 图2
(1)在A处不断鼓入空气的情况下,熄灭B处的酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是
(2)装置D使用冰水进行冷却的目的是
(3)反应开始一段时间,C中观察到的现象是
(4)为检测产物,取出试管a中部分液体,加入银氨溶液,水浴加热,可观察到E试管有银镜产生,说明乙醇的催化氧化产物中存在
(5)写出E处反应的化学方程式:
(6)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐1】烃A是一种重要的化工原料。已知A在标准 状况下的密度为1.25 g·L-1,B、D是生活中常见的两种有机物。它们之间的转化关系如下图所示:
状况下的密度为1.25 g·L-1,B、D是生活中常见的两种有机物。它们之间的转化关系如下图所示:

请回答:
(1)有机物A的结构简式为________________________ ,有机物C中含有的官能团的名称是________ 。
(2)第③步反应生成D的同时还生成HBr,写出该步反应的化学方程式:___________________ 。
(3)下列说法正确的是________ 。
a.石油裂解是工业上大量获得烃A的主要方法
b.相同条件下,有机物B与钠反应比水与钠反应更剧烈
c.用浓NaOH溶液可除去混在乙酸乙酯中的B、D杂质
d.有机物A与D在一定条件下生成乙酸乙酯的反应属于加成反应
 状况下的密度为1.25 g·L-1,B、D是生活中常见的两种有机物。它们之间的转化关系如下图所示:
状况下的密度为1.25 g·L-1,B、D是生活中常见的两种有机物。它们之间的转化关系如下图所示:
请回答:
(1)有机物A的结构简式为
(2)第③步反应生成D的同时还生成HBr,写出该步反应的化学方程式:
(3)下列说法正确的是
a.石油裂解是工业上大量获得烃A的主要方法
b.相同条件下,有机物B与钠反应比水与钠反应更剧烈
c.用浓NaOH溶液可除去混在乙酸乙酯中的B、D杂质
d.有机物A与D在一定条件下生成乙酸乙酯的反应属于加成反应
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】如图,是实验室制备乙酸乙酯的装置。a试管中加入3mL95%的乙醇、2mL浓硫酸、2mL冰醋酸;b试管中是饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
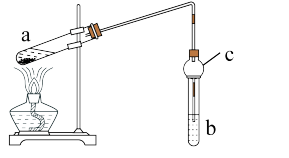
(1)在a试管中除了加入乙醇、浓硫酸和乙酸外,还应放入沸石(或碎瓷片,)目的是_______________ ,浓硫酸的作用是_______________ ,若开始加热后发现忘记加入沸石(或碎瓷片),处理方案是_______________ ;
(2)试管a中发生的主要反应方程式是_______________ ;
(3)c的名称是_______________ ,作用是_______________ ;
(4)饱和Na2CO3溶液的作用是_______________ ;
(5)反应结束后,将试管中收集到的产品倒入分液漏斗中,然后分液,得到乙酸乙酯。

(1)在a试管中除了加入乙醇、浓硫酸和乙酸外,还应放入沸石(或碎瓷片,)目的是
(2)试管a中发生的主要反应方程式是
(3)c的名称是
(4)饱和Na2CO3溶液的作用是
(5)反应结束后,将试管中收集到的产品倒入分液漏斗中,然后分液,得到乙酸乙酯。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】学习小组进行实验研究乙醇的化学性质。
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(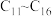 的烷烃)中,现象如下。
的烷烃)中,现象如下。
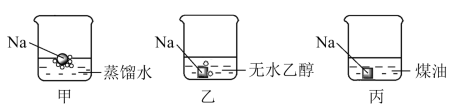
①乙中反应的化学方程式是___________ 。
②对比甲、乙的现象,乙中反应较为___________ (填“剧烈”或“缓慢”),原因是乙醇分子中乙基___________ (填“提高”或“降低”)了O-H键的活性。
(2)利用乙醇制乙烯的发生装置和探究乙烯性质实验装置如下图所示。
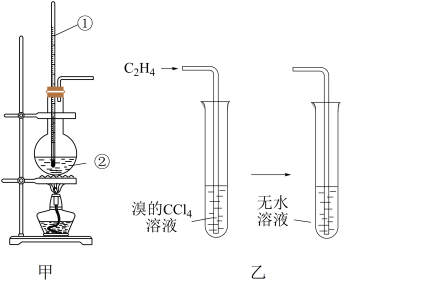
①写出图甲中仪器②中生成乙烯的化学方程式___________ ,该反应属于___________ 反应(填反应类型)。
②向溴的四氯化碳溶液中通入乙烯(图乙),溶液的颜色很快褪去,该反应的化学方程式为___________ ,该反应属于___________ 反应(填反应类型)。
(3)利用以下实验装置探究乙醇的催化氧化性质。
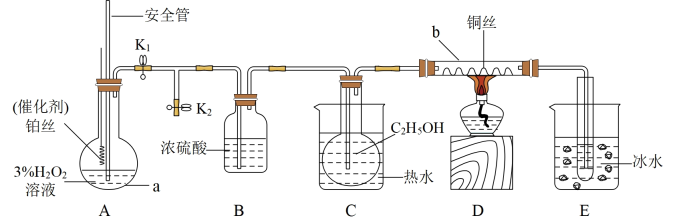
①C中热水的作用是___________ 。
②仪器b中发生反应的化学方程式为___________ 。
(4)该小组的同学利用乙醇制备乙酸乙酯的实验装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。
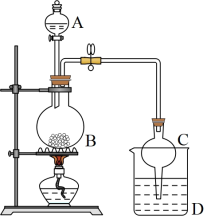
①浓硫酸的作用是___________ ;
②球形干燥管C的作用是___________ 。
③D中饱和 溶液的作用有降低乙酸乙酯的
溶液的作用有降低乙酸乙酯的___________ ;吸收乙醇;除去乙酸。
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(
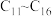 的烷烃)中,现象如下。
的烷烃)中,现象如下。
①乙中反应的化学方程式是
②对比甲、乙的现象,乙中反应较为
(2)利用乙醇制乙烯的发生装置和探究乙烯性质实验装置如下图所示。

①写出图甲中仪器②中生成乙烯的化学方程式
②向溴的四氯化碳溶液中通入乙烯(图乙),溶液的颜色很快褪去,该反应的化学方程式为
(3)利用以下实验装置探究乙醇的催化氧化性质。

①C中热水的作用是
②仪器b中发生反应的化学方程式为
(4)该小组的同学利用乙醇制备乙酸乙酯的实验装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。

①浓硫酸的作用是
②球形干燥管C的作用是
③D中饱和
 溶液的作用有降低乙酸乙酯的
溶液的作用有降低乙酸乙酯的
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某化学兴趣小组的同学利用如图所示实验装置进行实验。

请按要求填空:
(1)利用B装置可制取的气体有_____________ (写出两种即可)。
(2)A、C、D相连后的装置可用于制取 并进行相关的性质实验。
并进行相关的性质实验。
若在C中加入适量水,即可制得氯水。将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如表所示:
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由:__________________________ 。

请按要求填空:
(1)利用B装置可制取的气体有
(2)A、C、D相连后的装置可用于制取
 并进行相关的性质实验。
并进行相关的性质实验。若在C中加入适量水,即可制得氯水。将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如表所示:
实验序号 | 实验操作 | 现象 | 结论 |
Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
Ⅱ | 氯水中加入碳酸氢钠粉末 | 有气泡产生 | 氯气与水反应的产物具有酸性 |
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】利用以下装置完成下列实验(图中a、b、c、d 为止水夹)。

(1)仪器乙的名称_________ 。
(2)装置 A、B、D 相连,可证明 SO2在水中的溶解度,相关操作依次是:制取 SO2,收集 SO2, 关闭止水夹 b、d,打开止水夹 c,_____________ ,
(3)若烧杯中有大量水倒吸入丙试管中,说明 SO2 易溶于水。 装置 A、C 相连,可用于证明C、Si 的非金属性强弱,则试剂甲是_____________ ,C 中 的 现 象 是____________ 。

(1)仪器乙的名称
(2)装置 A、B、D 相连,可证明 SO2在水中的溶解度,相关操作依次是:制取 SO2,收集 SO2, 关闭止水夹 b、d,打开止水夹 c,
(3)若烧杯中有大量水倒吸入丙试管中,说明 SO2 易溶于水。 装置 A、C 相连,可用于证明C、Si 的非金属性强弱,则试剂甲是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】亚硫酰溴(SOBr2)可用作溴化剂,遇水能发生反应。如图为制备SOBr2的装置图(部分夹持仪器已略去),其制备原理为:SOCl2+2HBr=SOBr2+2HCl。

请回答下列问题:
(1)装浓H3PO4的仪器是___ (填名称)。
(2)试剂X可能是___ 。无水CaCl2和试剂X的作用相同,都是___ 。
(3)浓H3PO4与NaBr在加热条件下反应生成HBr,同时还生成磷酸二氢钠,写出该反应的化学方程式:___ 。若将浓H3PO4换为浓H2SO4,得到HBr的量很少,原因是__ 。
(4)装置E中漏斗反扣的目的是___ 。
(5)SOCl2和SOBr2是两种互溶的液体,其沸点分别为75.6℃、146.9℃,将这两种物质分离的方法__ 。

请回答下列问题:
(1)装浓H3PO4的仪器是
(2)试剂X可能是
(3)浓H3PO4与NaBr在加热条件下反应生成HBr,同时还生成磷酸二氢钠,写出该反应的化学方程式:
(4)装置E中漏斗反扣的目的是
(5)SOCl2和SOBr2是两种互溶的液体,其沸点分别为75.6℃、146.9℃,将这两种物质分离的方法
您最近一年使用:0次



