某小组探究一袋 “硫酸亚铁园艺精品肥料”的花肥是否变质并研究其相关性质。首先对该花肥的成分提出假设:
假设I:只含Fe2+;假设II:_______;假设III:只含Fe3+。
(1)假设II是_______ ,假设的依据是_______ (用文字表述)。
取适量花肥于试管中,加入适量稀硫酸溶解得到X溶液,进行如下实验:
(2)实验①发生反应的离子方程式为_______ 。
(3)由实验②可知,X溶液中一定含有_______ (填离子符号)。
为进一步验证假设,该小组又进行如下实验:
(4)通过实验③④可知,假设_______ (填“I”“II”或“III”)成立。
(5)该小组同学根据所学化学知识认为将变质的花肥与维生素C混合后溶于水,仍能正常使用。这是利用了维生素C的_______ (填“氧化性”或“还原性”)。
假设I:只含Fe2+;假设II:_______;假设III:只含Fe3+。
(1)假设II是
取适量花肥于试管中,加入适量稀硫酸溶解得到X溶液,进行如下实验:
| 实验序号 | 实验操作 | 实验现象 |
| ① | 取2 mL X溶液于试管中,滴加几滴酸性KMnO4溶液 | 溶液紫色褪去 |
| ② | 取2 mL X溶液于试管中,滴入1滴KSCN溶液 | 溶液显红色 |
(3)由实验②可知,X溶液中一定含有
为进一步验证假设,该小组又进行如下实验:
| 实验序号 | 实验操作 | 实验现象 |
| ③ | 取2 mL X溶液于试管中,加入1滴KSCN溶液,再加入1 mL H2O | 溶液显红色 |
| ④ | 取2 mL X溶液于试管中,加入1滴KSCN溶液,再加入1 mL新制氯水 | 溶液显红色,且比实验③中的红色深 |
(5)该小组同学根据所学化学知识认为将变质的花肥与维生素C混合后溶于水,仍能正常使用。这是利用了维生素C的
更新时间:2023-05-16 23:23:08
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
真题
【推荐1】聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70 ℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。H2O2氧化Fe2+的离子方程式为________ ;水解聚合反应会导致溶液的pH________ 。
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000 g,置于250 mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2 mol·L−1 K2Cr2O7溶液滴定至终点(滴定过程中 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将________ (填“偏大”或“偏小”或“无影响”)。
②计算该样品中铁的质量分数(写出计算过程)_____ 。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70 ℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。H2O2氧化Fe2+的离子方程式为
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000 g,置于250 mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2 mol·L−1 K2Cr2O7溶液滴定至终点(滴定过程中
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将
②计算该样品中铁的质量分数(写出计算过程)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A是一种常见金属,F是一种红褐色沉淀。根据图中转化关系,回答下列问题。
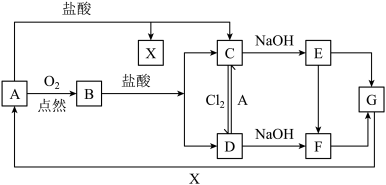
(1)写出F、G的化学式:F.________ ;G._______ 。
(2)检验D中阳离子的方法为_____________________________________________________
(3)保存C溶液时要加固体A的原因是_____________________________________________
(4)写出下列转化的离子方程式:
①B→C:______________________________________________________________________
②C→D:______________________________________________________________________

(1)写出F、G的化学式:F.
(2)检验D中阳离子的方法为
(3)保存C溶液时要加固体A的原因是
(4)写出下列转化的离子方程式:
①B→C:
②C→D:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下图为中学常见物质及其相互转化关系,已知:①A、B为单质,其余都是化合物;②将G放在酒精灯外焰上灼烧,观察到G的焰色为黄色;③E转化为F的现象为白色物质迅速变为灰绿色,最终变为红褐色。(注:s为固体、aq为溶液)

回答下列问题:
(1)推断以下物质的化学式:B_______ ,F_______ ;
(2)G物质中阳离子对应元素在周期表中的位置为第_______ 周期第_______ 族;
(3)写出E→F的化学方程式_______ ;
(4)检验C(aq)中阳离子常用的化学试剂是_______ ;
(5)下列物质中,能将D转化成C的试剂是_______ 。
A.铜粉 B.H2O2溶液 C.CaO固体

回答下列问题:
(1)推断以下物质的化学式:B
(2)G物质中阳离子对应元素在周期表中的位置为第
(3)写出E→F的化学方程式
(4)检验C(aq)中阳离子常用的化学试剂是
(5)下列物质中,能将D转化成C的试剂是
A.铜粉 B.H2O2溶液 C.CaO固体
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】为探究矿石样品A(仅含两种元素)的组成和性质,设计并完成如下实验:
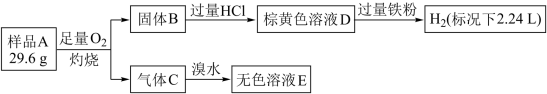
已知溶液D中只含一种金属阳离子,与铁粉充分反应后固体质量减少14 g。
请回答:
(1)样品A的化学式为________________ 。
(2)写出气体c与溴水反应的离子方程式___________________ 。
(3)写出样品A与盐酸发生氧化还原反应的化学方程式____________________ 。

已知溶液D中只含一种金属阳离子,与铁粉充分反应后固体质量减少14 g。
请回答:
(1)样品A的化学式为
(2)写出气体c与溴水反应的离子方程式
(3)写出样品A与盐酸发生氧化还原反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为探究某固体化合物X(仅含两种元素)的组成和性质,设计并完成如下实验。已知无色气体B能形成酸雨。请回答:
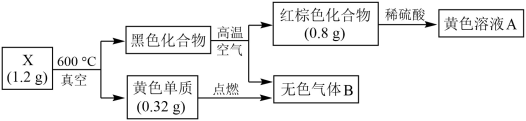
(1)写出一种检验黄色溶液中金属阳离子的试剂的化学式______________ 。
(2)将无色气体B通入黄色溶液A中,发现溶液变成浅绿色。请用离子方程式表示该反应_________ 。
(3)X的化学式是______________ 。

(1)写出一种检验黄色溶液中金属阳离子的试剂的化学式
(2)将无色气体B通入黄色溶液A中,发现溶液变成浅绿色。请用离子方程式表示该反应
(3)X的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某盐M只含有三种元素,某课外兴趣小组为分析其组成,进行了如下实验:
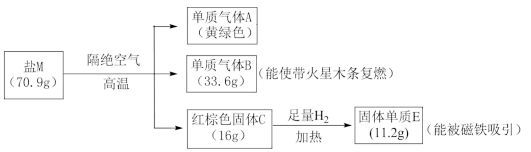
(1)C的化学式是___________ ,A的电子式是___________ 。
(2)M隔绝空气高温分解的化学方程式为___________ 。
(3)某同学取红棕色固体C与一定量的 反应后的固体,溶于足量稀盐酸中,再往其中滴加硫氰化钾溶液,溶液未变红。该同学得出结论:红棕色固体已反应完。你认为该同学的结论是否正确?
反应后的固体,溶于足量稀盐酸中,再往其中滴加硫氰化钾溶液,溶液未变红。该同学得出结论:红棕色固体已反应完。你认为该同学的结论是否正确?___________ (填“是”或“否”),请结合离子方程式说明原因___________ 。

(1)C的化学式是
(2)M隔绝空气高温分解的化学方程式为
(3)某同学取红棕色固体C与一定量的
 反应后的固体,溶于足量稀盐酸中,再往其中滴加硫氰化钾溶液,溶液未变红。该同学得出结论:红棕色固体已反应完。你认为该同学的结论是否正确?
反应后的固体,溶于足量稀盐酸中,再往其中滴加硫氰化钾溶液,溶液未变红。该同学得出结论:红棕色固体已反应完。你认为该同学的结论是否正确?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】工业上可用焦炭、二氧化硅的混合物在高温下与氧气反应生成SiCl4,SiCl4经提纯后用氢气还原得高纯硅。以下是某化学小组制备干燥的氧气并在实验室制备SiCl4的部分装置示意图(注: SiCl4遇水易水解)。
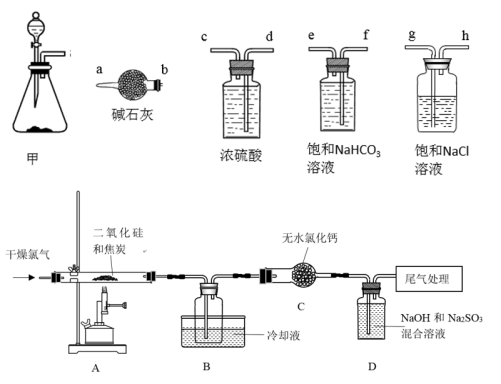
(1)选择上图部分装置,制备纯净干燥的氯气,正确的仪器连接顺序为:发生装置甲→___→____→_____→_____→装置A(用小写字母填空)。_____________
(2)上图C装置的作用是_______________ 。
(3)装置A的硬质玻璃管中二氧化硅和焦炭与氯气恰好完全反应生成SCl4,则二氧化硅和碳的物质的量之比为_________________ 。
(4)经过讨论,该小组认为D中吸收尾气一段时间后,除了过量的OH-,吸收液中阴离子肯定存在Cl-和SO42-,原因是__________ (用离子方程式解释)。
(5)有同学认为可能还存在其它酸根离子(忽略空气中CO2的影响),提出下列假设(不考虑各因素的叠加),假设1:只有SO32-,假设2:只有ClO-,假设3:……
设计实验验证上述假设1和假设2:取少量吸收液于试管中,滴加3mol/LH2SO4至溶液呈酸性,然后将所得溶液分置于a、b两试管中,请填写空白的实验步骤、预期现象。

(1)选择上图部分装置,制备纯净干燥的氯气,正确的仪器连接顺序为:发生装置甲→___→____→_____→_____→装置A(用小写字母填空)。
(2)上图C装置的作用是
(3)装置A的硬质玻璃管中二氧化硅和焦炭与氯气恰好完全反应生成SCl4,则二氧化硅和碳的物质的量之比为
(4)经过讨论,该小组认为D中吸收尾气一段时间后,除了过量的OH-,吸收液中阴离子肯定存在Cl-和SO42-,原因是
(5)有同学认为可能还存在其它酸根离子(忽略空气中CO2的影响),提出下列假设(不考虑各因素的叠加),假设1:只有SO32-,假设2:只有ClO-,假设3:……
设计实验验证上述假设1和假设2:取少量吸收液于试管中,滴加3mol/LH2SO4至溶液呈酸性,然后将所得溶液分置于a、b两试管中,请填写空白的实验步骤、预期现象。
| 实验步骤(简述操作过程) | 预期现象 | 结论 |
| 向a试管中滴加几滴品红溶液,观察现象,加热试管a,观察到 | 假设1成立 | |
| 向b试管中滴加 | 溶液变为蓝色。 | 假设2成立 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】图1、图2分别是甲同学和乙同学设计的制溴苯的装置。已知制备溴苯的反应是放热反应。
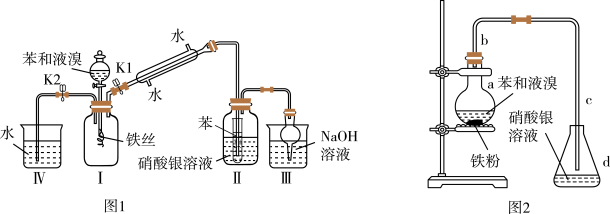
通过分析回答下列问题:
(1)实验室制溴苯的化学反应方程式为:________________________________ 。
(2)实验时,图1中看到的现象有:
①______________________________________________________ 。
②______________________________________________________ 。
(3)图2的操作和现象:
①中先关闭K2,开启K1和漏斗活塞滴加苯和液溴的混合液反应开始,观察到:____________________________________ 。
②关闭K1和漏斗活塞,开启K2发现___________________________________ 。
(4)比较两装置,图2优于图1有(答出主要的三点):
①______________________________________________________ 。
②______________________________________________________ 。
③______________________________________________________ 。

通过分析回答下列问题:
(1)实验室制溴苯的化学反应方程式为:
(2)实验时,图1中看到的现象有:
①
②
(3)图2的操作和现象:
①中先关闭K2,开启K1和漏斗活塞滴加苯和液溴的混合液反应开始,观察到:
②关闭K1和漏斗活塞,开启K2发现
(4)比较两装置,图2优于图1有(答出主要的三点):
①
②
③
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】甘氨酸亚铁晶体是一种新型的固体整合补铁剂。其实验室合成路线为:
铁片


 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品 甘氨酸亚铁晶体纯品
甘氨酸亚铁晶体纯品
已知:
相关物质的信息如下表所示
(一) 固体的制备
固体的制备
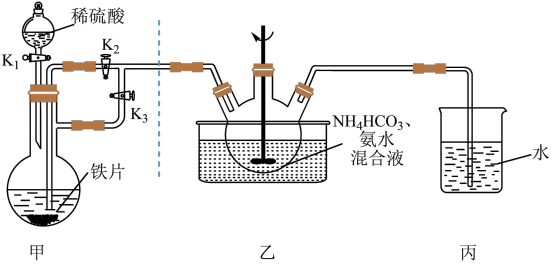
(1)实验开始时应先开 和
和_______ ,关_______ (填“ ”或“
”或“ ”)一段时间后,改变开关状态,生成
”)一段时间后,改变开关状态,生成 。
。
(2)三颈瓶中生成 的离子方程式为
的离子方程式为_______ 。
(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的 溶液调节
溶液调节 为5左右,
为5左右, 过高或过低都会使产率下降,原因是
过高或过低都会使产率下降,原因是_______ 。
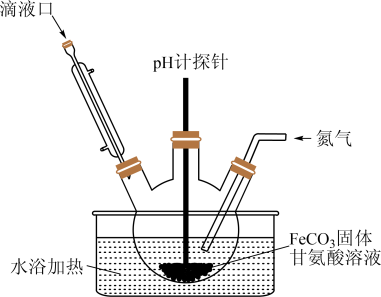
(4)当 固体完全溶解后,再通过滴液口加入乙醇,其作用是
固体完全溶解后,再通过滴液口加入乙醇,其作用是_______ 。
(5)反应结束后,过滤出产品粗品,依次用_______ 、_______ (填序号)洗涤,再经过一系列操作得纯品。
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800g于锥形瓶中,加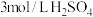 溶液15mL将样品溶解完全后,加入指示剂,立即用
溶液15mL将样品溶解完全后,加入指示剂,立即用 标准液滴定至终点,用去标准液20.20mL(反应为
标准液滴定至终点,用去标准液20.20mL(反应为 )。
)。
步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20mL。
回答下列问题:
(6)滴定时应选择_______ 滴定管。
(7)甘氨酸亚铁晶体中 的质量分数为
的质量分数为_______ %(保留小数点后一位)。
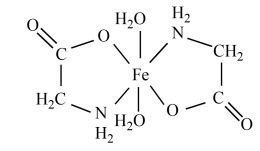
(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有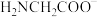 和
和 且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则
且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则 的配位数为
的配位数为_______ 。
铁片



 甘氨酸亚铁晶体粗品
甘氨酸亚铁晶体粗品 甘氨酸亚铁晶体纯品
甘氨酸亚铁晶体纯品已知:
相关物质的信息如下表所示
| 物质 | 化学式 | 摩尔质量 | 性质 |
| 甘氨酸 |  | 75g/mol | 两性物质,易溶于水,微溶于乙醇 |
| 甘氨酸亚铁晶体 | 易溶于水,溶解度随温度升高而增大:难溶于乙醇,在潮湿的空气中易被氧化 |
 固体的制备
固体的制备
(1)实验开始时应先开
 和
和 ”或“
”或“ ”)一段时间后,改变开关状态,生成
”)一段时间后,改变开关状态,生成 。
。(2)三颈瓶中生成
 的离子方程式为
的离子方程式为(二)甘氨酸亚铁的制备
(3)用如图装置制备甘氨酸亚铁。反应开始时,先通过滴液口滴入适量的
 溶液调节
溶液调节 为5左右,
为5左右, 过高或过低都会使产率下降,原因是
过高或过低都会使产率下降,原因是
(4)当
 固体完全溶解后,再通过滴液口加入乙醇,其作用是
固体完全溶解后,再通过滴液口加入乙醇,其作用是(5)反应结束后,过滤出产品粗品,依次用
a.热水 b.冰水 c.乙醇
(三)甘氨酸亚铁晶体结构的分析
步骤1:准确称取甘氨酸亚铁晶体纯品0.4800g于锥形瓶中,加
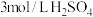 溶液15mL将样品溶解完全后,加入指示剂,立即用
溶液15mL将样品溶解完全后,加入指示剂,立即用 标准液滴定至终点,用去标准液20.20mL(反应为
标准液滴定至终点,用去标准液20.20mL(反应为 )。
)。步骤2:不加产品,重复步骤1操作,滴定至终点,用去标准液0.20mL。
回答下列问题:
(6)滴定时应选择
(7)甘氨酸亚铁晶体中
 的质量分数为
的质量分数为(8)进一步分析表明:甘氨酸亚铁晶体中,阴阳离子只有
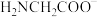 和
和 且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则
且存在五元鳌合环,甘氨酸亚铁晶体的结构简式如下图所示,则 的配位数为
的配位数为
您最近一年使用:0次



