除去下列物质中混有的少量杂质,选用的试剂及操作方法均正确的是
| 选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
| A | 甲烷 | 乙烯 | 通过装有酸性 溶液的洗气装置 溶液的洗气装置 |
| B | 苯 | 苯酚 | 溴水再过滤 |
| C | 乙酸乙酯 | 乙酸 | 加入NaOH溶液后振荡静置,分液 |
| D | 乙醇 | 水 | 加入CaO后再蒸馏 |
| A.A | B.B | C.C | D.D |
更新时间:2023-06-29 15:13:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】实验室欲制备少量乙烯并验证其性质,下列说法中正确的是
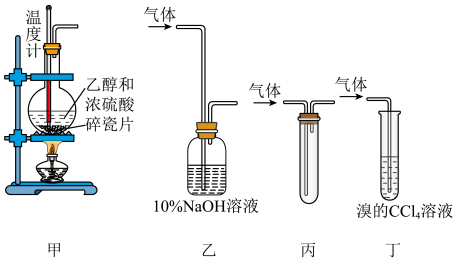
| A.用装置甲制备乙烯 | B.用装置乙除去挥发出来的浓硫酸 |
| C.用装置丙收集乙烯 | D.用装置丁验证乙烯的还原性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A.化合物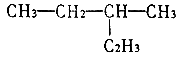 的名称是2-乙基丁烷 的名称是2-乙基丁烷 |
| B.将淀粉在酸性条件下水解后直接加入银氨溶液,水浴加热,检验葡萄糖的生成 |
| C.常温下,乙烯和苯都能被酸性KMnO4氧化,使KMnO4溶液褪色 |
| D.石油裂解、煤的干馏、玉米制醇、颜色反应都是化学变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如表所示,为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是
| 选项 | 待提纯物质 | 除杂试剂 | 分离方法 |
| A | 乙烷(乙烯) | KMnO4(酸化) | 洗气 |
| B | 苯(苯酚) | 浓溴水 | 过滤 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应中,反应类型相同的一组是
| A.由苯制硝基苯;由苯制环己烷 |
| B.乙醇和酸性重铬酸钾溶液;乙炔水化制乙醛 |
| C.乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色 |
| D.乙醇和氢溴酸反应;苯酚和饱和溴水反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
| A.相同物质的量的乙烯和乙醛完全燃烧时,耗氧量相同 |
| B.煤焦油中含有苯和甲苯 |
| C.乙酸乙酯会与水发生水解反应生成乙酸和乙醇 |
| D.苯分子具有平面正六边形结构,分子中6个碳原子之间的键完全相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】除去下列物质中少量杂质(括号内为杂质),所选试剂和分离方法能达到实验目的的是
选项 | 混合物 | 试剂 | 分离方法 |
A | 溴乙烷(溴) |
| 分液 |
B | 甲烷(乙烯) | 酸性 | 洗气 |
C | 乙酸乙酯(乙酸) |
| 蒸馏 |
D | 苯(苯酚) |
| 分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】锌猛干电池是日常生活中常用的一次电池。一种处理废旧干电池的流程如下:
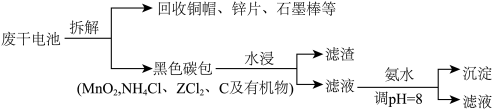
下列叙述错误的是

下列叙述错误的是
| A.合理处理废旧电池有利于保护环境和资源再利用 |
| B.“水浸”后的滤渣干燥后经充分灼烧可回收其中的MnO2 |
| C.“沉淀”反应后的滤液可通过蒸发至干回收NH4Cl |
| D.“沉淀”反应的离子方程式为:Zn2+ + 2NH3·H2O = Zn(OH)2↓ + 2NH4+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用图1所示的装置制备乙酸乙酯,并用图2所示的步骤分离乙酸乙酯、乙醇和乙酸。下列说法错误的是
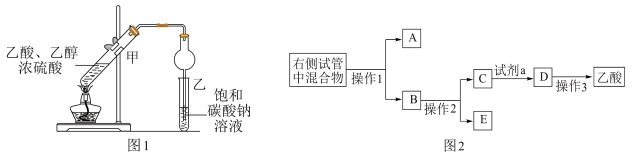

| A.反应试剂的加入顺序为乙醇→浓硫酸→乙酸 |
| B.乙试管内液体不可以用氢氧化钠溶液代替 |
| C.操作1、操作2是分液,操作3是蒸馏 |
| D.A是乙酸乙酯,E是乙醇,试剂a可以是硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】钴配合物[Co(NH3)6]Cl3溶于热水,在冷水中微溶,可通过如下反应制备:2CoCl2+2NH4Cl+10NH3+H2O2 [CO(NH3)6]Cl3+2H2O具体步骤如下:
[CO(NH3)6]Cl3+2H2O具体步骤如下:
①称取2.00gNH4Cl,用5mL水溶解。
②分批加入2.38gCoCl2·6H2O后,将溶液温度降至10℃以下,加入少许活性炭、10mL12mol/L浓氨水,搅拌下逐滴加入10mL0.6mol/L的双氧水。
③加热至55~60℃反应20min,冷却,过滤。
④将滤得的固体转入含有少量盐酸的25mL沸水中,趁热过滤洗涤。
⑤滤液洗涤液转入烧杯,加入4mL浓盐酸,经过一系列操作,最终得到晶体2.0g。
依据上述实验原理,下列说法正确的是
 [CO(NH3)6]Cl3+2H2O具体步骤如下:
[CO(NH3)6]Cl3+2H2O具体步骤如下:①称取2.00gNH4Cl,用5mL水溶解。
②分批加入2.38gCoCl2·6H2O后,将溶液温度降至10℃以下,加入少许活性炭、10mL12mol/L浓氨水,搅拌下逐滴加入10mL0.6mol/L的双氧水。
③加热至55~60℃反应20min,冷却,过滤。
④将滤得的固体转入含有少量盐酸的25mL沸水中,趁热过滤洗涤。
⑤滤液洗涤液转入烧杯,加入4mL浓盐酸,经过一系列操作,最终得到晶体2.0g。
依据上述实验原理,下列说法正确的是
| A.步骤②中逐滴加入10mL0.6mol/L的双氧水做氧化剂且全部反应 |
| B.步骤②中应用冷水浴降温,目的只是为了防止双氧水分解 |
| C.步骤④趁热过滤得到的固体要用冷水洗涤 |
| D.步骤⑤中滤液加入4mL浓盐酸,是为了析出更多的产品 |
您最近一年使用:0次


 溶液
溶液 溶液
溶液

