按照要求回答问题。
(1)硅是无机非金属材料的主角,Si在元素周期表中的位置___________ ,氮化硅是一种性能优异的无机非金属材料,化学式为___________ ,氮原子和硅原子通过___________ (填“离子键”或“共价键”)连接。建筑粘合剂和防火剂硅酸钠,可用 溶解在
溶解在 溶液中制备,反应的离子方程式为
溶液中制备,反应的离子方程式为___________ 。
(2)氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的部分流程图如下___________ 。
②氧化炉中,标准状况下
 转化为
转化为 时转移的电子数目为
时转移的电子数目为___________ 。
③吸收塔中出来的尾气 和
和 ,通过调节其体积比,可用
,通过调节其体积比,可用 溶液完全吸收,生成硫酸盐或亚硝酸盐。
溶液完全吸收,生成硫酸盐或亚硝酸盐。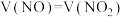 时,发生反应的化学方程式为
时,发生反应的化学方程式为___________ 。标准状况下22.4L仅含 和
和 的混合气被完全吸收,若
的混合气被完全吸收,若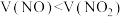 ,消耗
,消耗 的物质的是为
的物质的是为___________  。
。
(1)硅是无机非金属材料的主角,Si在元素周期表中的位置
 溶解在
溶解在 溶液中制备,反应的离子方程式为
溶液中制备,反应的离子方程式为(2)氨和硝酸是重要的化工产品,工业合成氨及制备硝酸的部分流程图如下
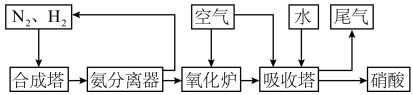
②氧化炉中,标准状况下

 转化为
转化为 时转移的电子数目为
时转移的电子数目为③吸收塔中出来的尾气
 和
和 ,通过调节其体积比,可用
,通过调节其体积比,可用 溶液完全吸收,生成硫酸盐或亚硝酸盐。
溶液完全吸收,生成硫酸盐或亚硝酸盐。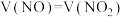 时,发生反应的化学方程式为
时,发生反应的化学方程式为 和
和 的混合气被完全吸收,若
的混合气被完全吸收,若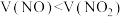 ,消耗
,消耗 的物质的是为
的物质的是为 。
。
更新时间:2023/07/01 16:21:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】填空。
(1)汽车尾气中的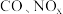 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式:
还原的化学方程式:_______ 。
(2)用氨可将氮氧化物转化为无毒气体。如 ,写出氨气转化
,写出氨气转化 的化学方程式:
的化学方程式:_______ ,该反应中氧化产物与还原产物的质量之比为_______ 。
(3)工业尾气中氮的氧化物常采用碱液吸收法处理。
① 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为
被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
② 与
与 按物质的量之比为
按物质的量之比为 被足量
被足量 溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_______ 。
(1)汽车尾气中的
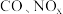 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式:
还原的化学方程式:(2)用氨可将氮氧化物转化为无毒气体。如
 ,写出氨气转化
,写出氨气转化 的化学方程式:
的化学方程式:(3)工业尾气中氮的氧化物常采用碱液吸收法处理。
①
 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为
被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为 ,写出该反应的化学方程式:
,写出该反应的化学方程式:②
 与
与 按物质的量之比为
按物质的量之比为 被足量
被足量 溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
溶液完全吸收后只得到一种钠盐,该钠盐的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨。用化学方程式表示NO2形成酸雨的原因_____________ ,该反应中氧化剂和还原剂的物质的量之比为_______ 。
(2)实验室常用的几种气体发生装置如图A、B、C所示:___________ ;
②如图1是某学生设计收集氨气的几种装置,其中可行的是___________ 。 装置制备氨气,并探究氨气的还原性并检验产物。
装置制备氨气,并探究氨气的还原性并检验产物。________________ 。
②该装置中碱石灰的作用是干燥氨气,无水CuSO4检验反应有水的生成,该装置存在明显缺陷,请提出改进意见_______________ 。
(1)氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨。用化学方程式表示NO2形成酸雨的原因
(2)实验室常用的几种气体发生装置如图A、B、C所示:
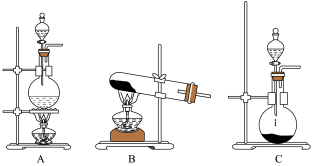
②如图1是某学生设计收集氨气的几种装置,其中可行的是
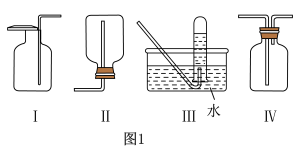
 装置制备氨气,并探究氨气的还原性并检验产物。
装置制备氨气,并探究氨气的还原性并检验产物。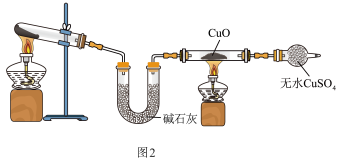
②该装置中碱石灰的作用是干燥氨气,无水CuSO4检验反应有水的生成,该装置存在明显缺陷,请提出改进意见
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①②③是工业生产硝酸的主要途径,线路I、II、III是雷电固氮过程中硝酸的产生途径。
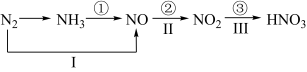
(1)写出各变化的化学方程式,如果属于氧化还原反应,指出其中的氧化剂和还原剂____ 、____ 、____ 、____ 、____ 。
(2)硝酸生产过程中排放出来的一氧化氮是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的条件下,用氨把一氧化氮还原成可直接排入大气的无色无毒气体。请写出有关反应的化学方程式____ 。

(1)写出各变化的化学方程式,如果属于氧化还原反应,指出其中的氧化剂和还原剂
(2)硝酸生产过程中排放出来的一氧化氮是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的条件下,用氨把一氧化氮还原成可直接排入大气的无色无毒气体。请写出有关反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】研究NO、NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)与氮氧化物有关的全球或区域性大气环境问题有_______ (填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2)NO2可与水发生反应,反应的化学方程式为___________ 。若该反应有0.6NA个电子转移,则参加反应的NO2的物质的量为___________ 。
(3)NH3也是重要的含氮化合物,实验室用NH4Cl和Ca(OH)2制取NH3。
①写出反应的化学方程式_________________
②若用下图所示装置收集氨气,气体由_____ 口进入。离子方程式解释 )_____________________
(5)若将12.8 g铜跟一定质量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况),则整个反应过程中,被还原的HNO3总的物质的量是___________ mol。
(1)与氮氧化物有关的全球或区域性大气环境问题有
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2)NO2可与水发生反应,反应的化学方程式为
(3)NH3也是重要的含氮化合物,实验室用NH4Cl和Ca(OH)2制取NH3。
①写出反应的化学方程式
②若用下图所示装置收集氨气,气体由
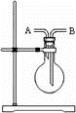
(5)若将12.8 g铜跟一定质量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况),则整个反应过程中,被还原的HNO3总的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“酸酐”是含氧酸脱水后的氧化物,比如SO3是硫酸的酸酐。酸酐与碱反应生成对应的含氧酸盐。NO2可被NaOH完全吸收生成盐,因此被称为______ 酸和______ 酸的“混合酸酐”。1:1的NO、NO2混合气体亦可被NaOH完全吸收生成盐,该混合物相当于______ 酸的酸酐。以上含氧酸中属于弱电解质的是____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对含有氮氧化物的废气进行处理。
(1)用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
在反应①中,被氧化物质是__ 。在反应②中,氧化剂是__ ,每生成1molNaNO3转移电子物质的量是__ 。
(2)汽车尾气中含有一氧化氮和一氧化碳,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成无污染物质,该反应的化学方程式为__ 。
(3)氨气也可用来处理氮氧化物,氨气与二氧化氮发生反应:6NO2+8NH3=7N2+12H2O,若某工厂排出的废气中二氧化氮含量为0.672%(体积分数),处理1×103m3(标准状况)这种废气,需要多少千克氨气?___ (写出计算过程)
(1)用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
在反应①中,被氧化物质是
(2)汽车尾气中含有一氧化氮和一氧化碳,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成无污染物质,该反应的化学方程式为
(3)氨气也可用来处理氮氧化物,氨气与二氧化氮发生反应:6NO2+8NH3=7N2+12H2O,若某工厂排出的废气中二氧化氮含量为0.672%(体积分数),处理1×103m3(标准状况)这种废气,需要多少千克氨气?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氮元素是地球上含量丰富的一种元素,氮单质及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)请写出工业固氮的化学方程式:_______ 。
(2)下列有关氮元素的说法正确的是_______ 。
A.氮气因为其化学性质不活泼,可以作保护气,比如充填食品包装,充填电灯泡等
B.医学上常用液氮作冷冻剂,在冷冻麻醉条件下做手术,是利用氮气化学性质的不活泼性
C.氮、磷、钾是植物生长必需的营养元素
(3)豆科植物种植时不需施加氮肥的原因是_______ 。
(1)请写出工业固氮的化学方程式:
(2)下列有关氮元素的说法正确的是
A.氮气因为其化学性质不活泼,可以作保护气,比如充填食品包装,充填电灯泡等
B.医学上常用液氮作冷冻剂,在冷冻麻醉条件下做手术,是利用氮气化学性质的不活泼性
C.氮、磷、钾是植物生长必需的营养元素
(3)豆科植物种植时不需施加氮肥的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮元素在地球上含量丰富,是构成生命体的基本元素之一。回答下列问题:
(1)下列变化中,属于固氮的是_______ (填字母)。
A.豆科植物把空气中的氮气转化为化合态的氮
B.分离液态空气获得氮气
C.用NH4Cl和熟石灰制备氨气
D.NO2溶于水得到HNO3
E.土壤中的硝酸盐被细菌分解转化为氮气
(2)受到阳光照射浓硝酸会变黄的原因是_______ (用化学方程式表示)。
(3)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题:
①氮氧化物是空气的主要污染物,用碱液脱硝是目前研究的课题之一。将NO2通入氢氧化钠溶液中可得到NaNO3和NaNO2,写出其反应方程式:_______ 。
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:_______ 。
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:_______ (填“正极”或“负极”)。
②电极b的电极反应式为_______ 。
(1)下列变化中,属于固氮的是
A.豆科植物把空气中的氮气转化为化合态的氮
B.分离液态空气获得氮气
C.用NH4Cl和熟石灰制备氨气
D.NO2溶于水得到HNO3
E.土壤中的硝酸盐被细菌分解转化为氮气
(2)受到阳光照射浓硝酸会变黄的原因是
(3)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题:
①氮氧化物是空气的主要污染物,用碱液脱硝是目前研究的课题之一。将NO2通入氢氧化钠溶液中可得到NaNO3和NaNO2,写出其反应方程式:
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH
 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
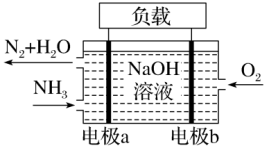
②电极b的电极反应式为
您最近一年使用:0次




